Сенсорная полинейропатия (врожденная нечувствительность к боли) — ДНК-диагностика
Группа редких наследственных заболеваний, основным симптомом которых является потеря глубокой болевой чувствительности
По неврологическим критериям выделяют следующие формы наследственной сенсорной нейропатии:
- НСАН I (OMIM #162400, ген SPTLC1) дистальная потеря чувствительности к боли, тепловой чувствительности, глухота и трофические язвы. Наследуется по аутосомно-доминантному типу.
- НСАН II (OMIM #201300, ген WNK1) характеризуется потерей дистальной болевой чувствительности, снижением тактильной и температурной чувствительности, сохранением проксимальной чувствительности, включая болевую, потерей сухожильных рефлексов, постепенным прогрессированием и деградацией периферических нервов и ганглиев. От НСАН I отличается ранним возрастом манифестации и аутосомно-рецессивным типом наследования.

- НСАН III (семейная дисавтономия OMIM #223900, ген
- НСАН IV (OMIM*191315, ген TRKA) врожденная нечувствительность к боли с нарушением потоотделения, связана с потерей глубокой болевой чувствительности, приводящей к повреждениям членовредительству, остеомиелиту, кроме того, для пациентов характерна умственная недостаточность. Тип наследования – аутосомно-рецессивный.
- НСАН V (OMIM #608654, ген NGF) эта форма характеризуется потерей глубокой болевой и нарушением температурной чувствительности. Снижение глубокой болевой чувствительности приводит к разрушению суставов (сустав Шарко) в детстве.
 Пациенты имеют нормальное умственное развитие, нормальные рефлексы, у них не наблюдается мышечной атрофии и атаксии. У них не нарушены тактильная, вибрационная и баро чувтвительности. Анатомически клинический фенотип связан с сильным уменьшением немиеленизированных и меньшей потерей тонких миелиновых волокон. За эту форму Наследственной сенсорной нейропатии ответственны мутации гена NGF, который кодирует фактор роста нервов. Тип наследования — аутосомно-рецессивный, аутосомно-доминантный (гомозиготных носителей мутации признаки заболевания появляются в раннем детстве, у гетерозигот клинический фенотип проявляется в зрелом возрасте).
Пациенты имеют нормальное умственное развитие, нормальные рефлексы, у них не наблюдается мышечной атрофии и атаксии. У них не нарушены тактильная, вибрационная и баро чувтвительности. Анатомически клинический фенотип связан с сильным уменьшением немиеленизированных и меньшей потерей тонких миелиновых волокон. За эту форму Наследственной сенсорной нейропатии ответственны мутации гена NGF, который кодирует фактор роста нервов. Тип наследования — аутосомно-рецессивный, аутосомно-доминантный (гомозиготных носителей мутации признаки заболевания появляются в раннем детстве, у гетерозигот клинический фенотип проявляется в зрелом возрасте).
В нашей лаборатории разработана прямая ДНК – диагностика двух типов наследственной сенсорной автономной нейропатии II и V типов поиск мутаций в генах WNK1 или NGF методом прямого автоматического секвенирования.
При проведении пренатальной (дородовой) ДНК-диагностики в отношении конкретного заболевания, имеет смысл на уже имеющемся плодном материале провести диагностику частых анеуплоидий (синдромы Дауна, Эдвардса, Шерешевского-Тернера и др), пункт 54. 1. Актуальность данного исследования обусловлена высокой суммарной частотой анеуплоидий — около 1 на 300 новорожденных, и отсутствием необходимости повторного забора плодного материала.
1. Актуальность данного исследования обусловлена высокой суммарной частотой анеуплоидий — около 1 на 300 новорожденных, и отсутствием необходимости повторного забора плодного материала.
| Пункт прейскуранта | Исследование | Цена | Срок исполнения (дней) |
|---|---|---|---|
| 73.6 | Поиск мутаций в гене NGF | 10 800 | 21 |
| 3.61 | Поиск выявленной в данной семье мутации у родственника | 4 800 | 21 |
| 11.7.31 | Пренатальная ДНК-диагностика | 15 000 | 14 |
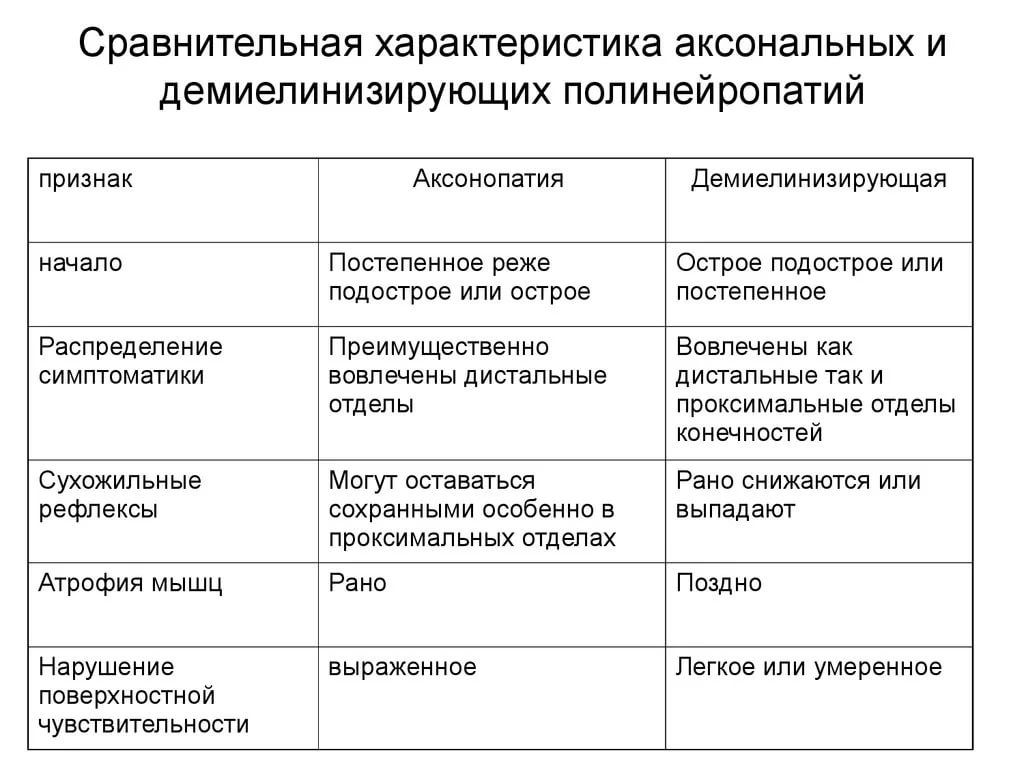
Полинейропатии при соматических заболеваниях: роль невролога в диагностике и лечении | Курушина О.В., Барулин А.Е.
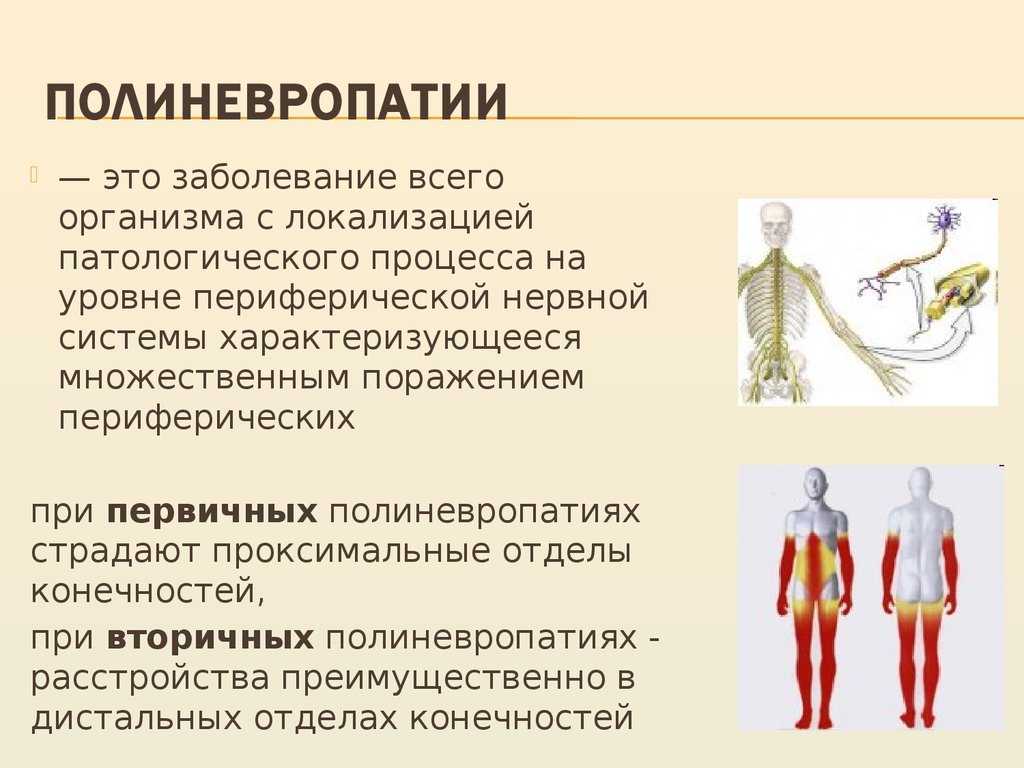
Полинейропатии, или множественные поражения периферических нервов, являются широко распространенными заболеваниями. Высокая подверженность дистальных участков нервов различным патологическим факторам легко объяснима особенностями строения нервных клеток. Питание и остальные метаболические процессы в отростках периферических нервов осуществляются за счет аксоплазматического тока веществ из тела клетки посредством специальной транспортной системы. А так как длина отростков во много тысяч раз превышает размеры самого тела нейрона, то концевые участки нервов являются чрезвычайно уязвимой зоной. При этом основными патогенетическими процессами чаще всего являются аксонопатия или демиелинизация нервных волокон.
Высокая подверженность дистальных участков нервов различным патологическим факторам легко объяснима особенностями строения нервных клеток. Питание и остальные метаболические процессы в отростках периферических нервов осуществляются за счет аксоплазматического тока веществ из тела клетки посредством специальной транспортной системы. А так как длина отростков во много тысяч раз превышает размеры самого тела нейрона, то концевые участки нервов являются чрезвычайно уязвимой зоной. При этом основными патогенетическими процессами чаще всего являются аксонопатия или демиелинизация нервных волокон.
Множество нозологических форм полинейропатий объясняется тем, что, по сути, это заболевание – проявление системного страдания периферической нервной системы при различных неблагоприятных условиях. При этом, несмотря на разнообразие клинических проявлений, синдромальная диагностика полинейропатий не вызывает сложностей. Для синдрома полинейропатии характерно наличие:
– слабости и/или атрофии мышц;
– снижения или выпадения сухожильных рефлексов;
– снижения чувствительности по полинейропатическому типу;
– болевого синдрома в дистальных отделах конечностей;
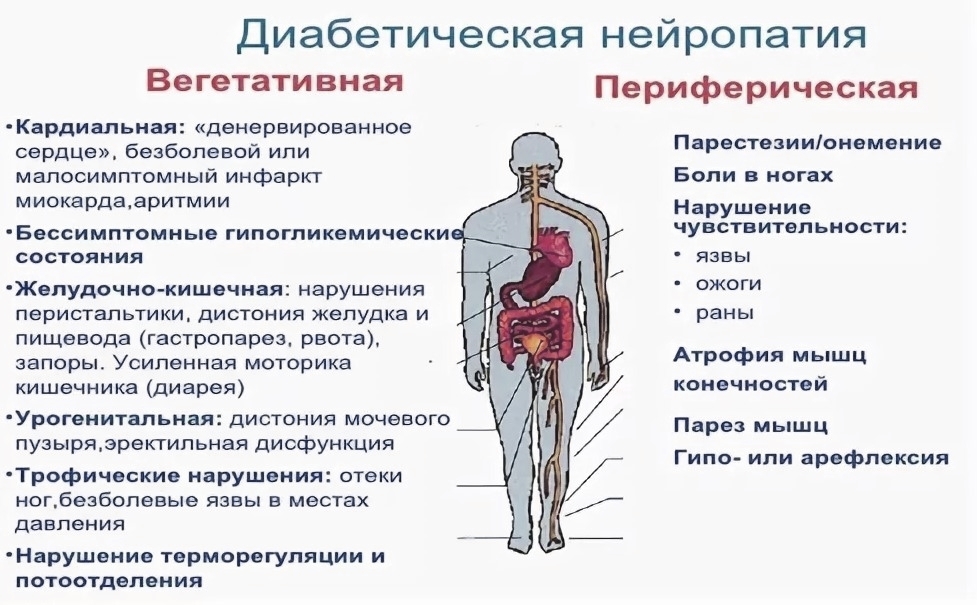
– вегетативных нарушений в виде расстройств деятельности сердечно-сосудистой, мочевыделительной систем, желудочно-кишечного тракта (ЖКТ), потоотделения и сексуальной функции.
Одними из ключевых критериев, позволяющих выделить полинейропатии из всего спектра поражений периферической нервной системы, являются преимущественно дистальное поражение и относительная симметричность патологического процесса.
При этом поиск причины полинейропатии никак нельзя считать избыточным. Неоспоримым фактом является необходимость выделения этиологического фактора как основного определяющего момента для выработки терапевтической стратегии.

Алгоритм диагностики полинейропатий может быть следующим:
1. Сбор анамнеза.
2. Неврологический осмотр.
3. Общий осмотр.
4. Электронейромиография (ЭНМГ).
5. Лабораторные методы исследования.
6. Инструментальные методы исследования.
7. Исследование цереброспинальной жидкости.
8. Биопсия нервов.
При сборе анамнеза в первую очередь необходимо обратить внимание на недавно перенесенные инфекционные заболевания, длительный прием лекарственных средств, условия работы и проживания, в частности, контакт с токсическими веществами. Семейный анамнез, наличие известных соматических заболеваний и особенности питания также являются определяющими факторами диагностического поиска. Ввиду высокой распространенности алкогольной полинейропатии необходимо особое внимание уделить свидетельствам хронической алкогольной интоксикации. Немаловажными диагностическими признаками являются скорость развития симптомов полинейропатии, течение заболевания и их связь с произошедшими жизненными событиями.

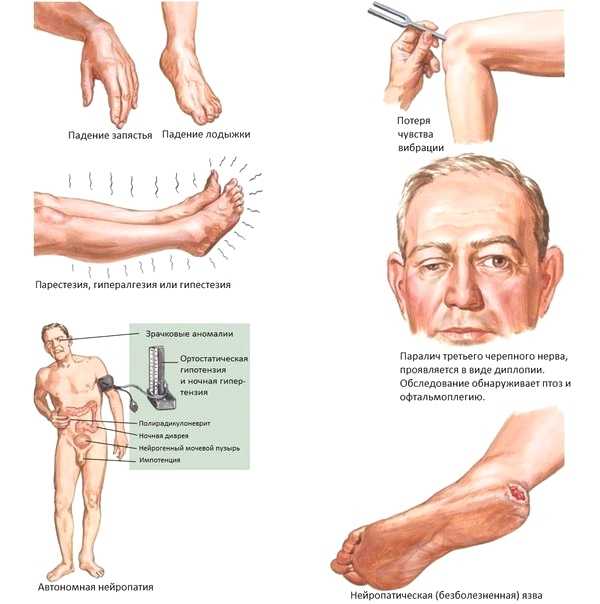
Неврологический осмотр пациента предусматривает как выявление симптомов, характерных для полинейропатий, так и выделение ведущей формы данной патологии. Среди проявлений полинейропатий принято выделять моторные, сенсорные и вегетативные группы признаков. При этом каждая из этих групп может проявляться как негативными, так и позитивными симптомами (табл. 1).
В ходе неврологического осмотра при неясном характере полинейропатии необходима пальпация доступных нервных стволов. Их утолщение может быть свидетельством специфических видов полинейропатий (при лепре, саркоидозе, болезни Рефсума и т.д.). Обследование других систем и функций нервной системы также может дать возможность поставить нозологический диагноз.

ЭНМГ является одним из наиболее чувствительных методов диагностики полинейропатий и помогает выявить даже субклинические формы. В то же время этот метод исследования определяет неспецифические изменения и не может быть единственным при выставлении нозологического диагноза. Стимуляционная ЭНМГ позволяет оценить скорость и качество проведения импульсов по сенсорным и моторным волокнам периферических нервов, что необходимо для определения уровня и характера (аксонопатии или демиелинизации) поражения.
Лабораторные методы исследования направлены на выявление, в первую очередь, метаболических и токсических нарушений у пациента. Кроме клинического анализа крови целесообразно рекомендовать исследование уровня мочевины, креатинина, гликированного гемоглобина, проведение печеночных проб, ревмопроб. При подозрении на интоксикацию необходимо проведение токсикологического скрининга.
При наличии показаний применяются инструментальные методы исследования соматического статуса, которые включают рентгенографию, ультразвуковое исследование и т.
 д. Отдельно следует отметить способы исследования вегетативной нервной системы, из которых наиболее доступной и информативной является кардиоинтервалография. Она позволяет судить как о состоянии вегетативной иннервации, так и об эффективности ее регулирующего влияния.
д. Отдельно следует отметить способы исследования вегетативной нервной системы, из которых наиболее доступной и информативной является кардиоинтервалография. Она позволяет судить как о состоянии вегетативной иннервации, так и об эффективности ее регулирующего влияния. Исследование цереброспинальной жидкости вынесено отдельным пунктом в алгоритме обследования, поскольку ее проведение показано при подозрении на демиелинизирующую полинейропатию, острую или хроническую, а также при поиске инфекционных агентов или неопластического процесса.

В результате проведенного диагностического процесса, как правило, удается выделить тот или иной вид полинейропатии по одному из предложенных способов классификации. Так, при соматической патологии наиболее часто выделяют следующие виды полинейропатий:
1. Метаболические: уремическая, печеночная, амилоидная.
2. Эндокринные: диабетическая, гипотиреоидная, гипертиреоидная.
3. Токсические: алкогольная, лекарственная, свинцовая, мышьяковая.
4. Инфекционные: дифтерийная, при лепре, СПИДе и т.д.
5. Системные: при системной красной волчанке, узелковом периартериите, склеродермии.
6. Паранеопластические.
Краткая клиническая характеристика наиболее часто встречающихся форм полинейропатий
Уремическая полинейропатия встречается практически у половины больных с хронической почечной недостаточностью. Характерны преимущественно сенсорные или сенсомоторные симметричные дистальные нарушения. Заболевание может дебютировать с крампи (болезненные судороги) и синдрома «беспокойных ног».
 Затем присоединяются дизестезии, жжение и онемение стоп. Гемодиализ, проводимый при данной патологии, имеет неоднозначное влияние. С одной стороны, отмечается его положительный эффект на течение полинейропатии, с другой – до четверти пациентов отмечают усиление сенсорных симптомов после начала этого вида терапии. Кроме того, формирование артериовенозной фистулы, ассоциированной с диализом, приводит к нарастанию ишемических механизмов повреждения периферических нервов.
Затем присоединяются дизестезии, жжение и онемение стоп. Гемодиализ, проводимый при данной патологии, имеет неоднозначное влияние. С одной стороны, отмечается его положительный эффект на течение полинейропатии, с другой – до четверти пациентов отмечают усиление сенсорных симптомов после начала этого вида терапии. Кроме того, формирование артериовенозной фистулы, ассоциированной с диализом, приводит к нарастанию ишемических механизмов повреждения периферических нервов. Печеночная полинейропатия возникает как при хроническом, так и при остром поражении печени. Наиболее частыми причинами являются первичный билиарный цирроз, алкогольный цирроз, гепатит С. Клиническая картина чаще всего представлена смешанной сенсо-моторной полинейропатией, которая сочетается с энцефалопатией. Признаки вовлечения вегетативной нервной системы – ортостатическая гипотензия, нарушение моторики ЖКТ – приводят к ухудшению прогноза у этой категории пациентов.
Амилоидная полинейропатия развивается у пациентов с первичным наследственным амилоидозом.
 Проявляется чаще всего болевыми синдромами в сочетании с нарушениями болевой и температурной чувствительности в дистальных отделах конечностей. Моторные и трофические расстройства возникают на поздних стадиях заболевания.
Проявляется чаще всего болевыми синдромами в сочетании с нарушениями болевой и температурной чувствительности в дистальных отделах конечностей. Моторные и трофические расстройства возникают на поздних стадиях заболевания. Диабетическая полинейропатия является наиболее распространенной и изученной формой соматических полинейропатий. Чаще всего представлена в виде дистальной симметричной сенсорной формы, которая отличается медленно прогрессирующим течением, начинается с утраты вибрационной чувствительности и выпадения коленных и ахилловых рефлексов. В то же время может проявляться в виде достаточно интенсивного болевого синдрома, с нарастанием алгий в вечернее и ночное время. Многообразие форм поражения периферической нервной системы при сахарном диабете (СД) не позволяет исключить из списка рассматриваемых полинейропатий и преимущественно вегетативную форму с минимальными сенсорными и моторными нарушениями. Она проявляется периферической вегетативной недостаточностью и помимо снижения качества жизни пациентов существенно ухудшает прогноз в связи с развитием вегетативной кардиальной недостаточности.
 Проксимальная моторная полинейропатия при СД встречается реже и характеризуется амиотрофией, сопровождающейся алгическими нарушениями.
Проксимальная моторная полинейропатия при СД встречается реже и характеризуется амиотрофией, сопровождающейся алгическими нарушениями.Алкогольная полинейропатия часто развивается подостро. Характерными симптомами являются парестезии в дистальных отделах конечностей, болезненность икроножных мышц во время пальпации, нейропатические боли, явления сенситивной атаксии. В дальнейшем развиваются слабость и парез конечностей, в частности при поражении малоберцового нерва с развитием перонеальной походки. Быстро развиваются гипотония, атрофия парализованных мышц. Сухожильные рефлексы сначала могут быть повышенными, а в дальнейшем снижаются или выпадают. Очень часто наблюдаются вазомоторные, трофические и секреторные расстройства: гипергидроз, отек дистальных отделов конечностей, нарушение их нормальной окраски, изменение температуры кожи. В дифференциальной диагностике этой формы полинейропатии большую роль играет ее сочетание с корсаковским синдромом.
Лекарственная полинейропатия развивается на фоне длительного приема целого ряда медикаментов.
 Наиболее часто полинейропатия встречается при приеме изониазида, метронидазола, препаратов золота, кардиологических (амиодарон, гидралазин, пергексилин, новокаинамид), онкологических (винкристин, прокарбазин, цисплатин) препаратов. Главными дифференциально-диагностическими признаками данного вида полинейропатий при всем разнообразии клинической картины являются улучшение состояния после отмены препарата и нарастание симптомов после возобновления терапии.
Наиболее часто полинейропатия встречается при приеме изониазида, метронидазола, препаратов золота, кардиологических (амиодарон, гидралазин, пергексилин, новокаинамид), онкологических (винкристин, прокарбазин, цисплатин) препаратов. Главными дифференциально-диагностическими признаками данного вида полинейропатий при всем разнообразии клинической картины являются улучшение состояния после отмены препарата и нарастание симптомов после возобновления терапии.Свинцовая полинейропатия развивается в основном подостро, на протяжении нескольких недель. Заболеванию предшествуют явления общей астенизации, которые проявляются головной болью, головокружением, повышенной утомляемостью, раздражительностью, нарушением сна, снижением памяти. Клинический рисунок нарушения функции периферических нервов при этой форме полинейропатии характеризуется своеобразием: поражение двигательных волокон лучевых нервов предшествует остальным видам расстройств. Если процесс распространяется на нижние конечности, парализуются прежде всего разгибатели стопы.
 Вместе с параличом дистальных отделов конечностей возникает боль в конечностях и нарушается чувствительность по полиневритическому типу. Течение заболевания обычно длительное – месяцы, а иногда и годы, даже при адекватном лечении, поскольку свинец выводится из организма медленно.
Вместе с параличом дистальных отделов конечностей возникает боль в конечностях и нарушается чувствительность по полиневритическому типу. Течение заболевания обычно длительное – месяцы, а иногда и годы, даже при адекватном лечении, поскольку свинец выводится из организма медленно.Мышьяковая полинейропатия: при повторных воздействиях небольших количеств мышьяка развивается дистальная симметричная сенсомоторная полинейропатия, при которой доминируют боли и нарушения чувствительности. В случае острого отравления развитие клиники полинейропатии следует за латентным периодом в 2–3 нед. При этом мышечная слабость развивается в основном в нижних конечностях. Имеются выраженные вегетативно-трофические расстройства: гиперкератоз, сухость и нарушение пигментации кожи, вазомоторные расстройства, отеки. На ногтях определяют утолщение в виде белой поперечной полоски (полоска Месса). Наблюдаются выпадение волос, трофические расстройства десен и неба (образуются язвы). Восстановление утраченных функций может продолжаться в течение многих месяцев.
 Диагностика строится на выявлении мышьяка в моче, волосах и ногтях.
Диагностика строится на выявлении мышьяка в моче, волосах и ногтях.Дифтерийная полинейропатия обусловлена не воспалительным процессом, а токсическим влиянием коринебактерии дифтерии и аутоимунными сдвигами. Разрушение миелина со следующей дегенерацией нервных волокон начинается из конечных разветвлений нервов в мышцах. Генерализированная форма постдифтерийной полинейропатии развивается на 4–7-й нед., в период угасания инфекции. Проявляется периферическим парезом конечностей с арефлексией, затем присоединяются нарушения поверхностной и глубокой чувствительности с развитием сенситивной атаксии.
Полинейропатия при СПИДе встречается почти у 30% больных. Проявляется, как правило, дистальной симметричной, преимущественно сенсорной формой. Обусловлена в основном аксонопатией. Начинается с выпадения вибрационной чувствительности, характеризуется гипералгезией с выраженным болевым компонентом. Данное состояние может усиливаться при лечении инфекционной или неопластической патологии в связи с развитием лекарственной полинейропатии, к которой данная категория пациентов особенно предрасположена.

Полинейропатии при системных заболеваниях могут быть как обусловлены самим патологическим процессом, так и являться результатом поражения печеночной, почечной систем и проведенного вследствие этого лечения (препараты золота и др.). Могут наблюдаться поражения одного нерва, множественная мононейропатия, симметричная сенсорная или сенсомоторная полинейропатия.
Паранеопластические полинейропатии не являются специфичными и встречаются достаточно редко. Проявляются преимущественно моторными, сенсорными или сенсомоторными симптомами. Для этого вида поражения периферической нервной системы характерно подострое развитие выраженного неврологического дефицита с последующей стабилизацией состояния, сопровождающееся воспалительными изменениями в цереброспинальной жидкости.
Принципы терапии полинейропатий при соматической патологии
Лечебные мероприятия при этой патологии должны проводиться с учетом традиционных направлений терапии: этиологического, патогенетического, симптоматического.

Этиологическое лечение, как следует из названия, будет учитывать ведущий этиологический фактор, вызвавший развитие данного вида полинейропатии. Необходимо отметить тот факт, что в ряде случаев устранение причины заболевания является неотъемлемым условием излечения (как при лекарственной полинейропатии). Но, к сожалению, не всегда это достижимо – например, при СД или системном аутоиммунном заболевании возможен только полноценный контроль симптомов. А иногда, как в случае с интоксикацией мышьяком или при дифтерийной полинейропатии, ведущий патологический фактор уже сыграл свою отрицательную роль, и дальнейшее воздействие на него лишено смысла. Не надо также упускать из внимания тот факт, что достаточно большой процент полинейропатий так и остается несистематизированным. Поэтому этиологическое лечение полинейропатий является желаемым, но не обязательным компонентом лечебного процесса, в отличие от патогенетической терапии.
Для патогенетического лечения необходимо воздействие на основной механизм, послуживший причиной развития полинейропатии.
 В случае демиелинизации и аксонопатии предпочтение отдается витаминотерапии, антиоксидантам и вазоактивным препаратам.
В случае демиелинизации и аксонопатии предпочтение отдается витаминотерапии, антиоксидантам и вазоактивным препаратам.Из широкого спектра антиоксидантов в терапии заболеваний периферических нервов при соматической патологии различного генеза хорошо себя зарекомендовали препараты α-липоевой кислоты. Изучение механизма действия этого вида терапии у больных полинейропатией показало комплексное воздействие на нормализацию эндоневрального кровотока, редукцию оксидативного стресса и улучшение васкулярной дисфункции.
В лечении витаминными комплексами при полинейропатиях предпочтение отдается витаминам группы В. Они оказывают метаболическое влияние на аксональный транспорт и процессы миелинизации в периферических нервных волокнах. Кроме того, воздействие витаминов группы В, в первую очередь тиамина, на центральную нервную систему опосредовано через метаболизм γ-аминомасляной кислоты и серотонина и вызывает анальгетический эффект.
Известно, что тиамин, локализующийся в мембранах нервных клеток, оказывает существенное влияние на процессы регенерации поврежденных нервных волокон, а также участвует в обеспечении энергетических процессов в нервных клетках, нормальной функции аксоплазматического тока.
 Пиридоксин поддерживает синтез транспортных белков в осевых цилиндрах, кроме того, в последние годы доказано, что витамин В6 имеет антиоксидантное действие. Цианокобаламин влияет на мембранные липиды и участвует в биохимических процессах, обеспечивающих нормальный синтез миелина; необходим для нормального кроветворения и созревания эритроцитов, обладает анальгетическим эффектом. Коферментные формы цианокобаламина – метилкобаламин и аденозилкобаламин – необходимы для репликации и роста клеток. В этой связи данные витамины группы В часто называют нейротропными. Комбинация этих витаминов оказывает положительное действие и на сосудистую систему: так, например, комбинация различных витамеров пиридоксина угнетает агрегацию тромбоцитов, реализуя свой эффект опосредованно через активацию рецепторов к простагландину Е.
Пиридоксин поддерживает синтез транспортных белков в осевых цилиндрах, кроме того, в последние годы доказано, что витамин В6 имеет антиоксидантное действие. Цианокобаламин влияет на мембранные липиды и участвует в биохимических процессах, обеспечивающих нормальный синтез миелина; необходим для нормального кроветворения и созревания эритроцитов, обладает анальгетическим эффектом. Коферментные формы цианокобаламина – метилкобаламин и аденозилкобаламин – необходимы для репликации и роста клеток. В этой связи данные витамины группы В часто называют нейротропными. Комбинация этих витаминов оказывает положительное действие и на сосудистую систему: так, например, комбинация различных витамеров пиридоксина угнетает агрегацию тромбоцитов, реализуя свой эффект опосредованно через активацию рецепторов к простагландину Е.Кроме того, недостаток каждого из витаминов группы В может сыграть свою отрицательную роль в формировании клинических проявлений полинейропатий при соматической патологии.
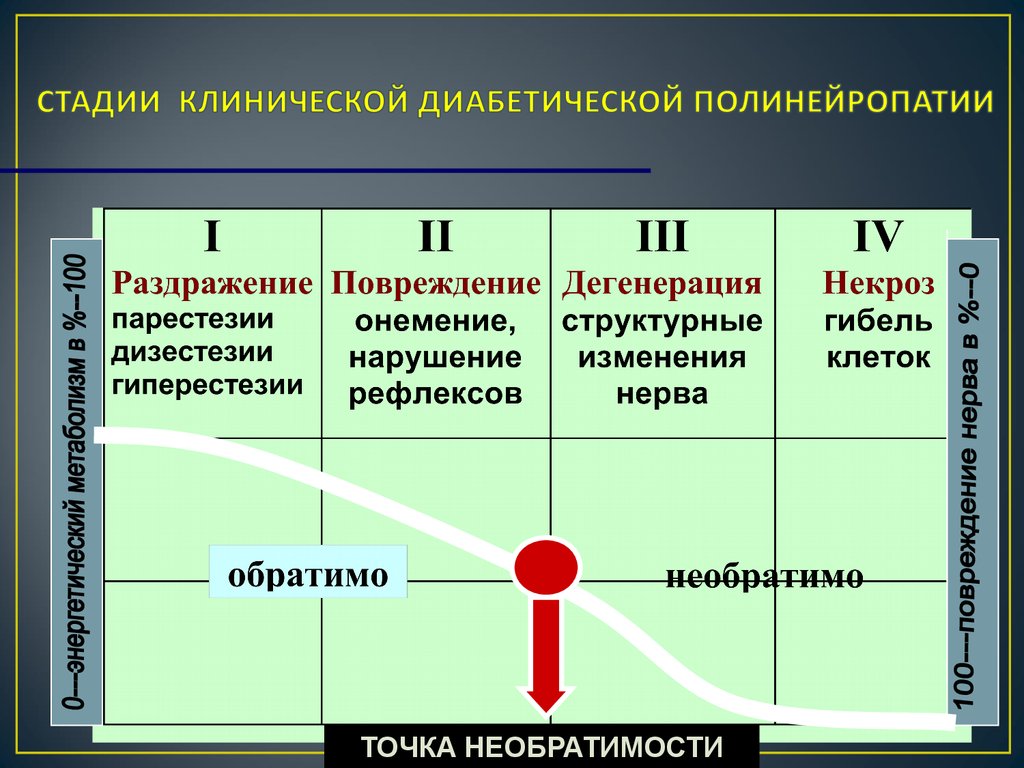
 При хроническом дефиците тиамина в пище развивается дистальная сенсорно-моторная полинейропатия, напоминающая алкогольную и диабетическую полинейропатии. Дефицит пиридоксина приводит к возникновению дистальной симметричной, преимущественно сенсорной полинейропатии, проявляющейся ощущением онемения и парестезиями в виде «покалывания иголками». Недостаток цианокобаламина проявляется в первую очередь пернициозной анемией. У многих больных с дефицитом витамина В12 развивается подострая дегенерация спинного мозга с поражением задних канатиков, а у относительно небольшого числа больных формируется дистальная сенсорная периферическая полинейропатия, характеризующаяся онемением и выпадением сухожильных рефлексов.
При хроническом дефиците тиамина в пище развивается дистальная сенсорно-моторная полинейропатия, напоминающая алкогольную и диабетическую полинейропатии. Дефицит пиридоксина приводит к возникновению дистальной симметричной, преимущественно сенсорной полинейропатии, проявляющейся ощущением онемения и парестезиями в виде «покалывания иголками». Недостаток цианокобаламина проявляется в первую очередь пернициозной анемией. У многих больных с дефицитом витамина В12 развивается подострая дегенерация спинного мозга с поражением задних канатиков, а у относительно небольшого числа больных формируется дистальная сенсорная периферическая полинейропатия, характеризующаяся онемением и выпадением сухожильных рефлексов.Таким образом, применение комплекса витаминов группы В нашло место во многих клинических рекомендациях по лечению полинейропатий. И одним из представителей грамотно составленных поливитаминных препаратов является Нейромультивит. Сочетанное применение тиамина гидрохлорида в дозе 100 мг, пиридоксина гидрохлорида – 200 мг, цианокобаламина – 200 мкг позволяет достичь значительного нейротропного эффекта, приводящего к благоприятным изменениям в метаболизме нервных волокон.
 При полинейропатиях различного генеза применение Нейромультивита способно улучшать как структурное, так и функциональное состояние периферической нервной системы.
При полинейропатиях различного генеза применение Нейромультивита способно улучшать как структурное, так и функциональное состояние периферической нервной системы. Определенным преимуществом обладает и лекарственная форма препарата Нейромультивит – таблетка, покрытая пленочной оболочкой. Для пациентов с комплексной соматической патологией применение инъекционных средств зачастую связано с нарастанием постинъекционных осложнений, болевых ощущений и, как следствие, хронического стресса, который значительно понижает их приверженность к терапии. Прием Нейромультивита 2–3 р./сут во время еды является достаточно удобной формой терапии.
Третье направление терапевтической стратегии – симптоматическое лечение полинейропатий. В этом случае из всего комплекса проблем на первый план выходят нарушения вегетативной функции и болевые синдромы. В ряде случаев противоболевая терапия получает поддержку еще на этапе патогенетического лечения. Так, комплексное применение витаминов группы В оказывает доказанное положительное влияние на антиноцицептивную систему, что является крайне важным при лечении нейропатической боли.
 Коррекция нейропатического болевого синдрома требует применения специфических анальгетиков – антидепрессантов и антиконвульсантов. Но сочетанное влияние витаминов группы В и нестероидных противовоспалительных препаратов способно существенно уменьшить спектр неприятных ощущений. Так, применение препарата Нейродикловит, в котором комплекс витаминов группы В сочетается с диклофенаком (50 мг), успешно приводит к снижению болевых ощущений у пациентов с различными видами полинейропатий.
Коррекция нейропатического болевого синдрома требует применения специфических анальгетиков – антидепрессантов и антиконвульсантов. Но сочетанное влияние витаминов группы В и нестероидных противовоспалительных препаратов способно существенно уменьшить спектр неприятных ощущений. Так, применение препарата Нейродикловит, в котором комплекс витаминов группы В сочетается с диклофенаком (50 мг), успешно приводит к снижению болевых ощущений у пациентов с различными видами полинейропатий. Наиболее сложной клинической задачей является терапия вегетативных нарушений у пациентов с различными видами полинейропатий. При этом прогноз у них существенно ухудшается вследствие именно нарушения вегетативной регуляции – из-за его негативного влияния на работу сердечно-сосудистой системы. Единых рекомендаций по коррекции данных патологических состояний в настоящее время не разработано. В основном отдается предпочтение немедикаментозным методам терапии ортостатической гипотензии.
Таким образом, диагностика и лечение полинейропатий при соматических заболеваниях являются непосредственной задачей врача-невролога, при решении которой возможно влияние как на состояние периферической нервной системы пациента, так и на прогноз ведущего заболевания и качество жизни этой категории больных в целом.
Литература
1. Баранцевич Е.Р., Мельникова Е.В., Скоромец А.А. Патогенетические аспекты неврологических расстройств при сахарном диабете // Ученые записки СПбГМУ им. И.П. Павлова. 1998. Т. 5. № 2. С. 26.
2. Бойко А.Н., Батышева Т.Т., Костенко Е.В., Пивоварчик Е.М., Ганжула П.А., Исмаилов А.М., Лисинкер Л.Н., Хозова А.А., Отческая О.В., Камчатнов П.Р. Нейродикловит: возможность применения у пациентов с болью в спине // Фарматека. 2010. № 7. С. 63–68.
3. Батуева Е.А., Кайгородова Н.Б., Каракулова Ю.В. Влияние нейротрофической терапии не нейропатическую боль и психовегетативный статус больных диабетической нейропатией // Российский журнал боли. 2011. № 2. С. 46.
4. Воробьева О.В. Полинейропатии. Возможности альфа-липоевой кислоты в терапии полинейропатий, ассоциированных с соматическими заболеваниями // Здоровье Украины. 2007. № 6/1. С. 52–53.
5. Курушина О.В., Рыбак В.А., Барулин А.Е., Саранов А.А. Психофизиологические аспекты формирования хронических болевых синдромов // Вестник Волгоградского государственного медицинского университета. 2010. № 02. С. 52–54.
2010. № 02. С. 52–54.
6. Левин О.С. Полинейропатии. М.: МИА, 2005. 496 с.
7. Морозова О.Г. Полинейропатии в соматической практике // Внутренняя медицина. 2007. № 4 (4). С. 37–39.
8. Вгownlee М. Biochemistry and molecular cell biology of diabetic complication // Nature. 2007. Vol. 414 (6865). Р. 613–820.
9. Granados-Soto V., Sanchez-Ramirez G., La-Torre M.R. et al. Effect of diclofenac on the antiallodinic activity of vitamin B12 in a neuropathic pain model in the rat // Proc West Pharmacol Soc. 2004. Vol. 47. P. 92–94.
10. Zambelis T., Karandreas N., Tzavellas E. et al. Large and small fiber neuropathy in chronic alcohol–dependent subject // J Periph Nerv Sys. 2005. Vol. 10. P. 375–338.
Сенсорная невропатия — StatPearls — NCBI Bookshelf
Непрерывное обучение
Сенсорная невропатия — распространенное заболевание, которое часто является прямым осложнением другого сопутствующего заболевания. При определенных обстоятельствах это может быть изнурительным, и требуется более широкое распространение информации во всех областях здравоохранения. В этом мероприятии рассматривается оценка и лечение сенсорной невропатии и подчеркивается роль межпрофессиональной команды в лечении и улучшении ухода за пациентами с этим заболеванием.
В этом мероприятии рассматривается оценка и лечение сенсорной невропатии и подчеркивается роль межпрофессиональной команды в лечении и улучшении ухода за пациентами с этим заболеванием.
Цели:
-
Обобщите этиологию сенсорной невропатии.
-
Объясните общие результаты медицинского осмотра, связанные с сенсорной невропатией.
-
Опишите возможные варианты лечения сенсорной невропатии.
-
Обсудите важность межпрофессиональных командных стратегий для улучшения координации помощи и коммуникации для развития сенсорной невропатии и улучшения исходов.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Сенсорные невропатии относятся к множеству заболеваний, которые приводят к потере чувствительности во всем теле. В совокупности сенсорные невропатии могут быть результатом множества состояний, которые будут обсуждаться в этом обзоре.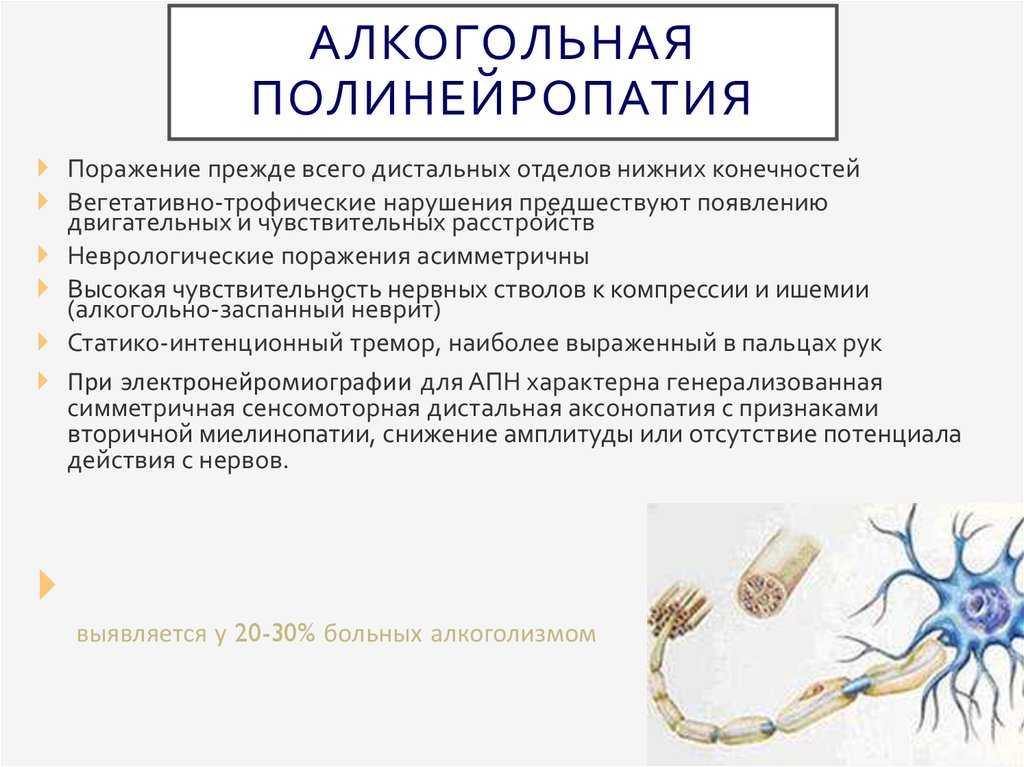 В дальнейшем они могут подразделяться на патологии мелких волокон (с преобладанием боли) и крупных волокон (с преобладанием атаксии).
В дальнейшем они могут подразделяться на патологии мелких волокон (с преобладанием боли) и крупных волокон (с преобладанием атаксии).
При классификации сенсорной невропатии для соответствующего лечения размер нерва и степень миелинизации играют ключевую роль. При оценке невропатий мелких волокон особый интерес представляют мелкие соматические волокна (Аδ и мелкие немиелинизированные С-волокна). Эти волокна передают вредные и тепловые сигналы и регулируют преганглионарную симпатическую и парасимпатическую функции (волокна Aδ), а также постганглионарную вегетативную функцию (волокна C) [1]. Нарушение нормального физиологического состояния этих волокон обычно приводит к жгучей и стреляющей боли с парестезиями.
Напротив, невропатии крупных волокон возникают в результате ослабления волокон Aβ, которые регулируют проприоцептивные сигналы вибрации и прикосновения. Грубо говоря, пациенты с сенсорной атаксией, вероятно, имеют деформацию задних столбов спинного мозга, а также ганглиев задних корешков. [2] Хотя атаксия патогномонична для сенсорной невропатии крупных волокон, может иметь место последующее поражение более мелких волокон. Таким образом, некоторые заболевания могут приводить к полинейропатиям смешанной этиологии, которые состоят как из мелких, так и из крупных волокон (например, сахарный диабет) и представляют собой одну из самых значительных проблем для общественного здравоохранения в современной медицине.
[2] Хотя атаксия патогномонична для сенсорной невропатии крупных волокон, может иметь место последующее поражение более мелких волокон. Таким образом, некоторые заболевания могут приводить к полинейропатиям смешанной этиологии, которые состоят как из мелких, так и из крупных волокон (например, сахарный диабет) и представляют собой одну из самых значительных проблем для общественного здравоохранения в современной медицине.
Этиология
Распознавание различных причинных факторов, непосредственно связанных с сенсорной невропатией, имеет первостепенное значение для обеспечения быстрого и эффективного лечения в качестве клинициста. Чтобы получить более полное представление о возможных основных этиологиях, необходимо рассмотреть следующие процессы, которые включают, но не ограничиваются:
-
Иммуноопосредованные
-
Саркоидоз, синдром Шегрена, системная красная волчанка, целиакия
-
-
Метаболический
-
Сахарный диабет, гиперлипидемия
-
-
Дефицит питательных веществ
-
Витамин B12, медь, витамин E, фолиевая кислота
-
-
Токсичные
-
Химиотерапия, медикаментозная, алкогольная
-
-
Наследственная
-
Гемохроматоз, болезнь Фабри, синдром Элерса-Данлоса, атаксия Фридрейха
-
-
Инфекционный
-
Сифилис, проказа, ВИЧ, гепатит С, криоглобулинемия
-
-
Прочие
-
Идиопатический, фибромиалгия, васкулит [4]
-
значительная часть случаев (от 20 до 30%). [5]
[5]
Эпидемиология
Исследования, в которых оценивалась заболеваемость сенсорной невропатией среди населения в целом, сообщают о распространенности от 1 до 3% с увеличением до 7% у пожилых людей.[5] Также было показано, что в развивающихся странах наблюдается более низкая распространенность, что может быть частично связано с различиями в ожидаемой продолжительности жизни. С глобальной точки зрения чаще всего страдают западные страны, с небольшой предрасположенностью к женщинам.
С точки зрения общественного здравоохранения важно отметить, что сахарный диабет является ведущей причиной периферической невропатии во всем мире.[6] До 50% пожилых пациентов с сахарным диабетом приобретают ту или иную форму дистальной периферической невропатии, которая влияет на их чувство боли и различение температуры [7]. Хирург-ортопед-новатор, доктор Пол Бранд, был известен своей работой по невропатии, вдохновленной работой в Индии, где он заметил, что потеря периферической чувствительности («дар боли») была причиной того, что его пациенты с болезнью Хансена страдали. от сильных рубцов и изъязвлений. Точно так же у диабетиков дистальная периферическая невропатия является одним из основных факторов риска на «пути» к развитию осложнений диабетической стопы.[8]
от сильных рубцов и изъязвлений. Точно так же у диабетиков дистальная периферическая невропатия является одним из основных факторов риска на «пути» к развитию осложнений диабетической стопы.[8]
Анамнез и физикальное исследование
Одним из наиболее отчетливых симптомов сенсорной невропатии является ранняя атаксия. Это проявление в основном связано с нарушением работы афферентных нейронов, передающих импульсы от конечностей тела.[9] Если эти симптомы прогрессируют, результирующие «корчащиеся» движения будут проявляться в руках и ногах, когда пациент закрывает глаза.[10] Положительные сенсорные симптомы также распространены при поражении волокон малого и среднего размера. Классические клинические признаки включают жалобы на «покалывание» и «электричество» в пораженных конечностях, которые напоминают чулки и перчатки. Особенно у людей с диабетом клиницист должен проявлять бдительность при оценке негативных невропатических симптомов, которые проявляются в невропатиях мелких волокон. Онемение, как негативный нейропатический симптом, обычно наблюдается в стопах, не зависит от длины и многоочаговое.
Онемение, как негативный нейропатический симптом, обычно наблюдается в стопах, не зависит от длины и многоочаговое.
При проведении субъективного опроса пациента вариабельность течения заболевания будет значительной. Подострые сенсорные невропатии обычно наблюдаются в иммунно-опосредованных и постинфекционных случаях, тогда как идиопатические варианты оказались более застойными [11]. Во многих случаях двигательная слабость не сопровождает сенсорную невропатию. Однако двигательная активность может быть нарушена у пациентов с паранеопластическими сенсорными нейропатиями, приводящими к отсутствию рефлексов растяжения.
Оценка
Критерии оценки сенсорной невропатии в основном связаны с нейрофизиологическим обследованием и дерматопатологическими исследованиями, такими как биопсия кожи. При диагностике невропатии мелких волокон результаты электромиографии (ЭМГ) могут казаться нормальными, а наличие икроножных и подошвенных реакций не исключает чисто невропатию мелких волокон. В исследованиях ЭМГ сенсорные невропатии демонстрируют сниженный или отсутствующий потенциал действия сенсорного нерва [12]. Пациентам с диабетической периферической сенсорной невропатией часто проводят тест Semmes-Weinstein 5.07 с нейлоновой мононитью в различных местах стопы для проверки защитного порога (формально определяемого как 10 грамм силы).
В исследованиях ЭМГ сенсорные невропатии демонстрируют сниженный или отсутствующий потенциал действия сенсорного нерва [12]. Пациентам с диабетической периферической сенсорной невропатией часто проводят тест Semmes-Weinstein 5.07 с нейлоновой мононитью в различных местах стопы для проверки защитного порога (формально определяемого как 10 грамм силы).
Что касается вегетативных сенсорных тестов, существуют количественные исследования, которые оценивают ощущение тепла и холода, преходящие изменения электрического потенциала кожи (например, активность потовых желез) и неинвазивные исследования электрохимической проводимости кожи для выявления судомоторной дисфункции.[13] ] Для нейропатии с преобладанием мелких волокон одними из наиболее полезных исследований являются терморегуляторные тесты пота и количественный тест судомоторного рефлекса аксонов. Хотя эти исследования недоступны, недавняя литература показывает, что их клинические дополнения обеспечивают более высокий диагностический успех. [14]
[14]
В настоящее время утвержденным золотым стандартом диагностики невропатии мелких волокон является биопсия кожи.[15] В зависимости от исследования чувствительность биопсии кожи может достигать 90 %, а специфичность — до 97 %.[15][16] Преимущества биопсии кожи включают простоту использования и низкую заболеваемость. Общие места приобретения включают дистальную часть ноги, всего 10 см. проксимальнее латеральной лодыжки и латерально дистальнее или проксимальнее бедра.[1] Как правило, биопсия нерва не требуется для диагностики сенсорной невропатии.
Визуализирующие исследования также играют роль в диагностике сенсорных невропатий и наиболее полезны при оценке паранеопластической этиологии. Магнитно-резонансная томография и ее аналоги, инверсионно-восстановительная МРТ-последовательность импульсов и Т2-взвешенная испорченная градиент-эхо-последовательность имеют особое значение для визуализации патологии дорсального столба [17].
Лечение/управление
Руководящих принципов, касающихся конкретных методов лечения сенсорных невропатий, как правило, не существует.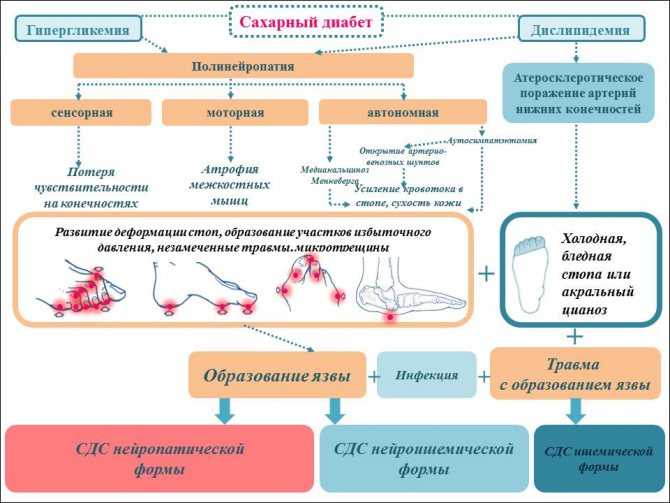 Большая часть данных о лечении основана на мнениях экспертов, а также на хорошо спланированных исследованиях. Некоторые методы лечения включают инъекции внутривенных иммуноглобулинов, метотрексата, кортикостероидов, инфликсимаба и плазмаферез, среди прочего, в зависимости от этиологии.[18] Последние данные свидетельствуют о том, что сенсорная симптоматика обычно выходит на плато через 7–10 месяцев.[19]] Если возможно, протоколы лечения следует начинать в течение этого периода.
Большая часть данных о лечении основана на мнениях экспертов, а также на хорошо спланированных исследованиях. Некоторые методы лечения включают инъекции внутривенных иммуноглобулинов, метотрексата, кортикостероидов, инфликсимаба и плазмаферез, среди прочего, в зависимости от этиологии.[18] Последние данные свидетельствуют о том, что сенсорная симптоматика обычно выходит на плато через 7–10 месяцев.[19]] Если возможно, протоколы лечения следует начинать в течение этого периода.
Эффективность различных пероральных препаратов, таких как противосудорожные средства (прегабалин и окскарбазепин), ингибиторы обратного захвата серотонина и норадреналина (дулоксетин и венлафаксин), трициклические антидепрессанты, опиоиды (трамадол и тапентадол) и ботулинический токсин А (с хемоденервацией и без нее) была продемонстрирована более эффективен, чем плацебо в многочисленных рандомизированных контролируемых исследованиях.[20][21] Местные агенты, такие как лидокаин и капсаицин, были рекомендованы с уровнем доказательности B в соответствии со стандартами Американской академии неврологии.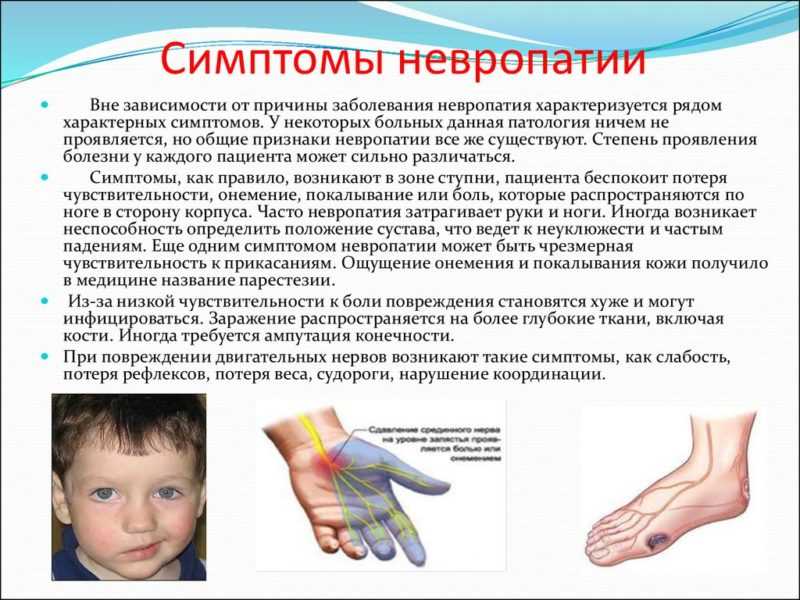
Будущие клинические направления для исследований обещают полезность физических упражнений при сенсорной нейропатии, вторичной по отношению к сахарному диабету. Некоторые из самых последних исследований показывают повышенную плотность нервных волокон у пациентов с сахарным диабетом, а также измеренную реакцию боли на физические упражнения у пациентов с установленной невропатией. Результаты, подобные этим, обнадеживают и в значительной степени оправданы, поскольку общая этиология сенсорной невропатии считается редкой по сравнению со случаями, вызванными сахарным диабетом, который гораздо более распространен.
Дифференциальный диагноз
У значительной части пациентов точная причина сенсорной невропатии не очевидна, и заболевание считается идиопатическим.[24] Литература предполагает, что идиопатическая сенсорная невропатия является диагнозом исключения и что за болезнью может стоять аутоиммунный компонент патофизиологии.[25]
Другие заболевания, которые могут проявляться аналогичным клиническим образом, включают дистальную приобретенную демиелинизирующую симметричную невропатию, а также сенсорную хроническую воспалительную демиелинизирующую полирадикулоневропатию. Эти симптомы могут также имитировать симптомы других радикулопатий, миелопатий и различных аутоиммунных заболеваний.
Эти симптомы могут также имитировать симптомы других радикулопатий, миелопатий и различных аутоиммунных заболеваний.
Прогноз
Исходы для пациентов, страдающих различными формами сенсорной невропатии, будут различаться. Когда возникает валлеровская дегенерация, ряд событий приводит к полной структурной и химической дезинтеграции нерва и приводит к более осторожному прогнозу. Восстановление зависит от регенерации нерва и в значительной степени зависит от того, насколько хорошо выровнены перерезанные нервные окончания, а также от тяжести любого повреждения прилегающих мягких тканей и рубцевания. Для достижения заметного клинического результата пораженные мышцы и/или органы должны реиннервироваться после адекватной регенерации нервов и ремиелинизации. Если патология, вызывающая какие-либо сенсорные нейропатические симптомы, связана исключительно с сегментарной демиелинизацией, прогноз будет гораздо более положительным, поскольку это влечет за собой более короткое восстановление с более быстрым возвращением к функции. Боль и температура обычно являются первыми ощущениями, которые восстанавливаются.
Боль и температура обычно являются первыми ощущениями, которые восстанавливаются.
Что касается пациентов с нарушением регуляции уровня глюкозы, жизненно важно контролировать их лабораторное значение гемоглобина A1c, чтобы отслеживать прогрессирование заболевания. Текущие рекомендации Американской диабетической ассоциации подчеркивают важность поддержания значения ниже 7,0% в сочетании со здоровым образом жизни (диета и физические упражнения) для людей с уже установленным диабетом.[26]
Осложнения
Если сенсорную невропатию не лечить в неотложные сроки, результаты могут быть изнурительными. Пациенты часто страдают от ожогов различной степени и других травматических повреждений кожи из-за отсутствия защитной чувствительности. Эта потеря чувствительности, в свою очередь, увеличивает риск инфекции, вторичной по отношению к этим травмирующим событиям, поскольку эти травмы обычно не лечатся быстро и эффективно. У пожилых людей риск случайных падений также увеличивается по мере снижения баланса и силы.
Опять же, у пациентов с сахарным диабетом, у которых имеется сопутствующая сенсорная нейропатия, осложнения являются значительными и могут изменить жизнь. Когда защитный порог утрачен, пациент нередко наступает на острый предмет, такой как стекло или ржавый гвоздь, и остается в неведении, пока не заметит кровотечение из носков. Эти травмы чрезвычайно распространены в отделении неотложной помощи и представляют собой серьезную проблему для медицинской бригады.
Тяжелые инфекции, приводящие к сепсису и гангрене нижних конечностей из-за хронических нейропатических изъязвлений или задержки инородного тела, являются одной из основных причин ампутации у людей с диабетом. Общий риск развития диабетической язвы стопы составляет около 2% в год; эта статистика увеличивается примерно до 7% у пациентов с сенсорной невропатией, что является ошеломляющим причинным открытием. Чтобы снизить эти риски, необходимо надлежащее обучение пациентов в сочетании с коммуникативной междисциплинарной медицинской командой.
Предупреждение и обучение пациентов
Для эффективного сдерживания течения этого заболевания врачи должны надлежащим образом информировать пациентов о потенциальных признаках и симптомах, которые обсуждались ранее. Не менее важно внести необходимые изменения в повседневную жизнь, если пациент начинает замечать симптомы. Пациенты с установленной сенсорной невропатией должны ограничить воздействие экстремальных температур и следить за внезапными очевидными изменениями в характере походки, чтобы уменьшить влияние повторяющихся микродвижений на ноги; также могут потребоваться модификации обувного снаряжения.
Для пациентов с диабетом необходимо ежедневно выполнять установленный протокол ежедневного скрининга стопы для раннего выявления возможных поражений. Этим пациентам также следует планировать частые визиты к своему врачу-ортопеду, по крайней мере, каждые 2–3 месяца для формальной оценки и лечения в рамках целостного подхода к лечению их сенсорной невропатии. Врач первичной медико-санитарной помощи или эндокринолог также играет жизненно важную роль в общем лечении диабета и ограничении симптоматики сенсорной невропатии.
Улучшение результатов работы команды здравоохранения
Доступность медицинской помощи в целом не является по-настоящему повсеместной во всех частях мира, и необходимо предпринять шаги, чтобы предоставить лечение, основанное на фактических данных, с помощью подхода межпрофессиональной команды к тем, кто в ней нуждается. Поскольку обучение пациентов имеет важное значение для предотвращения заболеваний, связанных с сенсорной невропатией, так же важны неврологи, сосудистые хирурги, физиотерапевты и эрготерапевты, специалисты по инфекционным заболеваниям, эндокринологи и врачи-ортопеды, каждый из которых предоставляет необходимые инструменты из своего арсенала для борьбы с этим заболеванием. и его симптомы.
Контрольные вопросы
-
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
-
Комментарий к этой статье.
Ссылки
- 1.
-
Hoeijmakers JG, Faber CG, Lauria G, Merkies IS, Waxman SG.
 Нейропатии мелких волокон — достижения в диагностике, патофизиологии и лечении. Нат Рев Нейрол. 2012 29 мая; 8 (7): 369-79. [PubMed: 22641108]
Нейропатии мелких волокон — достижения в диагностике, патофизиологии и лечении. Нат Рев Нейрол. 2012 29 мая; 8 (7): 369-79. [PubMed: 22641108] - 2.
-
Сяо П., Каку М. Клиницистский подход к периферической невропатии. Семин Нейрол. 201939 октября (5): 519-530. [PubMed: 31639835]
- 3.
-
Boulton AJM, Armstrong DG, Kirsner RS, Attinger CE, Lavery LA, Lipsky BA, Mills JL, Steinberg JS. Диагностика и лечение осложнений диабетической стопы. Американская диабетическая ассоциация; Арлингтон (Вирджиния): октябрь 2018 г. [PubMed: 30958663]
- 4.
-
Гинзберг Л. Васкулит и периферическая нервная система. Ревматология (Оксфорд). 2020 01 мая: 59 (Приложение 3): iii55-iii59. [PubMed: 32348511]
- 5.
-
Ханевинкель Р., ван Ойен М., Икрам М.А., ван Доорн П.А. Эпидемиология и факторы риска хронической полинейропатии. Евр J Эпидемиол. 2016 янв;31(1):5-20. [Статья PMC бесплатно: PMC4756033] [PubMed: 26700499]
- 6.
-
Гордон Смит А., Робинсон Синглтон Дж. Идиопатическая невропатия, предиабет и метаболический синдром. J Neurol Sci. 2006 15 марта; 242 (1-2): 9-14. [PubMed: 16448668]
- 7.
-
Boulton AJM, Armstrong DG, Hardman MJ, Malone M, Embil JM, Attinger CE, Lipsky BA, Aragón-Sánchez J, Li HK, Schultz G, Kirsner RS. Диагностика и лечение инфекций диабетической стопы. Американская диабетическая ассоциация; Арлингтон (Вирджиния): январь 2020 г. [PubMed: 32105420]
- 8.
-
Armstrong DG, Boulton AJM, Bus SA. Диабетические язвы стопы и их рецидивы. N Engl J Med. 2017 15 июня; 376 (24): 2367-2375. [PubMed: 28614678]
- 9.
-
Сгирланзони А., Парейсон Д., Лаурия Г. Заболевания сенсорных нейронов. Ланцет Нейрол. 2005 г., июнь; 4(6):349-61. [PubMed: 15907739]
- 10.
-
Шейх С.И., Амато А.А. Ганглий задних корешков под атакой: приобретенные сенсорные ганглионопатии. Практика Нейрол. 2010 дек;10(6):326-34.
 [ПубМед: 21097829]
[ПубМед: 21097829] - 11.
-
Далакаш МЦ. Хроническая идиопатическая атаксическая невропатия. Энн Нейрол. 1986 июнь; 19 (6): 545-54. [PubMed: 3014995]
- 12.
-
Camdessanché JP, Antoine JC, Honnorat J, Vial C, Petiot P, Convers P, Michel D. Паранеопластическая периферическая невропатия, связанная с антителами против Hu. Проведено клинико-электрофизиологическое исследование 20 больных. Мозг. 2002 г., январь; 125 (часть 1): 166–75. [PubMed: 11834602]
- 13.
-
Лефошёр Дж. П., Вахаб А., Планте-Борденев В., Сен Д., Менар-Лефошёр И., Руи Д., Теббал Д., Салхи Х., Креанж А., Зуари Х., Нг Винг Тин S. Диагностика невропатии мелких волокон: сравнительное исследование пяти нейрофизиологических тестов. Нейрофизиол клин. 2015 дек;45(6):445-55. [В паблике: 26596193]
- 14.
-
Thaisetthawatkul P, Fernandes Filho JA, Herrmann DN. Вклад QSART в диагностику невропатии мелких волокон. Мышечный нерв. 2013 декабрь; 48 (6): 883-8.
 [PubMed: 23649502]
[PubMed: 23649502] - 15.
-
England JD, Gronseth GS, Franklin G, Carter GT, Kinsella LJ, Cohen JA, Asbury AK, Szigeti K, Lupski JR, Latov N, Lewis RA, Low PA, Fisher MA, Herrmann DN, Howard JF, Lauria G, Miller RG, Polydefkis M, Sumner AJ., Американская академия неврологии. Американская ассоциация нейромышечной и электродиагностической медицины. Американская академия физической медицины и реабилитации. Практический параметр: оценка дистальной симметричной полинейропатии: роль лабораторного и генетического тестирования (доказательный обзор). Отчет Американской академии неврологии, Американской ассоциации нейромышечной и электродиагностической медицины и Американской академии физической медицины и реабилитации. ПМ Р. 2009 г.Январь; 1(1):5-13. [PubMed: 19627867]
- 16.
-
Hays AP. Полезность биопсии кожи для оценки периферической невропатии. Curr Neurol Neurosci Rep. 2010 Mar; 10(2):101-7. [PubMed: 20425234]
- 17.
-
Bao YF, Tang WJ, Zhu DQ, Li YX, Zee CS, Chen XJ, Geng DY.
 Сенсорная нейропатия затрагивает спинной мозг и плечевое сплетение: количественное исследование с использованием комбинации изображений с множественными эхо-сигналами (MEDIC) и величины восстановления с турбоинверсией (TIRM). Нейрорадиология. 2013 Январь; 55 (1): 41-8. [В паблике: 22922867]
Сенсорная нейропатия затрагивает спинной мозг и плечевое сплетение: количественное исследование с использованием комбинации изображений с множественными эхо-сигналами (MEDIC) и величины восстановления с турбоинверсией (TIRM). Нейрорадиология. 2013 Январь; 55 (1): 41-8. [В паблике: 22922867] - 18.
-
Тави Дж.О., Карва К., Ахмед З., Томпсон Н., Парамбил Дж., Калвер Д.А. Ассоциированная с саркоидозом невропатия мелких волокон в большой когорте: клинические аспекты и ответ на лечение ВВИГ и анти-ФНО-альфа. Респир Мед. 2017 Май; 126:135-138. [PubMed: 28318820]
- 19.
-
Antoine JC, Robert-Varvat F, Maisonobe T, Créange A, Franques J, Mathis S, Delmont E, Kuntzer T, Lefaucheur JP, Pouget J, Viala K, Desnuelle C , Echaniz-Laguna A, Rotolo F, Camdessanché JP., Французская нервно-мышечная сеть FILNEMUS. Определение терапевтического окна при острых и подострых воспалительных сенсорных нейропатиях. J Neurol Sci. 2016 15 февраля; 361: 187-91. [PubMed: 26810539]
- 20.

-
Лахан С.Е., Веласко Д.Н., Теппер Д. Ботулинический токсин-А при болезненной диабетической нейропатии: метаанализ. Боль Мед. 2015 сен; 16 (9): 1773-80. [PubMed: 25800040]
- 21.
-
Waldfogel JM, Nesbit SA, Dy SM, Sharma R, Zhang A, Wilson LM, Bennett WL, Yeh HC, Chelladurai Y, Feldman D, Robinson KA. Фармакотерапия боли при диабетической периферической невропатии и качество жизни: систематический обзор. Неврология. 2017 16 мая;88(20):1958-1967. [PubMed: 28341643]
- 22.
-
Синглтон Дж. Р., Маркус Р. Л., Джексон Дж. Э., К. Лессард М., Грэм Т. Э., Смит А. Г. Упражнения увеличивают плотность кожных нервов у пациентов с диабетом без невропатии. Энн Клин Перевод Neurol. 2014 Октябрь; 1 (10): 844-9. [Бесплатная статья PMC: PMC4241811] [PubMed: 25493275]
- 23.
-
Kluding PM, Pasnoor M, Singh R, Jernigan S, Farmer K, Rucker J, Sharma NK, Wright DE. Влияние физических упражнений на нейропатические симптомы, нервную функцию и кожную иннервацию у людей с диабетической периферической невропатией.
 J Осложнения диабета. 2012 сен-октябрь;26(5):424-9. [Бесплатная статья PMC: PMC3436981] [PubMed: 22717465]
J Осложнения диабета. 2012 сен-октябрь;26(5):424-9. [Бесплатная статья PMC: PMC3436981] [PubMed: 22717465] - 24.
-
Gwathmey KG, Pearson KT. Диагностика и лечение сенсорной полинейропатии. БМЖ. 2019 Май 08;365:l1108. [PubMed: 31068323]
- 25.
-
Dalakas MC. Патогенез иммуноопосредованных невропатий. Биохим Биофиз Акта. 2015 апрель; 1852 (4): 658-66. [PubMed: 24949885]
- 26.
-
Шервани С.И., Хан Х.А., Эхзайми А., Масуд А., Сахаркар М.К. Значение теста HbA1c в диагностике и прогнозе больных сахарным диабетом. Инсайты Биомарк. 2016;11:95-104. [Бесплатная статья PMC: PMC4933534] [PubMed: 27398023]
Сенсорная невропатия — StatPearls — NCBI Bookshelf
Continuing Education Activity
Сенсорная невропатия — распространенное заболевание, которое часто является прямым осложнением другого сопутствующего заболевания. При определенных обстоятельствах это может быть изнурительным, и требуется более широкое распространение информации во всех областях здравоохранения. В этом мероприятии рассматривается оценка и лечение сенсорной невропатии и подчеркивается роль межпрофессиональной команды в лечении и улучшении ухода за пациентами с этим заболеванием.
В этом мероприятии рассматривается оценка и лечение сенсорной невропатии и подчеркивается роль межпрофессиональной команды в лечении и улучшении ухода за пациентами с этим заболеванием.
Цели:
-
Обобщите этиологию сенсорной невропатии.
-
Объясните общие результаты медицинского осмотра, связанные с сенсорной невропатией.
-
Опишите возможные варианты лечения сенсорной невропатии.
-
Обсудите важность межпрофессиональных командных стратегий для улучшения координации помощи и коммуникации для развития сенсорной невропатии и улучшения исходов.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Сенсорные невропатии относятся к множеству заболеваний, которые приводят к потере чувствительности во всем теле. В совокупности сенсорные невропатии могут быть результатом множества состояний, которые будут обсуждаться в этом обзоре. В дальнейшем они могут подразделяться на патологии мелких волокон (с преобладанием боли) и крупных волокон (с преобладанием атаксии).
В дальнейшем они могут подразделяться на патологии мелких волокон (с преобладанием боли) и крупных волокон (с преобладанием атаксии).
При классификации сенсорной невропатии для соответствующего лечения размер нерва и степень миелинизации играют ключевую роль. При оценке невропатий мелких волокон особый интерес представляют мелкие соматические волокна (Аδ и мелкие немиелинизированные С-волокна). Эти волокна передают вредные и тепловые сигналы и регулируют преганглионарную симпатическую и парасимпатическую функции (волокна Aδ), а также постганглионарную вегетативную функцию (волокна C) [1]. Нарушение нормального физиологического состояния этих волокон обычно приводит к жгучей и стреляющей боли с парестезиями.
Напротив, невропатии крупных волокон возникают в результате ослабления волокон Aβ, которые регулируют проприоцептивные сигналы вибрации и прикосновения. Грубо говоря, пациенты с сенсорной атаксией, вероятно, имеют деформацию задних столбов спинного мозга, а также ганглиев задних корешков. [2] Хотя атаксия патогномонична для сенсорной невропатии крупных волокон, может иметь место последующее поражение более мелких волокон. Таким образом, некоторые заболевания могут приводить к полинейропатиям смешанной этиологии, которые состоят как из мелких, так и из крупных волокон (например, сахарный диабет) и представляют собой одну из самых значительных проблем для общественного здравоохранения в современной медицине.
[2] Хотя атаксия патогномонична для сенсорной невропатии крупных волокон, может иметь место последующее поражение более мелких волокон. Таким образом, некоторые заболевания могут приводить к полинейропатиям смешанной этиологии, которые состоят как из мелких, так и из крупных волокон (например, сахарный диабет) и представляют собой одну из самых значительных проблем для общественного здравоохранения в современной медицине.
Этиология
Распознавание различных причинных факторов, непосредственно связанных с сенсорной невропатией, имеет первостепенное значение для обеспечения быстрого и эффективного лечения в качестве клинициста. Чтобы получить более полное представление о возможных основных этиологиях, необходимо рассмотреть следующие процессы, которые включают, но не ограничиваются:
-
Иммуноопосредованные
-
Саркоидоз, синдром Шегрена, системная красная волчанка, целиакия
-
-
Метаболический
-
Сахарный диабет, гиперлипидемия
-
-
Дефицит питательных веществ
-
Витамин B12, медь, витамин E, фолиевая кислота
-
-
Токсичные
-
Химиотерапия, медикаментозная, алкогольная
-
-
Наследственная
-
Гемохроматоз, болезнь Фабри, синдром Элерса-Данлоса, атаксия Фридрейха
-
-
Инфекционный
-
Сифилис, проказа, ВИЧ, гепатит С, криоглобулинемия
-
-
Прочие
-
Идиопатический, фибромиалгия, васкулит [4]
-
значительная часть случаев (от 20 до 30%).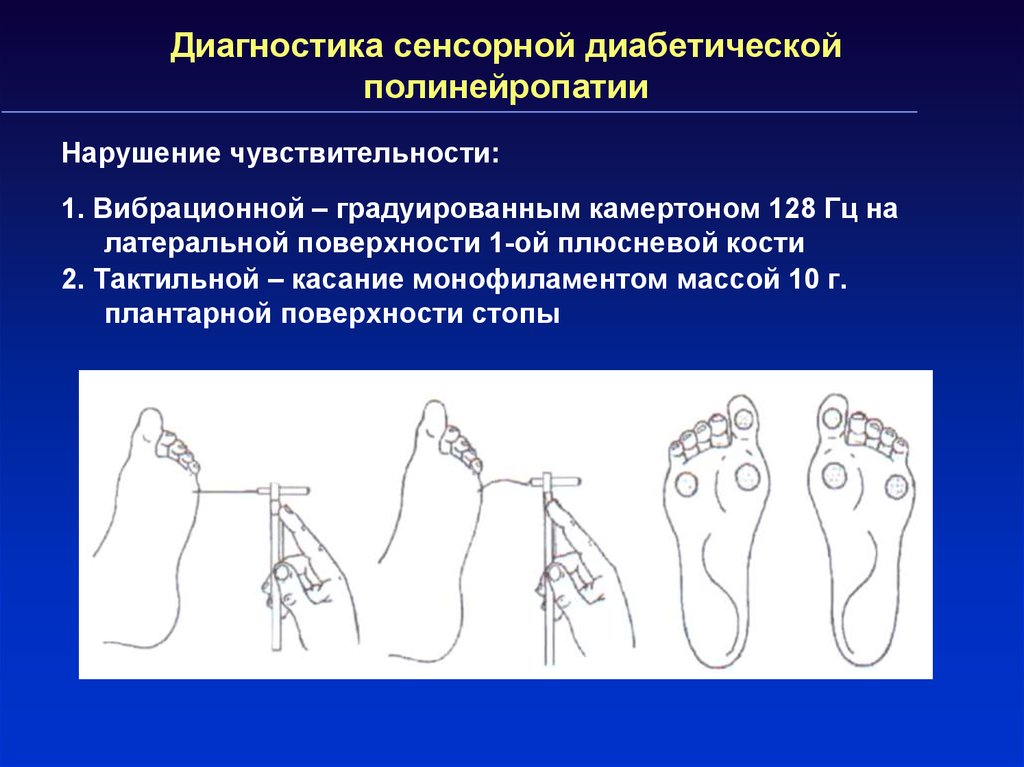 [5]
[5]
Эпидемиология
Исследования, в которых оценивалась заболеваемость сенсорной невропатией среди населения в целом, сообщают о распространенности от 1 до 3% с увеличением до 7% у пожилых людей.[5] Также было показано, что в развивающихся странах наблюдается более низкая распространенность, что может быть частично связано с различиями в ожидаемой продолжительности жизни. С глобальной точки зрения чаще всего страдают западные страны, с небольшой предрасположенностью к женщинам.
С точки зрения общественного здравоохранения важно отметить, что сахарный диабет является ведущей причиной периферической невропатии во всем мире.[6] До 50% пожилых пациентов с сахарным диабетом приобретают ту или иную форму дистальной периферической невропатии, которая влияет на их чувство боли и различение температуры [7]. Хирург-ортопед-новатор, доктор Пол Бранд, был известен своей работой по невропатии, вдохновленной работой в Индии, где он заметил, что потеря периферической чувствительности («дар боли») была причиной того, что его пациенты с болезнью Хансена страдали.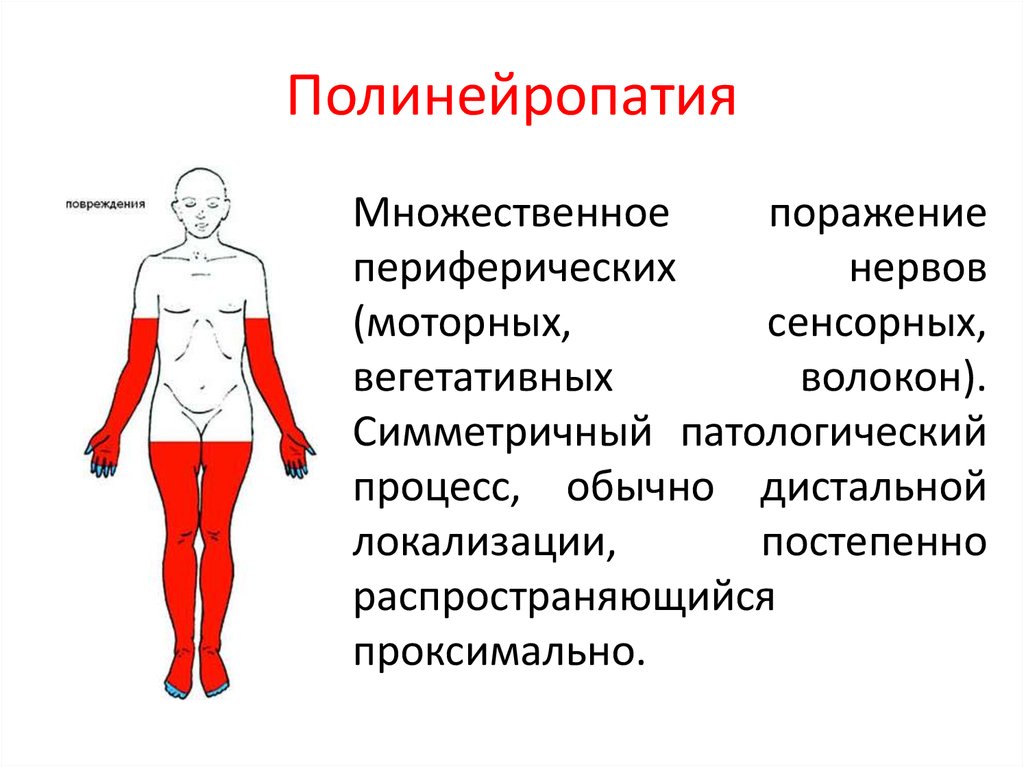 от сильных рубцов и изъязвлений. Точно так же у диабетиков дистальная периферическая невропатия является одним из основных факторов риска на «пути» к развитию осложнений диабетической стопы.[8]
от сильных рубцов и изъязвлений. Точно так же у диабетиков дистальная периферическая невропатия является одним из основных факторов риска на «пути» к развитию осложнений диабетической стопы.[8]
Анамнез и физикальное исследование
Одним из наиболее отчетливых симптомов сенсорной невропатии является ранняя атаксия. Это проявление в основном связано с нарушением работы афферентных нейронов, передающих импульсы от конечностей тела.[9] Если эти симптомы прогрессируют, результирующие «корчащиеся» движения будут проявляться в руках и ногах, когда пациент закрывает глаза.[10] Положительные сенсорные симптомы также распространены при поражении волокон малого и среднего размера. Классические клинические признаки включают жалобы на «покалывание» и «электричество» в пораженных конечностях, которые напоминают чулки и перчатки. Особенно у людей с диабетом клиницист должен проявлять бдительность при оценке негативных невропатических симптомов, которые проявляются в невропатиях мелких волокон.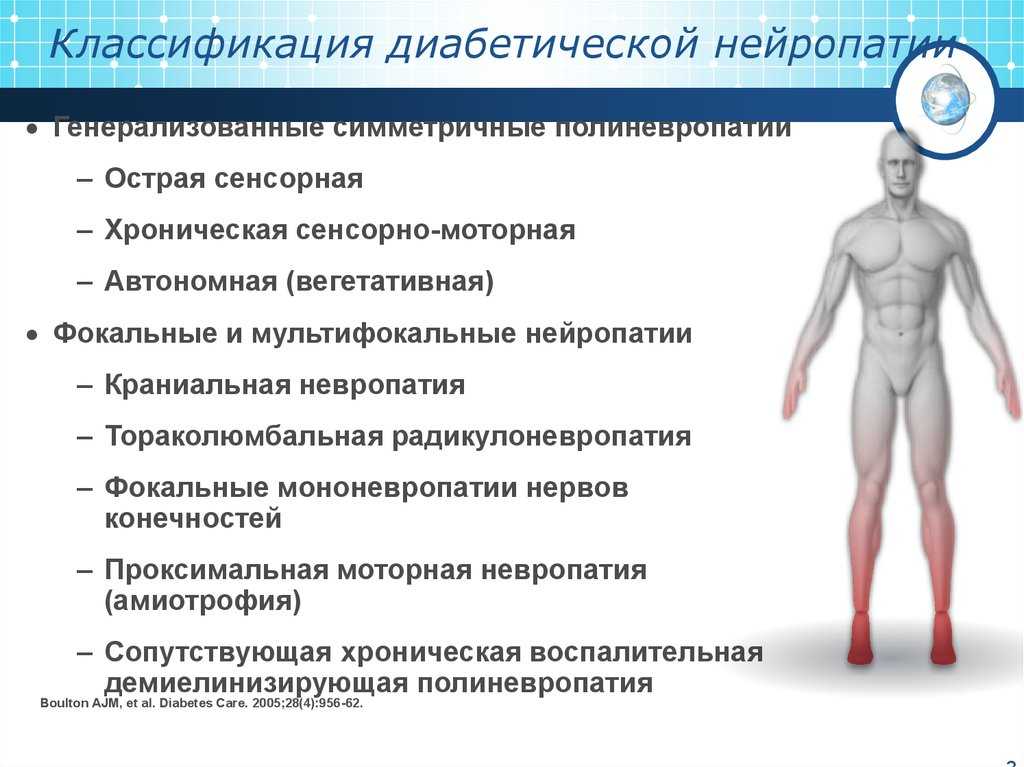 Онемение, как негативный нейропатический симптом, обычно наблюдается в стопах, не зависит от длины и многоочаговое.
Онемение, как негативный нейропатический симптом, обычно наблюдается в стопах, не зависит от длины и многоочаговое.
При проведении субъективного опроса пациента вариабельность течения заболевания будет значительной. Подострые сенсорные невропатии обычно наблюдаются в иммунно-опосредованных и постинфекционных случаях, тогда как идиопатические варианты оказались более застойными [11]. Во многих случаях двигательная слабость не сопровождает сенсорную невропатию. Однако двигательная активность может быть нарушена у пациентов с паранеопластическими сенсорными нейропатиями, приводящими к отсутствию рефлексов растяжения.
Оценка
Критерии оценки сенсорной невропатии в основном связаны с нейрофизиологическим обследованием и дерматопатологическими исследованиями, такими как биопсия кожи. При диагностике невропатии мелких волокон результаты электромиографии (ЭМГ) могут казаться нормальными, а наличие икроножных и подошвенных реакций не исключает чисто невропатию мелких волокон. В исследованиях ЭМГ сенсорные невропатии демонстрируют сниженный или отсутствующий потенциал действия сенсорного нерва [12]. Пациентам с диабетической периферической сенсорной невропатией часто проводят тест Semmes-Weinstein 5.07 с нейлоновой мононитью в различных местах стопы для проверки защитного порога (формально определяемого как 10 грамм силы).
В исследованиях ЭМГ сенсорные невропатии демонстрируют сниженный или отсутствующий потенциал действия сенсорного нерва [12]. Пациентам с диабетической периферической сенсорной невропатией часто проводят тест Semmes-Weinstein 5.07 с нейлоновой мононитью в различных местах стопы для проверки защитного порога (формально определяемого как 10 грамм силы).
Что касается вегетативных сенсорных тестов, существуют количественные исследования, которые оценивают ощущение тепла и холода, преходящие изменения электрического потенциала кожи (например, активность потовых желез) и неинвазивные исследования электрохимической проводимости кожи для выявления судомоторной дисфункции.[13] ] Для нейропатии с преобладанием мелких волокон одними из наиболее полезных исследований являются терморегуляторные тесты пота и количественный тест судомоторного рефлекса аксонов. Хотя эти исследования недоступны, недавняя литература показывает, что их клинические дополнения обеспечивают более высокий диагностический успех. [14]
[14]
В настоящее время утвержденным золотым стандартом диагностики невропатии мелких волокон является биопсия кожи.[15] В зависимости от исследования чувствительность биопсии кожи может достигать 90 %, а специфичность — до 97 %.[15][16] Преимущества биопсии кожи включают простоту использования и низкую заболеваемость. Общие места приобретения включают дистальную часть ноги, всего 10 см. проксимальнее латеральной лодыжки и латерально дистальнее или проксимальнее бедра.[1] Как правило, биопсия нерва не требуется для диагностики сенсорной невропатии.
Визуализирующие исследования также играют роль в диагностике сенсорных невропатий и наиболее полезны при оценке паранеопластической этиологии. Магнитно-резонансная томография и ее аналоги, инверсионно-восстановительная МРТ-последовательность импульсов и Т2-взвешенная испорченная градиент-эхо-последовательность имеют особое значение для визуализации патологии дорсального столба [17].
Лечение/управление
Руководящих принципов, касающихся конкретных методов лечения сенсорных невропатий, как правило, не существует. Большая часть данных о лечении основана на мнениях экспертов, а также на хорошо спланированных исследованиях. Некоторые методы лечения включают инъекции внутривенных иммуноглобулинов, метотрексата, кортикостероидов, инфликсимаба и плазмаферез, среди прочего, в зависимости от этиологии.[18] Последние данные свидетельствуют о том, что сенсорная симптоматика обычно выходит на плато через 7–10 месяцев.[19]] Если возможно, протоколы лечения следует начинать в течение этого периода.
Большая часть данных о лечении основана на мнениях экспертов, а также на хорошо спланированных исследованиях. Некоторые методы лечения включают инъекции внутривенных иммуноглобулинов, метотрексата, кортикостероидов, инфликсимаба и плазмаферез, среди прочего, в зависимости от этиологии.[18] Последние данные свидетельствуют о том, что сенсорная симптоматика обычно выходит на плато через 7–10 месяцев.[19]] Если возможно, протоколы лечения следует начинать в течение этого периода.
Эффективность различных пероральных препаратов, таких как противосудорожные средства (прегабалин и окскарбазепин), ингибиторы обратного захвата серотонина и норадреналина (дулоксетин и венлафаксин), трициклические антидепрессанты, опиоиды (трамадол и тапентадол) и ботулинический токсин А (с хемоденервацией и без нее) была продемонстрирована более эффективен, чем плацебо в многочисленных рандомизированных контролируемых исследованиях.[20][21] Местные агенты, такие как лидокаин и капсаицин, были рекомендованы с уровнем доказательности B в соответствии со стандартами Американской академии неврологии.
Будущие клинические направления для исследований обещают полезность физических упражнений при сенсорной нейропатии, вторичной по отношению к сахарному диабету. Некоторые из самых последних исследований показывают повышенную плотность нервных волокон у пациентов с сахарным диабетом, а также измеренную реакцию боли на физические упражнения у пациентов с установленной невропатией. Результаты, подобные этим, обнадеживают и в значительной степени оправданы, поскольку общая этиология сенсорной невропатии считается редкой по сравнению со случаями, вызванными сахарным диабетом, который гораздо более распространен.
Дифференциальный диагноз
У значительной части пациентов точная причина сенсорной невропатии не очевидна, и заболевание считается идиопатическим.[24] Литература предполагает, что идиопатическая сенсорная невропатия является диагнозом исключения и что за болезнью может стоять аутоиммунный компонент патофизиологии.[25]
Другие заболевания, которые могут проявляться аналогичным клиническим образом, включают дистальную приобретенную демиелинизирующую симметричную невропатию, а также сенсорную хроническую воспалительную демиелинизирующую полирадикулоневропатию.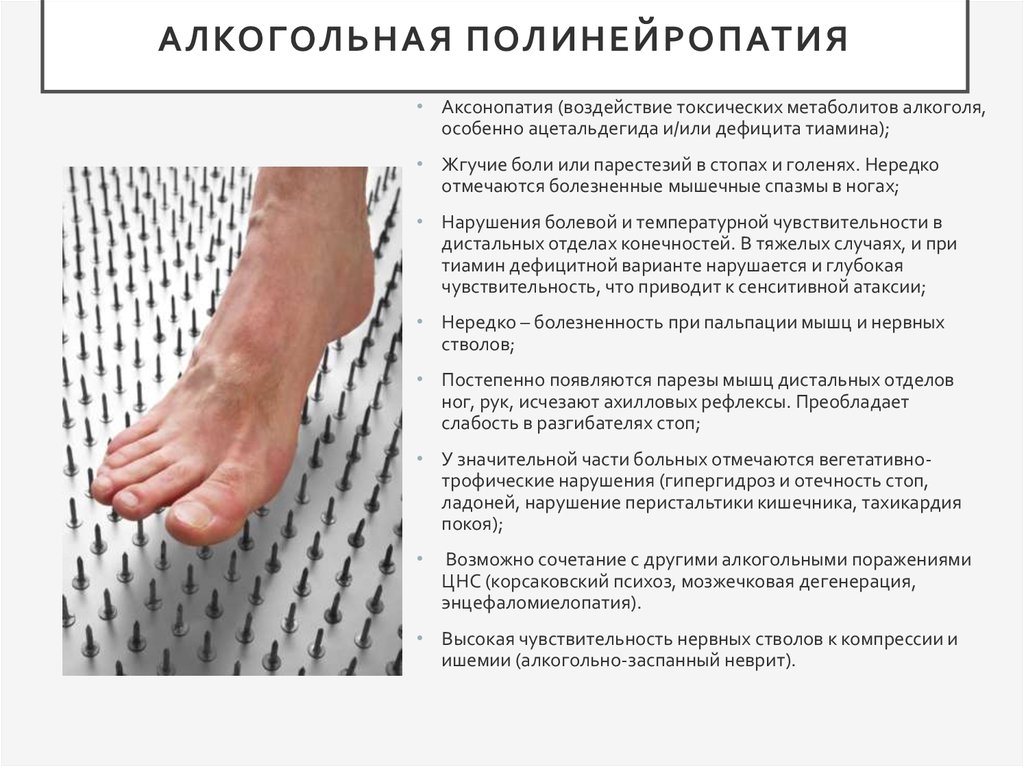 Эти симптомы могут также имитировать симптомы других радикулопатий, миелопатий и различных аутоиммунных заболеваний.
Эти симптомы могут также имитировать симптомы других радикулопатий, миелопатий и различных аутоиммунных заболеваний.
Прогноз
Исходы для пациентов, страдающих различными формами сенсорной невропатии, будут различаться. Когда возникает валлеровская дегенерация, ряд событий приводит к полной структурной и химической дезинтеграции нерва и приводит к более осторожному прогнозу. Восстановление зависит от регенерации нерва и в значительной степени зависит от того, насколько хорошо выровнены перерезанные нервные окончания, а также от тяжести любого повреждения прилегающих мягких тканей и рубцевания. Для достижения заметного клинического результата пораженные мышцы и/или органы должны реиннервироваться после адекватной регенерации нервов и ремиелинизации. Если патология, вызывающая какие-либо сенсорные нейропатические симптомы, связана исключительно с сегментарной демиелинизацией, прогноз будет гораздо более положительным, поскольку это влечет за собой более короткое восстановление с более быстрым возвращением к функции. Боль и температура обычно являются первыми ощущениями, которые восстанавливаются.
Боль и температура обычно являются первыми ощущениями, которые восстанавливаются.
Что касается пациентов с нарушением регуляции уровня глюкозы, жизненно важно контролировать их лабораторное значение гемоглобина A1c, чтобы отслеживать прогрессирование заболевания. Текущие рекомендации Американской диабетической ассоциации подчеркивают важность поддержания значения ниже 7,0% в сочетании со здоровым образом жизни (диета и физические упражнения) для людей с уже установленным диабетом.[26]
Осложнения
Если сенсорную невропатию не лечить в неотложные сроки, результаты могут быть изнурительными. Пациенты часто страдают от ожогов различной степени и других травматических повреждений кожи из-за отсутствия защитной чувствительности. Эта потеря чувствительности, в свою очередь, увеличивает риск инфекции, вторичной по отношению к этим травмирующим событиям, поскольку эти травмы обычно не лечатся быстро и эффективно. У пожилых людей риск случайных падений также увеличивается по мере снижения баланса и силы.
Опять же, у пациентов с сахарным диабетом, у которых имеется сопутствующая сенсорная нейропатия, осложнения являются значительными и могут изменить жизнь. Когда защитный порог утрачен, пациент нередко наступает на острый предмет, такой как стекло или ржавый гвоздь, и остается в неведении, пока не заметит кровотечение из носков. Эти травмы чрезвычайно распространены в отделении неотложной помощи и представляют собой серьезную проблему для медицинской бригады.
Тяжелые инфекции, приводящие к сепсису и гангрене нижних конечностей из-за хронических нейропатических изъязвлений или задержки инородного тела, являются одной из основных причин ампутации у людей с диабетом. Общий риск развития диабетической язвы стопы составляет около 2% в год; эта статистика увеличивается примерно до 7% у пациентов с сенсорной невропатией, что является ошеломляющим причинным открытием. Чтобы снизить эти риски, необходимо надлежащее обучение пациентов в сочетании с коммуникативной междисциплинарной медицинской командой.
Предупреждение и обучение пациентов
Для эффективного сдерживания течения этого заболевания врачи должны надлежащим образом информировать пациентов о потенциальных признаках и симптомах, которые обсуждались ранее. Не менее важно внести необходимые изменения в повседневную жизнь, если пациент начинает замечать симптомы. Пациенты с установленной сенсорной невропатией должны ограничить воздействие экстремальных температур и следить за внезапными очевидными изменениями в характере походки, чтобы уменьшить влияние повторяющихся микродвижений на ноги; также могут потребоваться модификации обувного снаряжения.
Для пациентов с диабетом необходимо ежедневно выполнять установленный протокол ежедневного скрининга стопы для раннего выявления возможных поражений. Этим пациентам также следует планировать частые визиты к своему врачу-ортопеду, по крайней мере, каждые 2–3 месяца для формальной оценки и лечения в рамках целостного подхода к лечению их сенсорной невропатии. Врач первичной медико-санитарной помощи или эндокринолог также играет жизненно важную роль в общем лечении диабета и ограничении симптоматики сенсорной невропатии.
Улучшение результатов работы команды здравоохранения
Доступность медицинской помощи в целом не является по-настоящему повсеместной во всех частях мира, и необходимо предпринять шаги, чтобы предоставить лечение, основанное на фактических данных, с помощью подхода межпрофессиональной команды к тем, кто в ней нуждается. Поскольку обучение пациентов имеет важное значение для предотвращения заболеваний, связанных с сенсорной невропатией, так же важны неврологи, сосудистые хирурги, физиотерапевты и эрготерапевты, специалисты по инфекционным заболеваниям, эндокринологи и врачи-ортопеды, каждый из которых предоставляет необходимые инструменты из своего арсенала для борьбы с этим заболеванием. и его симптомы.
Контрольные вопросы
-
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
-
Комментарий к этой статье.
Ссылки
- 1.
-
Hoeijmakers JG, Faber CG, Lauria G, Merkies IS, Waxman SG.
 Нейропатии мелких волокон — достижения в диагностике, патофизиологии и лечении. Нат Рев Нейрол. 2012 29 мая; 8 (7): 369-79. [PubMed: 22641108]
Нейропатии мелких волокон — достижения в диагностике, патофизиологии и лечении. Нат Рев Нейрол. 2012 29 мая; 8 (7): 369-79. [PubMed: 22641108] - 2.
-
Сяо П., Каку М. Клиницистский подход к периферической невропатии. Семин Нейрол. 201939 октября (5): 519-530. [PubMed: 31639835]
- 3.
-
Boulton AJM, Armstrong DG, Kirsner RS, Attinger CE, Lavery LA, Lipsky BA, Mills JL, Steinberg JS. Диагностика и лечение осложнений диабетической стопы. Американская диабетическая ассоциация; Арлингтон (Вирджиния): октябрь 2018 г. [PubMed: 30958663]
- 4.
-
Гинзберг Л. Васкулит и периферическая нервная система. Ревматология (Оксфорд). 2020 01 мая: 59 (Приложение 3): iii55-iii59. [PubMed: 32348511]
- 5.
-
Ханевинкель Р., ван Ойен М., Икрам М.А., ван Доорн П.А. Эпидемиология и факторы риска хронической полинейропатии. Евр J Эпидемиол. 2016 янв;31(1):5-20. [Статья PMC бесплатно: PMC4756033] [PubMed: 26700499]
- 6.

-
Гордон Смит А., Робинсон Синглтон Дж. Идиопатическая невропатия, предиабет и метаболический синдром. J Neurol Sci. 2006 15 марта; 242 (1-2): 9-14. [PubMed: 16448668]
- 7.
-
Boulton AJM, Armstrong DG, Hardman MJ, Malone M, Embil JM, Attinger CE, Lipsky BA, Aragón-Sánchez J, Li HK, Schultz G, Kirsner RS. Диагностика и лечение инфекций диабетической стопы. Американская диабетическая ассоциация; Арлингтон (Вирджиния): январь 2020 г. [PubMed: 32105420]
- 8.
-
Armstrong DG, Boulton AJM, Bus SA. Диабетические язвы стопы и их рецидивы. N Engl J Med. 2017 15 июня; 376 (24): 2367-2375. [PubMed: 28614678]
- 9.
-
Сгирланзони А., Парейсон Д., Лаурия Г. Заболевания сенсорных нейронов. Ланцет Нейрол. 2005 г., июнь; 4(6):349-61. [PubMed: 15907739]
- 10.
-
Шейх С.И., Амато А.А. Ганглий задних корешков под атакой: приобретенные сенсорные ганглионопатии. Практика Нейрол. 2010 дек;10(6):326-34.
 [ПубМед: 21097829]
[ПубМед: 21097829] - 11.
-
Далакаш МЦ. Хроническая идиопатическая атаксическая невропатия. Энн Нейрол. 1986 июнь; 19 (6): 545-54. [PubMed: 3014995]
- 12.
-
Camdessanché JP, Antoine JC, Honnorat J, Vial C, Petiot P, Convers P, Michel D. Паранеопластическая периферическая невропатия, связанная с антителами против Hu. Проведено клинико-электрофизиологическое исследование 20 больных. Мозг. 2002 г., январь; 125 (часть 1): 166–75. [PubMed: 11834602]
- 13.
-
Лефошёр Дж. П., Вахаб А., Планте-Борденев В., Сен Д., Менар-Лефошёр И., Руи Д., Теббал Д., Салхи Х., Креанж А., Зуари Х., Нг Винг Тин S. Диагностика невропатии мелких волокон: сравнительное исследование пяти нейрофизиологических тестов. Нейрофизиол клин. 2015 дек;45(6):445-55. [В паблике: 26596193]
- 14.
-
Thaisetthawatkul P, Fernandes Filho JA, Herrmann DN. Вклад QSART в диагностику невропатии мелких волокон. Мышечный нерв. 2013 декабрь; 48 (6): 883-8.
 [PubMed: 23649502]
[PubMed: 23649502] - 15.
-
England JD, Gronseth GS, Franklin G, Carter GT, Kinsella LJ, Cohen JA, Asbury AK, Szigeti K, Lupski JR, Latov N, Lewis RA, Low PA, Fisher MA, Herrmann DN, Howard JF, Lauria G, Miller RG, Polydefkis M, Sumner AJ., Американская академия неврологии. Американская ассоциация нейромышечной и электродиагностической медицины. Американская академия физической медицины и реабилитации. Практический параметр: оценка дистальной симметричной полинейропатии: роль лабораторного и генетического тестирования (доказательный обзор). Отчет Американской академии неврологии, Американской ассоциации нейромышечной и электродиагностической медицины и Американской академии физической медицины и реабилитации. ПМ Р. 2009 г.Январь; 1(1):5-13. [PubMed: 19627867]
- 16.
-
Hays AP. Полезность биопсии кожи для оценки периферической невропатии. Curr Neurol Neurosci Rep. 2010 Mar; 10(2):101-7. [PubMed: 20425234]
- 17.
-
Bao YF, Tang WJ, Zhu DQ, Li YX, Zee CS, Chen XJ, Geng DY.
 Сенсорная нейропатия затрагивает спинной мозг и плечевое сплетение: количественное исследование с использованием комбинации изображений с множественными эхо-сигналами (MEDIC) и величины восстановления с турбоинверсией (TIRM). Нейрорадиология. 2013 Январь; 55 (1): 41-8. [В паблике: 22922867]
Сенсорная нейропатия затрагивает спинной мозг и плечевое сплетение: количественное исследование с использованием комбинации изображений с множественными эхо-сигналами (MEDIC) и величины восстановления с турбоинверсией (TIRM). Нейрорадиология. 2013 Январь; 55 (1): 41-8. [В паблике: 22922867] - 18.
-
Тави Дж.О., Карва К., Ахмед З., Томпсон Н., Парамбил Дж., Калвер Д.А. Ассоциированная с саркоидозом невропатия мелких волокон в большой когорте: клинические аспекты и ответ на лечение ВВИГ и анти-ФНО-альфа. Респир Мед. 2017 Май; 126:135-138. [PubMed: 28318820]
- 19.
-
Antoine JC, Robert-Varvat F, Maisonobe T, Créange A, Franques J, Mathis S, Delmont E, Kuntzer T, Lefaucheur JP, Pouget J, Viala K, Desnuelle C , Echaniz-Laguna A, Rotolo F, Camdessanché JP., Французская нервно-мышечная сеть FILNEMUS. Определение терапевтического окна при острых и подострых воспалительных сенсорных нейропатиях. J Neurol Sci. 2016 15 февраля; 361: 187-91. [PubMed: 26810539]
- 20.

-
Лахан С.Е., Веласко Д.Н., Теппер Д. Ботулинический токсин-А при болезненной диабетической нейропатии: метаанализ. Боль Мед. 2015 сен; 16 (9): 1773-80. [PubMed: 25800040]
- 21.
-
Waldfogel JM, Nesbit SA, Dy SM, Sharma R, Zhang A, Wilson LM, Bennett WL, Yeh HC, Chelladurai Y, Feldman D, Robinson KA. Фармакотерапия боли при диабетической периферической невропатии и качество жизни: систематический обзор. Неврология. 2017 16 мая;88(20):1958-1967. [PubMed: 28341643]
- 22.
-
Синглтон Дж. Р., Маркус Р. Л., Джексон Дж. Э., К. Лессард М., Грэм Т. Э., Смит А. Г. Упражнения увеличивают плотность кожных нервов у пациентов с диабетом без невропатии. Энн Клин Перевод Neurol. 2014 Октябрь; 1 (10): 844-9. [Бесплатная статья PMC: PMC4241811] [PubMed: 25493275]
- 23.
-
Kluding PM, Pasnoor M, Singh R, Jernigan S, Farmer K, Rucker J, Sharma NK, Wright DE. Влияние физических упражнений на нейропатические симптомы, нервную функцию и кожную иннервацию у людей с диабетической периферической невропатией.


