Синдром гипервозбудимости у детей
Синдром гипервозбудимости — это функциональное расстройство, для которого характерно появление соматовегетативных нарушений и повышенной нервной возбудимости. Первые признаки болезни проявляются у новорожденных и детей 1-2 года жизни. У малышей старше 3 лет патологию выявляют гораздо реже. Тем не менее статистика говорит о том, что повышенной возбудимостью страдает около 10% школьников.
Для борьбы с этой проблемой в клинике «ЛЕКАРЬ» применяются методики лечения и профилактики, основанные на сочетании современных медицинский практики и традиционных восточных приемов. Благодаря строго индивидуальному подбору процедур это позволяет надежно устранять проявления заболевания без побочных эффектов.
Причины появления патологии
У грудничка синдром повышенной возбудимости чаще всего развивается вследствие родовых травм или осложненного течения беременности. У школьников патология обычно является следствием несвоевременного лечения в раннем возрасте. Иногда причиной становится дефицит родительского внимания или равнодушие сверстников.
Иногда причиной становится дефицит родительского внимания или равнодушие сверстников.
Распространенные причины перинатальной возбудимости:
- Травмы, полученные во время родов. Чаще всего к ним приводят слишком быстрые и стремительные роды или большой размер плода.
- Гипоксия. Дефицит кислорода во время беременности приводит к ишемии головного мозга малыша. Причиной этого чаще всего бывает плацентарная недостаточность.
- Инфекции. Дети, чьи мамы во время беременности переболели инфекционными болезнями, страдают от патологии чаще остальных.
- Воздействие тератогенных факторов. Курение и употребление алкоголя во время вынашивания малыша также способствует развитию синдрома.
- Отягощенная наследственность. Холерический темперамент и наличие психических расстройств у родителей могут быть причиной гипервозбудимости их детей.
- Болезни детского возраста. Кишечные колики, рахит и спазмофилия могут приводить к развитию повышенной возбудимости в более старшем возрасте.

Характерные симптомы
Заметить признаки гипервозбудимости у неврожденного младенца довольно просто. Малыш становится плаксивым, раздражительным, плохо спит и отказывается от груди. Врачи нередко выявляют снижение мышечного тонуса и появление патологических ритмичных движений рук и ног. При отсутствии лечения у ребенка нарушается психомоторное, речевое и умственное развитие.
Симптомы, позволяющие заподозрить патологию:
- плаксивость;
- частый отказ от кормления;
- повышенная двигательная активность;
- бессонница;
- постоянные срыгивания и рвота;
- склонность к поносам;
- тремор, хаотичные движения рук и ног;
- вегетативные расстройства.
Методы диагностики
Диагностикой и лечением патологии занимается врач-невропатолог. Опытный специалист может поставить диагноз «гипервозбудимость» уже после осмотра и обследования ребенка. Для выявление сопутствующих расстройств в работе других органов используется биорезонансная диагностика. Методика позволяет комплексно оценить состояние нервной системы малыша и понять, что вызвало проблему.
Методика позволяет комплексно оценить состояние нервной системы малыша и понять, что вызвало проблему.
Лечение гипервозбудимости у детей
Для лечения повышенной возбудимости у ребенка в нашем центре используются физиотерапия и методики восточной медицины. Давать малышу седативные препараты, нейролептики или транквилизаторы не только нежелательно, но и опасно, и токсичные аптечные лекарства лучше заменить лечебными травами (фитотерапией).
Также в такой ситуации полезны гомеопатия, иглорефлексотерапия, остеопатия, ЛФК. Не менее эффективен и точечный массаж при гипервозбудимости. При необходимости ребенку назначаются занятия с логопедом, дефектологом, психиатром, психотерапевтом или нейропсихологом.
Цены и методы лечения в нашей клинике
Для борьбы с синдромом гипервозбудимости у детей наши специалисты используют комплексную терапию, включающую психолого-педагогическую помощь. Получить более подробную информацию вы можете, записавшись на прием с помощью наших администраторов.
Синдром гипервозбудимости у детей. Что такое Синдром гипервозбудимости у детей?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Синдром гипервозбудимости у детей – симптомокомплекс у детей раннего возраста, характеризующийся различными соматовегетативными расстройствами и повышенной нервно-рефлекторной возбудимостью. Синдром гипервозбудимости у детей проявляется двигательным беспокойством, тремором подбородка и конечностей, беспричинным плачем, нарушением сна, повышенным мышечным тонусом, частыми и обильными срыгиваниями и т. д. Для выявления органической основы синдрома гипервозбудимости детям проводится нейросонография, дуплексное сканирование сосудов головного мозга, ЭЭГ, ЭНМГ, УЗИ или рентгенография шейного отдела позвоночника.
- Причины гипервозбудимости у детей
- Симптомы гипервозбудимости
- Диагностика у детей
- Лечение синдрома гипервозбудимости у детей
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Синдром гипервозбудимости у детей (синдром повышенной нервно-рефлекторной возбудимости) – комплекс патологических проявлений, развивающихся у детей с легкой формой перинатального поражения нервной системы. У детей раннего возраста синдром гипервозбудимости диагностируется в 42-44% случаев. В отечественной и зарубежной детской неврологии сложилось различное отношение к синдрому гипервозбудимости у детей. Так, отечественные неврологи рассматривают данное состояние исключительно как патологический синдром, в то время как их зарубежные коллеги склонны считать его скорее пограничным состоянием, не всегда требующим активной коррекции.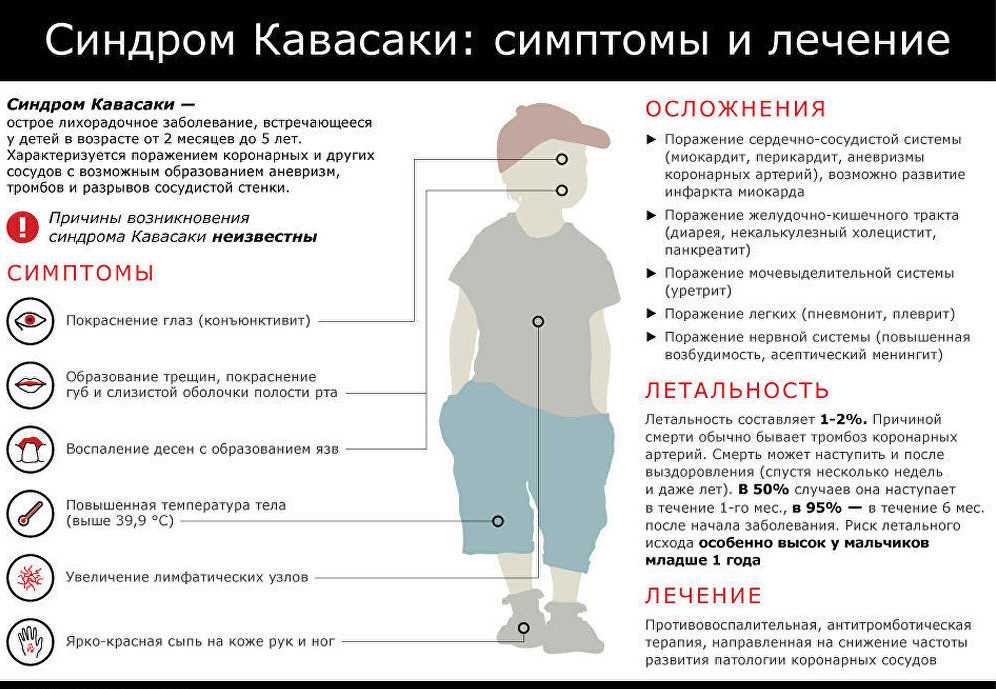
Синдром гипервозбудимости у детей
Причины гипервозбудимости у детей
Синдром гипервозбудимости может являться следствием перинатальной патологии ЦНС (гипоксической, травматической, инфекционной, токсико-метаболической) или других заболеваний детей раннего возраста.
Чаще всего причина синдрома гипервозбудимости у детей кроется в неблагополучном течении беременности и родовых травмах новорожденного, приводящих к внутриутробной гипоксии и поражению ЦНС. Этому могут способствовать токсикозы беременности, фетоплацентарная недостаточность, инфекционные заболевания будущей мамы, преждевременные роды, переношенная беременность, затяжное или стремительное родоразрешение, узкий таз роженицы и др.
Появление преходящей гипервозбудимости у детей может быть связано с нарушением реакции адаптации вследствие стресса, заболеваниями детского возраста (кишечными коликами, прорезыванием зубов, спазмофилией и рахитом, грыжами, дисбактериозом и пр.). Наконец, к гипервозбудимости склонны дети с особенностями темперамента (холерическим типом реагирования). Синдром гипервозбудимости характерен для детей с нервно-артритическим диатезом.
Симптомы гипервозбудимости
Проявления синдрома гипервозбудимости обычно развиваются в первые месяцы жизни ребенка. Основные признаки синдрома гипервозбудимости у детей включают соматовегетативные расстройства, повышенную нервно-психическую возбудимость и одновременно истощаемость.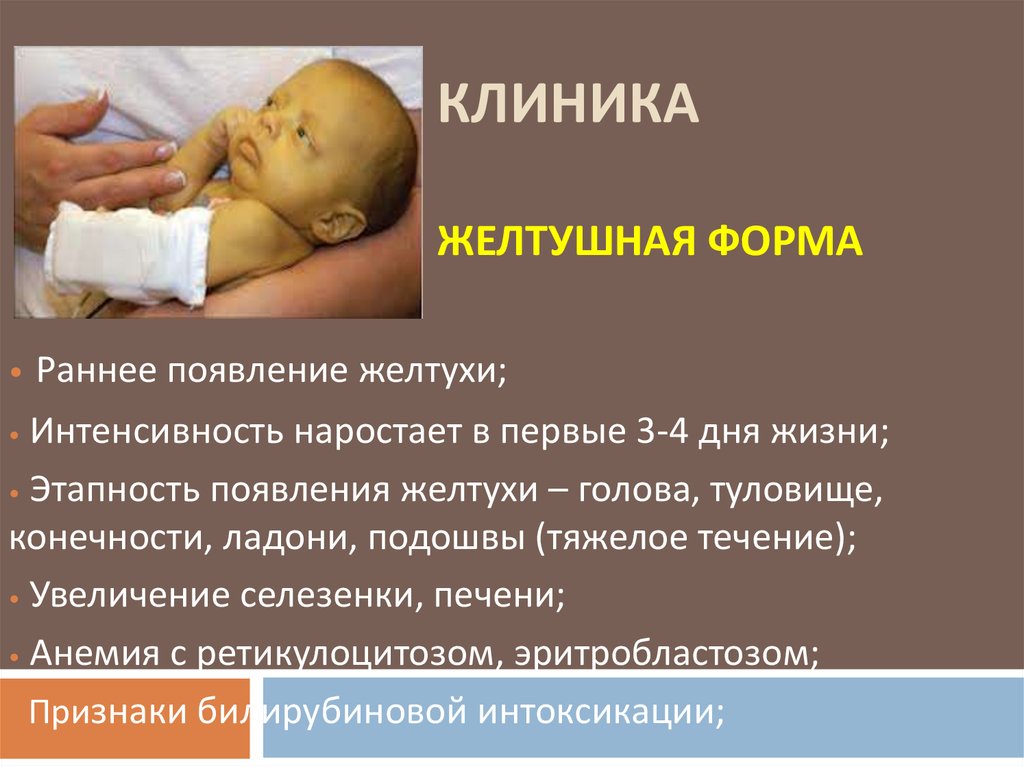
У детей с синдромом гипервозбудимости отмечается усиленная спонтанная двигательная активность, нарушение сна (удлинение периода бодрствования, трудности засыпания, прерывистый сон, вздрагивания во сне). Несмотря на хороший уход и достаточное количество пищи, дети ведут себя беспокойно, часто и беспричинно плачут. Во время крика у ребенка развиваются вегетативные реакции: акроцианоз, мраморность или покраснение кожных покровов, тахипноэ, тахикардия, усиление потливости. Дети с синдромом гипервозбудимости плохо берут грудь, часто прерываются во время кормления, склонны к обильным срыгиваниям, пищеварительным расстройствам (чередованию поносов и запоров), плохого прибавляют в весе.
Характерными признаками синдрома гипервозбудимости у детей служат переменный мышечный тонус, тремор подбородка и рук, клонусы стоп, оживление врожденных безусловных рефлексов (спонтанного рефлекса Моро), горизонтальный нистагм. Различные внешние стимулы вызывают у детей быстрое развитие двигательных, сенсорных и эмоциональных реакций, которые столь же быстро угасают, что свидетельствует о повышенной психической истощаемости.
У недоношенных детей синдром гипервозбудимости обычно является отражением снижения порога судорожной готовности, поэтому у таких малышей могут легко развиваться судороги (при гипертермии, действии чрезмерных раздражителей и т. п.).
В случае благоприятного течения выраженность проявлений синдрома гипервозбудимости у детей обычно уменьшается к 4-6 месяцам и исчезает в сроки до 1 года. В противном случае, по мере развития ребенка может обнаруживаться негрубое отставание в психомоторном и речевом развитии, гиперактивность, энурез, энкопрез, заикание, тики, парасомнии, тревожные расстройства, эпилепсия.
Диагностика у детей
Правильная оценка причин и проявлений синдрома гипервозбудимости у детей может быть дана только детскими специалистами: педиатром и детским неврологом. Осмотр таких детей должен проводиться осторожно, поскольку незнакомая обстановка, раздевание, касание тела холодными инструментами может вызвать у ребенка сопротивление обследованию, повышение тонуса мышц, плач, затрудняющие интерпретацию объективных данных.
После сбора перинатального анамнеза для уточнения диагноза может потребоваться инструментальное дообследование: УЗИ и рентгенография шейного отдела позвоночника, нейросонография, УЗДГ и дуплексное сканирование сосудов головного мозга, электроэнцефалография, электронейромиография. Дополнительные исследования дают представление о наличии или отсутствии органических поражений ткани и сосудов головного мозга, особенностях протекания электрофизиологических процессов в нервно-мышечной ткани.
Главной задачей диагностики синдрома гипервозбудимости у детей является определение его причин (неврологических, метаболических, психологических, соматических и др.), отчего будет зависеть лечебная тактика.
Лечение синдрома гипервозбудимости у детей
При синдроме гипервозбудимости, связанном с перинатальным поражением ЦНС, на первом году жизни детям показаны неоднократные курсы массажа, ЛФК, гидротерапии (плавание, солевые и хвойные ванны), физиотерапии (электрофорез, амплипульстерапия, парафиновые аппликации и др.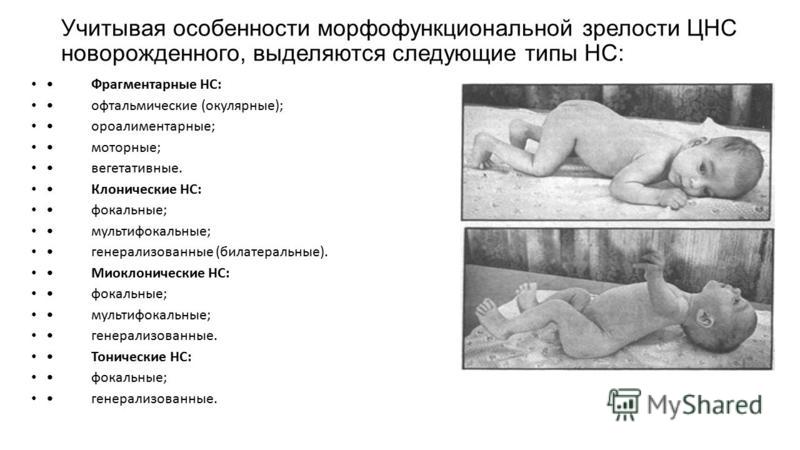
По мере его взросления ребенку может потребоваться помощь логопеда и детского психолога.
Прогноз и профилактика
Профилактика синдрома гипервозбудимости у детей заключается в предупреждении перинатального поражения ЦНС: внутриутробной гипоксии и инфицирования плода, внутричерепных родовых травм, повреждений позвоночника у новорожденных и т. д. После рождения малыша наибольшее значение приобретает полноценное вскармливание, закаливание, соблюдение режима, проведение профилактического массажа и гимнастики.
При отсутствии внимания к проблеме гипервозбудимости, все проявления синдрома у детей могут усилиться в раннем и дошкольном возрасте. В будущем у таких детей могут сформироваться стойкие невротические расстройства, нарушения поведения и социальная дезадаптация. Дети с синдромом гипервозбудимости нуждаются в наблюдении невролога и периодических курсах поддерживающей терапии.
В будущем у таких детей могут сформироваться стойкие невротические расстройства, нарушения поведения и социальная дезадаптация. Дети с синдромом гипервозбудимости нуждаются в наблюдении невролога и периодических курсах поддерживающей терапии.
Источники
- Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гиперестезия — StatPearls — NCBI Bookshelf
Продолжение обучения
Гиперестезия возникает как симптом невропатической боли и может присутствовать при любом болезненном процессе, поражающем соматосенсорную нервную систему. Лечение включает лечение основных состояний и симптоматическую поддержку. Мультидисциплинарный подход, способный обеспечить своевременную диагностику и лечение, дает наилучшие результаты. В этом упражнении описывается оценка и лечение гиперестезии, а также рассматривается роль межпрофессиональной команды в оценке и лечении пациентов с этим заболеванием.
Мультидисциплинарный подход, способный обеспечить своевременную диагностику и лечение, дает наилучшие результаты. В этом упражнении описывается оценка и лечение гиперестезии, а также рассматривается роль межпрофессиональной команды в оценке и лечении пациентов с этим заболеванием.
Цели:
-
Обобщите этиологию гиперестезии.
-
Определите, какие исследования подходят для постановки диагноза гиперестезии.
-
Опишите стратегию лечения гиперестезии/нейропатической боли.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Международная ассоциация по изучению боли определяет гиперестезию как «повышенную чувствительность к стимуляции, за исключением специальных органов чувств», которая «может относиться к различным видам кожной чувствительности, включая прикосновение и тепловое ощущение без боли, а также к боль.» В то время как гиперестезия может использоваться для описания любой повышенной чувствительности к раздражителю, она обычно используется для описания болезненных ощущений от раздражителя.
Гиперестезия является частым симптомом невропатической боли. Международная ассоциация по изучению боли определяет нейропатическую боль как «боль, вызванную поражением или заболеванием соматосенсорной системы». Фенотип нейропатической боли содержит спектр симптомов, которые можно условно разделить на положительные и отрицательные симптомы. Гиперестезия является положительным симптомом невропатической боли. Положительные симптомы подразделяются на стимул-зависимую боль, стимул-независимую боль и парестезии.[1] Нейропатическая боль затрагивает около 7-8% населения в целом.[2][3]
В этой статье гиперестезия определяется как повышенная кожная чувствительность, проявляющаяся в виде стимул-зависимой невропатической боли. Наиболее распространенными гиперестезиями являются аллодиния и гипералгезия. Аллодиния — это боль, вызванная раздражителем, который обычно не вызывает болевой реакции (например, боль при легком прикосновении). Гипералгезия — это преувеличенная болевая реакция на раздражитель, который обычно вызывает боль (т. е. непропорциональная боль от укола булавкой). В то время как большинство нейропатических болевых симптомов локализуются в пределах дерматомного распределения пораженного нерва, известно, что гиперестезия распространяется за пределы распределения пораженного нерва. Иногда это может затруднить постановку правильного диагноза и привести к неправильной диагностике психосоматического расстройства.[4]
е. непропорциональная боль от укола булавкой). В то время как большинство нейропатических болевых симптомов локализуются в пределах дерматомного распределения пораженного нерва, известно, что гиперестезия распространяется за пределы распределения пораженного нерва. Иногда это может затруднить постановку правильного диагноза и привести к неправильной диагностике психосоматического расстройства.[4]
Подробного анамнеза и тщательного медицинского осмотра должно быть достаточно для определения основной этиологии. Обычные лаборатории должны быть заказаны как часть исследования. Для постановки окончательного диагноза этиологии может потребоваться назначение специальных лабораторных, диагностических и визуализирующих тестов. Лечение поддающихся лечению и обратимых этиологий требует незамедлительного лечения. Основой лечения является симптоматическое облегчение с помощью фармакологической, нефармакологической и интервенционной терапии. Симптомы, как правило, сложно устранить, и пациенты, скорее всего, будут продолжать испытывать постоянные симптомы. Было показано, что междисциплинарный командный подход обеспечивает наиболее эффективные и устойчивые результаты.
Было показано, что междисциплинарный командный подход обеспечивает наиболее эффективные и устойчивые результаты.
Этиология
Нейропатические болевые симптомы, включая гиперестезию, развиваются вторично по отношению к заболеванию или поражению нервной системы, приводящему к нарушению функционирования соматосенсорной системы. Этиология гиперестезии может быть классифицирована анатомически или этиологически. С анатомической точки зрения источник может быть как центральным, так и периферическим.
Периферийный
-
Системные заболевания: сахарный диабет (СД), дефицит питательных веществ, гипотиреоз, васкулит, саркоидоз, карцинома/паранеопластический рак, синдром Гийена-Барре/острая воспалительная демиелинизирующая полинейропатия, хронические демиелинизирующие воспалительные невропатии, моноклональная гаммапатия (амилоидоз, множественная миелома, плазмоцитома) , моноклональная гаммапатия неустановленной значимости), порфирия, синдром Шегрена и критическое состояние.

-
Инфекционные: вирусы иммунодефицита человека (ВИЧ), Т-клеточный лимфотропный вирус человека, вирус простого герпеса, вирус ветряной оспы, вирус Эбштейна-Барр, вирус Западного Нила, вирус гепатита С, вирус бешенства, цитомегаловирус, дифтерия, кампилобактер jejuni, Mycobacterium tuberculosis, Mycobacterium leprae, Brucella spp., Clostridium botulinum и Borrelia burgdorferi.[5]
-
Токсичные:
-
-
Лекарственные препараты: изониазид, химиотерапевтические средства (алкалоиды барвинка, таксаны, соединения платины), статины, амиодарон, противомикробные препараты (изониазид, линезолид и метронидазол) ) и иммунодепрессанты (ингибиторы фактора некроза опухоли, лефлуномид и нуклеозидные аналоги ингибиторов обратной транскриптазы) [6].
-
Прочие токсины: этанол и тяжелые металлы
-
-
Механические: травмы, компрессионные мононейропатии, комплексный регионарный болевой синдром, постампутационные боли/фантомные боли в конечностях, невралгия тройничного нерва, постмастэктомический болевой синдром, несостоятельность спины хирургический синдром и радикулопатии (компрессия нервных корешков)
-
Наследственные: болезнь Шарко-Мари-Тута и метахроматическая лейкодистрофия
Центральная
-
Системные заболевания: миелопатия B12, рассеянный склероз, инсульт спинного мозга, мозговой инсульт/центральный постинсультный болевой синдром (CPSP), опиоид-индуцированная гипералгезия и инфекционные заболевания (вирус простого герпеса, миелит, энцефалит)
-
Механические: повреждение спинного мозга, компрессия опухолью (головного и спинного мозга), сирингомиелия и миелопатия[1][7][8][9]
Эпидемиология
Эпидемиологические исследования гиперестезии технически сложны. Препятствия для проведения точных эпидемиологических исследований включают огромное количество состояний, которые могут вызывать гиперестезию, и субъективный характер гиперестезии. Два эпидемиологических исследования, посвященные распространенности хронической боли с признаками невропатической боли, показали, что распространенность невропатической боли среди населения в целом составляет от 7% до 8%.[2][3]
Препятствия для проведения точных эпидемиологических исследований включают огромное количество состояний, которые могут вызывать гиперестезию, и субъективный характер гиперестезии. Два эпидемиологических исследования, посвященные распространенности хронической боли с признаками невропатической боли, показали, что распространенность невропатической боли среди населения в целом составляет от 7% до 8%.[2][3]
В одном исследовании, в котором использовался вопросник для оценки сенсорных симптомов у пациентов с болезненной диабетической невропатией (ПДН) и постгерпетической невралгией (ПГН), было обнаружено, что аллодиния присутствовала примерно у 50% пациентов с ПГН. В этом исследовании приняли участие 1600 пациентов с ПДН, из которых 18% сообщили о боли при легком прикосновении, а 14% сообщили о периодической боли при жаре или холоде.[10] В другом исследовании было проведено количественное сенсорное тестирование 1236 пациентов с диагностированной невропатической болью. В исследовании использовались как механические, так и термические раздражители. Их результаты показали, что у 20% пациентов была аллодиния, спровоцированная щеткой. Исследование также показало, что механическая гипералгезия (булавочный укол 29% и тупое давление 36%) встречались чаще, чем термическая гипералгезия (горячая 24% и холодная 19%).[11]
Их результаты показали, что у 20% пациентов была аллодиния, спровоцированная щеткой. Исследование также показало, что механическая гипералгезия (булавочный укол 29% и тупое давление 36%) встречались чаще, чем термическая гипералгезия (горячая 24% и холодная 19%).[11]
Патофизиология
Патофизиология невропатической боли была тщательно изучена, и было выявлено несколько важных механизмов. Некоторые из выявленных механизмов дают четкое объяснение развития гиперестезии.[7] Механизмами, приводящими к развитию гиперестезии, являются центральная сенсибилизация соматосенсорной системы, периферическая сенсибилизация соматосенсорной системы и дисфункция эндогенного торможения боли. Считается, что механическая гиперестезия (например, легкий укол булавкой и легкое мануальное давление) и механическая аллодиния (т. е. поглаживание кожи щеткой) обусловлены сенсибилизацией соматосенсорной системы (т. е. периферической сенсибилизацией и центральной сенсибилизацией) и дисфункцией эндогенное подавление боли.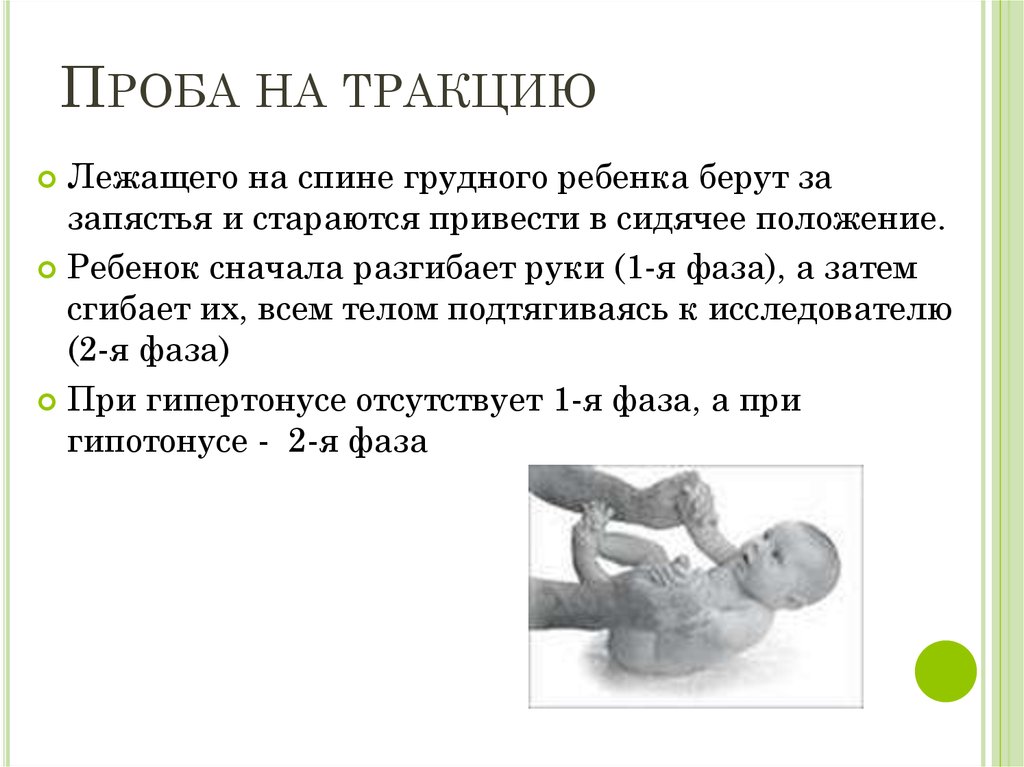 [12] Считается, что холодовая гиперестезия обусловлена либо периферической сенсибилизацией, либо центральной расторможенностью. Считается, что тепловая гиперестезия возникает из-за периферической сенсибилизации нервных волокон.[13]
[12] Считается, что холодовая гиперестезия обусловлена либо периферической сенсибилизацией, либо центральной расторможенностью. Считается, что тепловая гиперестезия возникает из-за периферической сенсибилизации нервных волокон.[13]
-
Центральная сенсибилизация определяется как увеличение синаптической эффективности и возбудимости ноцицептивных путей в центральной нервной системе (ЦНС). Благодаря этому механизму усиливаются болевые сигналы, поступающие в ЦНС. Процесс, посредством которого происходит центральная сенсибилизация соматосенсорной системы, изучен недостаточно. Один из предложенных механизмов предполагает, что сенсорные клетки A-бета претерпевают фенотипические изменения, которые затем выражают повышенный уровень нейропептидов и повышенную активность передачи аминокислот.
-
Периферическая сенсибилизация чаще всего возникает после воспаления периферических нервов и приводит к снижению порога активации и повышенной возбудимости первичных афферентных нейронов.
 Считается, что это происходит из-за посттрансляционных изменений, переноса и экспрессии члена 1 подсемейства V подсемейства катионных каналов временного рецепторного потенциала (TRPV1), которые возникают после повреждения нерва. После этих изменений периферические нервы становятся более чувствительными к механическим и термическим раздражителям.[13]
Считается, что это происходит из-за посттрансляционных изменений, переноса и экспрессии члена 1 подсемейства V подсемейства катионных каналов временного рецепторного потенциала (TRPV1), которые возникают после повреждения нерва. После этих изменений периферические нервы становятся более чувствительными к механическим и термическим раздражителям.[13] -
Дисфункция эндогенного торможения боли, скорее всего, возникает из-за снижения ГАМК и ингибирования глицином нейронов второго порядка, что приводит к чистому возбуждению этих нейронов.[14]
Анамнез и физикальное исследование
Анамнез: Должен быть собран тщательный анамнез, так как этого должно быть достаточно для постановки диагноза гиперестезии.
-
Анамнез заболевания (сахарный диабет, инсульт, переломы, синдром раздраженного кишечника)
-
Психиатрический анамнез (аффективные расстройства)
-
Лекарства (применение нейротоксических препаратов)
-
Хирургия
-
Семейный анамнез
-
Сексуальный анамнез
-
Злоупотребление психоактивными веществами (алкоголем или опиоидами)
-
Функциональный анамнез: Должен быть выполнен функциональный анамнез, который исследует влияние симптомов пациента на его способность функционировать.
 Он должен быть сосредоточен на любых нарушениях повседневной деятельности пациента, инструментальной деятельности в повседневной жизни, амбулаторном статусе (использовании вспомогательных устройств), работе или сне.[4]
Он должен быть сосредоточен на любых нарушениях повседневной деятельности пациента, инструментальной деятельности в повседневной жизни, амбулаторном статусе (использовании вспомогательных устройств), работе или сне.[4] -
История болезни: Исследователь должен собрать подробное описание болевых симптомов пациента. Описание симптомов пациента должно включать все следующие компоненты.
-
Местоположение
-
Интенсивность (оценочная шкала от 0 до 10)
-
Качество (жжение, холод, жар или аллодиния) Болевые дескрипторы, такие как жжение, покалывание или стреляющая боль, наиболее характерны для невропатии болевой синдром и имеют высокую вероятность присутствия наряду с гиперестезией.[7]
-
Начало (появились ли симптомы после провоцирующего события)
-
Временные вариации: В какое время суток боль усиливается? (нейропатическая боль, как правило, усиливается к концу дня) Боль постепенно усиливалась в течение некоторого времени?
-
Иррадиация (имеет ли боль аксиальное происхождение)
-
Изменение положения (т.
 е. сильнее ли боль в пояснице или бедре)
е. сильнее ли боль в пояснице или бедре) -
Отягчающие/облегчающие факторы
-
Попытки лечения (симптомы невропатической боли, как правило, не реагируют на ацетаминофен или нестероидные противовоспалительные препараты)
-
Частота
-
Сопутствующие симптомы (потеря диапазона движений, изменения кожи или волос, спазм мышц) смс, мышечная слабость, изменения чувствительности, покраснение или отек)
-
Физикальное обследование: В дополнение к общему целенаправленному физикальному обследованию необходимо провести полное неврологическое обследование.
-
Исследование черепных нервов (поражения ЦНС могут сопровождаться поражением черепных нервов)
-
Мануальное моторное исследование (слабость может быть как периферической, так и центральной этиологии, и любую слабость следует дифференцировать как реальную слабость или анталгическую слабость)
-
Глубокие сухожильные рефлексы (могут быть повышены при центральной этиологии и снижены при периферической этиологии)0004 Легкое прикосновение (аллодиния)
-
Укол булавкой (гипералгезия)
-
Вибрация и проприоцепция
Температура (лед и горячий компресс) s для возможной термической аллодинии)
Тест на прямую ногу или тест на сгибание (радикулопатия
Симптом Тинеля (защемление периферического нерва)
Миофасциальные триггерные точки
изменения цвета, потливость, рубцы при дерматомном распространении и изменениях волос.
Оценка
Первым шагом должно быть определение того, является ли этиология периферической или центральной. Очень важно точно диагностировать причину гиперестезии, чтобы обеспечить лечение любой излечимой основной причины.
Лабораторные исследования:
-
Рутинно: следует рассматривать как часть стандартного обследования периферической гиперестезии
-
-
Общий анализ крови
-
Комплексная метаболическая панель
-
Глюкоза крови натощак
-
Скорость оседания эритроцитов
-
Тиреотропный гормон
-
Витамин B12
-
-
По показаниям, на основании клинического подозрения:
-
-
Гемоглобин A1c (HbA1c)
-
Антитела к ВИЧ
-
Панель печени
-
Лайм-антитела
-
Экспресс-реагин плазмы (RPR), лаборатория исследований венерических болезней (VDRL)
-
Анализ мочи
-
Электрофорез белков мочи
- 90 004 Электрофорез белков сыворотки
-
Уровни ангиотензинпревращающего фермента
-
Тест на антинуклеарные антитела (ANA)
-
Тест на перинуклеарные антинейтрофильные цитоплазматические антитела (P-ANCA)
-
Тест на антинейтрофильные цитоплазматические антитела (C-ANCA)
-
-
Тесты на редкие состояния
-
-
Паранеопластическая панель
-
Антимиелин-ассоциированный гликопротеин
9 0014 -
Антиганглиозидные антитела
-
Скорость слюноотделения
-
Анализ спинномозговой жидкости
-
Генетический тестирование
-
Визуализация: визуализация обычно не требуется для диагностики гиперестезии, но она помогает диагностировать определенные состояния.
-
Компьютерная томография и магнитно-резонансная томография (компрессия нервных корешков, грыжа диска, миелопатия, опухоль головного или спинного мозга)
-
Трехфазное сканирование костей (может использоваться для подтверждения диагноза КРБС)[7 ]
Специальные тесты:
-
Электродиагностика: электромиография и исследования нервной проводимости (только тесты крупных волокон)
-
Пункционная биопсия кожи (выявляет невропатию мелких волокон)[7]
Лечение/управление
Лечение гиперестезии и других симптомов невропатической боли представляет собой сложную задачу, но лучше всего достигается с помощью междисциплинарного командного подхода, который может сосредоточиться на лечении основных причин, назначении фармакотерапии, применении интервенционной терапии, устранении функциональных нарушений и обеспечении психиатрические услуги, если это необходимо.[7][9] Реалистичные цели для гиперестезии должны быть установлены на ранней стадии. Любые сопутствующие заболевания, такие как расстройства настроения или нарушения сна, следует лечить незамедлительно. Пациенты, как правило, требуют тщательного наблюдения для мониторинга реакции на терапию и постоянной оценки основной причины.
Любые сопутствующие заболевания, такие как расстройства настроения или нарушения сна, следует лечить незамедлительно. Пациенты, как правило, требуют тщательного наблюдения для мониторинга реакции на терапию и постоянной оценки основной причины.
Наиболее распространенными излечимыми причинами периферической невропатии являются сахарный диабет, гипотиреоз и дефицит питательных веществ.[8] Другие причины гиперестезии, такие как компрессия нервных корешков или защемление периферических нервов, могут первоначально лечиться консервативно с симптоматической фармакотерапевтической поддержкой, физиотерапией, изменением образа жизни и минимально инвазивными процедурами (например, эпидуральной инъекцией стероидов или инъекцией периферического нерва). Однако при ухудшении или застое функции может потребоваться хирургическое вмешательство.
Фармакологическое лечение может быть использовано для лечения как центральных, так и периферических причин гиперестезии. Из доступных фармакологических средств наиболее широко используются антидепрессанты и противоэпилептические препараты. [15] Общие рекомендации по лечению приведены ниже; тем не менее, даны рекомендации по выбору лечения для конкретных этиологий.
[15] Общие рекомендации по лечению приведены ниже; тем не менее, даны рекомендации по выбору лечения для конкретных этиологий.
Препараты первой линии: Эти препараты имеют наиболее существенные доказательства в поддержку их лечения симптомов невропатической боли. Эта группа содержит два класса антидепрессантов и один класс противоэпилептических препаратов.
-
Антидепрессанты: все препараты этого класса обладают дополнительным преимуществом лечения сопутствующих расстройств настроения. ТЦА: амитриптилин, имипрамин и нортриптилин 49 (PHN), центральная постинсультная боль (ЦББ)
SNRIs : дулоксетин и венлафаксин
-
Показания: БДН, посттравматическая невропатическая боль, КРБС, радикулопатия и центральная боль
Противоэпилептические препараты:
-
Габапентиноиды: габапентин и прегабалин
-
-
Показания: ПДН, ПГН, центральная боль, посттравматическая невропатическая боль, КРБС, радикулопатия.
 Прегабалин доказал свою эффективность при лечении центральной боли при травме спинного мозга.[16][17]
Прегабалин доказал свою эффективность при лечении центральной боли при травме спинного мозга.[16][17]
-
Лечение второй линии:
Препараты третьего ряда:
Не все пациенты реагируют на монотерапию; на самом деле, 45% людей с невропатической болью принимают два или более обезболивающих препарата. Если пациенту не помогает монотерапия первой линии, их можно использовать в комбинации (например, габапентиноид + ТЦА или СИОЗСН) [18].
Интервенционная терапия:
-
Эпидуральные инъекции стероидов: считается терапией третьей линии.
-
Блокада симпатического нерва
-
Нейростимуляция: терапия четвертой линии[18] 0005
Чрескожная электрическая стимуляция нервов (ЧЭНС)
Для некоторых интервенционных методов лечения, применяемых в настоящее время, отсутствуют надежные испытания, которые могли бы быть рекомендованы руководствами. Некоторые из вмешательств, требующих продолжения исследований, включают радиочастотную денервацию ганглия задних корешков, адгезиолизис для FBSS, TENS, стимуляцию спинного мозга и стимуляцию моторной коры.
Некоторые из вмешательств, требующих продолжения исследований, включают радиочастотную денервацию ганглия задних корешков, адгезиолизис для FBSS, TENS, стимуляцию спинного мозга и стимуляцию моторной коры.
Дифференциальный диагноз
-
Ноцицептивный источник боли
-
Миофасциальный болевой синдром
-
Фибромиалгия
90 011
Синдром хронической усталости
Прогноз
Полностью устранить гиперестезии и другие нейропатические болевые симптомы сложно . Это следует объяснить пациенту в начале курса лечения. Первоначально следует начинать монотерапию; однако 45 % пациентов с невропатической болью принимают два или более обезболивающих препарата.
Осложнения
Осложнения гиперестезии включают повышенную заболеваемость, если симптомы не контролируются. Пациент также может испытывать повышенную заболеваемость в результате обширных интервенционных процедур. Кроме того, если пациент начинает лечение сильнодействующими опиоидами, у него может развиться зависимость.
Консультации
Могут потребоваться консультации со следующими лицами:
-
Специалист по обезболиванию
-
Специалист по сомнологии
-
Физиотерапия
-
Трудотерапия
-
Психиатр
-
Психолог
9001 4 -
Невролог
-
Нейрохирург
Устрашение и обучение пациентов
Вот важные моменты, на которые следует обратить внимание :
-
Управление ожиданиями пациента имеет решающее значение в плане лечения. Гиперестезия и другие нейропатические болевые симптомы трудно поддаются контролю, и полное разрешение, скорее всего, никогда не будет достигнуто. Важно обсудить это с пациентом на ранней стадии курса лечения.
-
С гиперестезией и другими нейропатическими болевыми симптомами лучше всего справится междисциплинарная бригада. Это обеспечивает наилучший контроль над болью и дает наилучшие результаты.
-
Лечение следует проводить поэтапно.

-
Интервенционные процедуры должны быть предложены пациентам, которые не получают адекватного фармакотерапии или хотят отказаться от препаратов высокого риска, таких как опиоиды.
-
Крайне важно лечить сопутствующие заболевания, такие как расстройства настроения и проблемы со сном.
-
Текущий план лечения и возможные методы лечения следует регулярно обсуждать с пациентом.
Улучшение результатов работы медицинской бригады
Раннее выявление гиперестезии и других нейропатических болевых симптомов необходимо для того, чтобы пациент начал следовать правильному плану лечения. Обучение пациента на ранней стадии лечения необходимо для установления реалистичных целей в отношении боли. Всегда обращайтесь с междисциплинарным командным подходом. В то время как врач общей практики почти всегда участвует в уходе за пациентами с гиперестезией, важно проконсультироваться с межпрофессиональной командой специалистов, в которую входят специалисты по обезболиванию, специалистам по сну, физиотерапии и трудотерапии. Рекомендуется обследование у психиатра и психолога, так как многие пациенты страдают расстройствами настроения.
Рекомендуется обследование у психиатра и психолога, так как многие пациенты страдают расстройствами настроения.
Контрольные вопросы
-
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
-
Комментарий к этой статье.
Ссылки
- 1.
-
Gilron I, Baron R, Jensen T. Нейропатическая боль: принципы диагностики и лечения. Мэйо Клин Proc. 2015 Апрель; 90 (4): 532-45. [PubMed: 25841257]
- 2.
-
Bouhassira D, Lantéri-Minet M, Attal N, Laurent B, Touboul C. Распространенность хронической боли с нейропатическими характеристиками среди населения в целом. Боль. 2008 г., июнь; 136 (3): 380–387. [В паблике: 17888574]
- 3.
-
Торранс Н., Смит Б.Х., Беннетт М.И., Ли А.Дж. Эпидемиология хронической боли преимущественно невропатического генеза. Результаты общего опроса населения. Джей Пейн. 2006 апр; 7 (4): 281-9. [PubMed: 16618472]
- 4.

-
Gilron I, Watson CP, Cahill CM, Moulin DE. Нейропатическая боль: практическое руководство для клинициста. CMAJ. 2006 01 августа; 175 (3): 265-75. [Бесплатная статья PMC: PMC1513412] [PubMed: 16880448]
- 5.
-
Брицци КТ, Лайонс Дж.Л. Проявления периферической нервной системы при инфекционных заболеваниях. нейрогоспиталист. 2014 Октябрь; 4 (4): 230-40. [Статья PMC бесплатно: PMC4212417] [PubMed: 25360209]
- 6.
-
Вилхольм О.Дж., Кристенсен А.А., Зедан А.Х., Итани М. Лекарственная периферическая невропатия. Основной Клин Фармакол Токсикол. 2014 г., август; 115 (2): 185–92. [PubMed: 24786912]
- 7.
-
Watson JC, Dyck PJ. Периферическая невропатия: практический подход к диагностике и лечению симптомов. Мэйо Клин Proc. 2015 июль;90(7):940-51. [PubMed: 26141332]
- 8.
-
Ажари Х., Фарук М.Ю., Бханушали М., Маджид А., Кассаб М.Ю. Периферическая невропатия: дифференциальная диагностика и лечение.
 Ам семейный врач. 01 апреля 2010 г .; 81 (7): 887–92. [PubMed: 20353146]
Ам семейный врач. 01 апреля 2010 г .; 81 (7): 887–92. [PubMed: 20353146] - 9.
-
Zilliox LA. Нейропатическая боль. Континуум (Миннеап Минн). 23 апреля 2017 г. (2, Избранные темы амбулаторной неврологии): 512–532. [PubMed: 28375916]
- 10.
-
Baron R, Tölle TR, Gockel U, Brosz M, Freynhagen R. Поперечное когортное исследование 2100 пациентов с болезненной диабетической невропатией и постгерпетической невралгией: различия в демографических данных и сенсорные симптомы. Боль. 2009 г.Ноябрь; 146 (1-2): 34-40. [PubMed: 19592166]
- 11.
-
Johnson RW, Wasner G, Saddier P, Baron R. Опоясывающий герпес и постгерпетическая невралгия: оптимизация лечения пожилых пациентов. Наркотики Старение. 2008;25(12):991-1006. [PubMed: 1
99]
- 12.
-
Гиртмюлен Дж., барон Р. Нейропатическая боль. Семин Нейрол. 2016 окт; 36 (5): 462-468. [PubMed: 27704502]
- 13.
-
фон Хен К.А., барон Р.
 , Вульф К.Дж. Деконструкция фенотипа нейропатической боли для выявления нейронных механизмов. Нейрон. 2012 23 февраля; 73 (4): 638-52. [Бесплатная статья PMC: PMC3319438] [PubMed: 22365541]
, Вульф К.Дж. Деконструкция фенотипа нейропатической боли для выявления нейронных механизмов. Нейрон. 2012 23 февраля; 73 (4): 638-52. [Бесплатная статья PMC: PMC3319438] [PubMed: 22365541] - 14.
-
Дженсен Т.С., Финнеруп Н.Б. Аллодиния и гипералгезия при нейропатической боли: клинические проявления и механизмы. Ланцет Нейрол. 2014 сен; 13 (9): 924-35. [PubMed: 25142459]
- 15.
-
Finnerup NB, Attal N, Haroutounian S, McNicol E, Baron R, Dworkin RH, Gilron I, Haanpää M, Hansson P, Jensen TS, Kamerman PR, Lund K, Mo руда A, Raja SN, Rice AS, Rowbotham M, Sena E, Siddall P, Smith BH, Wallace M. Фармакотерапия невропатической боли у взрослых: систематический обзор и метаанализ. Ланцет Нейрол. 2015 Февраль; 14 (2): 162-73. [Бесплатная статья PMC: PMC4493167] [PubMed: 25575710]
- 16.
-
Siddall PJ, Cousins MJ, Otte A, Griesing T, Chambers R, Murphy TK. Прегабалин при центральной нейропатической боли, связанной с повреждением спинного мозга: плацебо-контролируемое исследование.
 Неврология. 2006 28 ноября; 67 (10): 1792-800. [PubMed: 17130411]
Неврология. 2006 28 ноября; 67 (10): 1792-800. [PubMed: 17130411] - 17.
-
Cardenas DD, Nieshoff EC, Suda K, Goto S, Sanin L, Kaneko T, Sporn J, Parsons B, Soulsby M, Yang R, Whalen E, Scavone JM, Suzuki ММ, Кнапп Л.Е. Рандомизированное исследование прегабалина у пациентов с нейропатической болью, вызванной повреждением спинного мозга. Неврология. 2013 05 февраля; 80 (6): 533-9. [Бесплатная статья PMC: PMC3589291] [PubMed: 23345639]
- 18.
-
Bates D, Schultheis BC, Hanes MC, Jolly SM, Chakravarthy KV, Deer TR, Levy RM, Hunter CW. Комплексный алгоритм лечения нейропатической боли. Боль Мед. 2019 01 июня; 20 (Приложение 1): S2-S12. [Бесплатная статья PMC: PMC6544553] [PubMed: 31152178]
- 19.
-
Чоу Р., Лозер Дж. Д., Оуэнс Д. К., Розенквист Р. В., Атлас С. Дж., Байсден Дж., Карраджи Э. Дж., Грабуа М., Мерфи Д. Р., Ре сник ДК, Станос С.П., Шаффер В.О., Уолл Э.М., Группа рекомендаций Американского общества по борьбе с болью в нижней части спины.
 Интервенционная терапия, хирургия и междисциплинарная реабилитация при болях в пояснице: научно-обоснованное руководство по клинической практике Американского общества боли. Позвоночник (Фила Па 1976). 2009 01 мая; 34 (10): 1066-77. [PubMed: 19363457]
Интервенционная терапия, хирургия и междисциплинарная реабилитация при болях в пояснице: научно-обоснованное руководство по клинической практике Американского общества боли. Позвоночник (Фила Па 1976). 2009 01 мая; 34 (10): 1066-77. [PubMed: 19363457] - 20.
-
Manchikanti L, Abdi S, Atluri S, Benyamin RM, Boswell MV, Buenaventura RM, Bryce DA, Burks PA, Caraway DL, Calodney AK, Cash KA, Christo PJ, Co курица SP, Colson J, Conn A, Cordner H, Coubarous S, Datta S, Deer TR, Diwan S, Falco FJ, Fellows B, Geffert S, Grider JS, Gupta S, Hameed H, Hameed M, Hansen H, Helm S, Джаната Дж.В., Джастис Р., Кэй А.Д., Ли М., Манчиканти К.Н., Макманус К.Д., Оньеву О., Парр А.Т., Патель В.Б., Рач Г.Б., Сегал Н., Шарма М.Л., Симопулос Т.Т., Сингх В., Смит Х.С., Снук Л.Т., Суайсгуд Д.Р. , Вальехо Р., Уорд С.П., Варго Б.В., Чжу Дж., Хирш Дж.А. Обновление комплексных научно-обоснованных руководств по интервенционным методам лечения хронической боли в позвоночнике. Часть II: руководство и рекомендации.
 Врач боли. 2013 Апр; 16 (2 Приложение): S49-283. [PubMed: 23615883]
Врач боли. 2013 Апр; 16 (2 Приложение): S49-283. [PubMed: 23615883] - 21.
-
Дворкин Р.Х., О’Коннор А.Б., Кент Дж., Макки С.К., Раджа С.Н., Стейси Б.Р., Леви Р.М., Баконджа М., Барон Р., Харке Х., Лозер Д.Д., Триде Р.Д. , Терк, округ Колумбия, Уэллс, компакт-диск. Интервенционное лечение нейропатической боли: рекомендации NeuPSIG. Боль. 2013 ноябрь;154(11):2249-2261. [Бесплатная статья PMC: PMC4484720] [PubMed: 23748119]
- 22.
-
Cruccu G, Aziz TZ, Garcia-Larrea L, Hansson P, Jensen TS, Lefaucheur JP, Simpson BA, Taylor RS. Рекомендации EFNS по нейростимуляции при нейропатической боли. Евр Дж Нейрол. 2007 Сентябрь; 14 (9)):952-70. [PubMed: 17718686]
Хронический кашель: от сложной дисфункции неврологической цепи до возникновения упорного кашля
Текст статьи
Меню статьи
- Статья
Текст - Артикул
информация - Цитата
Инструменты - Поделиться
- Быстрое реагирование
- Артикул
метрика - Оповещения
Клиника грудной клетки
Мнение
Хронический кашель: от комплексной дисфункции неврологической цепи до возникновения упорного кашля
- Адальберто Пачеко
- Соответствие
Доктор Адальберто Пачеко, отделение хронического кашля, служба пульмонологии, больница Рамон-и-Кахаль, Crtra.
 Colmenar Km 9, Мадрид 28234, Испания; adalberto.pacheco{at}salud.madrid.org
Colmenar Km 9, Мадрид 28234, Испания; adalberto.pacheco{at}salud.madrid.org
Abstract
Хронический кашель или кашель, длящийся более 8 недель, после того, как рентгенограмма грудной клетки и спирометрия подтвердят норму, вызван изменением участка пути между периферическими рецепторами, главным образом в верхних и нижних дыхательных путей и пищевода, спинного мозга и кашлевого центра в стволе головного мозга с вовлечением коры. Эти механизмы кашля имеют свою гомологию в цепи хронической боли, и на этой основе следует расширить будущие исследования хронического кашля. Клинически хронический кашель легко диагностировать по чрезмерной реакции или гиперкашлю на раздражители низкой интенсивности или банальные раздражители, которые мы теперь называем синдромом гиперчувствительного кашля, количественно определяемым положительным рефлекторным кашлем с капсаицином или лимонной кислотой. Однако синдром гиперчувствительного кашля может быть невозможно количественно определить в лаборатории, если гиперреактивность возникает в центральной нервной системе. Обычно это вызвано чрезмерным периферическим входом или конвергенцией стимулов из разных источников. Как только центральная гиперчувствительность приобретена, периферический вход не так важен для активации кашля.
Обычно это вызвано чрезмерным периферическим входом или конвергенцией стимулов из разных источников. Как только центральная гиперчувствительность приобретена, периферический вход не так важен для активации кашля.
- Кашель/Механизмы/Фармакология
http://dx.doi.org/10.1136/thoraxjnl-2014-205661
Статистика с Altmetric.com
Запрос разрешений 9000 3
Если вы хотите повторно использовать некоторые или все эту статью, пожалуйста, используйте приведенную ниже ссылку, которая приведет вас к службе RightsLink Центра защиты авторских прав. Вы сможете получить быструю цену и мгновенное разрешение на повторное использование контента различными способами.
- Кашель/Механизмы/Фармакология
Распространенность хронического кашля (ХК), зарегистрированная в исследованиях, проведенных в Европе и США, колеблется от 9% до 30%.1 Однако у двух третей пациентов кашель полностью или частично не поддается обычному лечению.2 В В последнее десятилетие важным событием стало признание сходства между нейробиологическими механизмами, лежащими в основе кашля и боли. 3 К настоящему времени хроническая боль изучена достаточно глубоко, и теперь пришло время применить результаты исследований хронической боли к управление ЦК.
3 К настоящему времени хроническая боль изучена достаточно глубоко, и теперь пришло время применить результаты исследований хронической боли к управление ЦК.
Механизм кашля структурирован как неврологическая цепь, соединяющая периферию с центральной нервной системой (ЦНС). В некоторых случаях кора головного мозга включается в контур в виде ощущения позывов к кашлю или произвольного кашля, в отличие от другого вида кашля, кашлевого рефлекса. Как и при хронической боли, при ВК клиническая проблема возникает при длительном дисбалансе между стимулом и реакцией, что ухудшает качество жизни пациентов и вызывает у них кашель в ответ на слабые раздражители или даже в ответ на безобидные раздражители, такие как разговор или смеющийся. По этой причине этот продолжительный кашель в настоящее время классифицируется как синдром кашлевой гиперчувствительности4 или сенсорная гиперчувствительность к многочисленным механическим или химическим раздражителям, возникающим в различных анатомических областях, особенно в верхних и нижних дыхательных путях и пищеводе. Эти стимулы преобразуются в электрические потенциалы действия в терминальных волокнах блуждающих или тройничных нейронов, все из которых имеют свои клеточные тела в спинном мозге. Эти волокна, участвующие в кашлевом цикле, были тщательно изучены на лабораторных животных. В основном существует три типа5: рецепторы надувания и сдувания — быстро адаптирующиеся рецепторы и медленно адаптирующиеся рецепторы, — которые не играют большой роли в возникновении кашля; миелиновые волокна Aδ (называемые некоторыми авторами «кашлевыми рецепторами»), которые реагируют на механические раздражители и кислоты; и немиелинизированные С-волокна, которые реагируют на термические и химические раздражители, такие как капсаицин.
Эти стимулы преобразуются в электрические потенциалы действия в терминальных волокнах блуждающих или тройничных нейронов, все из которых имеют свои клеточные тела в спинном мозге. Эти волокна, участвующие в кашлевом цикле, были тщательно изучены на лабораторных животных. В основном существует три типа5: рецепторы надувания и сдувания — быстро адаптирующиеся рецепторы и медленно адаптирующиеся рецепторы, — которые не играют большой роли в возникновении кашля; миелиновые волокна Aδ (называемые некоторыми авторами «кашлевыми рецепторами»), которые реагируют на механические раздражители и кислоты; и немиелинизированные С-волокна, которые реагируют на термические и химические раздражители, такие как капсаицин.
Первым механизмом возникновения кашля является повышенная возбудимость окончаний периферических нервов на данный раздражитель. Многие типы химических раздражителей могут вызывать нейровоспалительную реакцию; эти стимулы были названы «воспалительным супом». Активация рецепторов TRPV1 и TRPA1, присутствующих в С-волокнах дыхательной системы, была тщательно изучена. Одно исследование на людях показало, что ингаляция простагландина Е2 усиливает кашлевую реакцию на последующую ингаляцию капсаицина,6 но также может иметь значение активация волокон Aδ; в модели морской свинки после аллерген-индуцированной активации тучных клеток наблюдалось состояние повышенной чувствительности к механическим раздражителям, активирующим эти ноцицепторы.7,
Одно исследование на людях показало, что ингаляция простагландина Е2 усиливает кашлевую реакцию на последующую ингаляцию капсаицина,6 но также может иметь значение активация волокон Aδ; в модели морской свинки после аллерген-индуцированной активации тучных клеток наблюдалось состояние повышенной чувствительности к механическим раздражителям, активирующим эти ноцицепторы.7,
Если повышение возбудимости происходит в терминальных волокнах двух разных типов, это может привести к явлению конвергенции и синергии перед кашлем. кислота (опосредованная С-волокнами, в дистальной трети пищевода) была спровоцирована у морских свинок; было показано, что ни одно из событий не было достаточным для того, чтобы вызвать кашель по отдельности, но одновременная стимуляция могла вызвать кашель.9У людей перфузия пищевода кислотой вызывала кашель только у субъектов с предшествующими состояниями раздражения дыхательных путей, такими как астма, но не у здоровых людей.10 Это сочетание двух участков активации было определено некоторыми авторами как источник висцеральной гиперчувствительности, полезного концепция для объяснения того, что даже нормальный уровень кислоты в дистальной трети пищевода у здоровых людей может в случае сопутствующего РХ повышать кашлевую чувствительность. в верхних дыхательных путях.12 Эти результаты показывают, что воздействие на два или более потенциальных источника кашля, таких как пищевод и верхние или нижние дыхательные пути, может быть полезным для лечения СС. Эта конкретная взаимосвязь была целью клинического исследования связи между гастроэзофагеальным рефлюксом и эозинофильным воспалением дыхательных путей.13,
в верхних дыхательных путях.12 Эти результаты показывают, что воздействие на два или более потенциальных источника кашля, таких как пищевод и верхние или нижние дыхательные пути, может быть полезным для лечения СС. Эта конкретная взаимосвязь была целью клинического исследования связи между гастроэзофагеальным рефлюксом и эозинофильным воспалением дыхательных путей.13,
Второй механизм предполагает более активное участие со стороны ЦНС в виде центральной сенсибилизации. Повторяющиеся периферические стимулы могут вызвать состояние центральной гиперчувствительности, которое может быть обратимым, хотя, если активность ноцицепторов сохраняется в течение долгого времени, это может вызвать гиперчувствительность, известную как спинальная долговременная потенциация. и ЦНС может развиваться. Один из них — через взаимодействие между терминальными волокнами, то есть когда сенсорная информация, поступающая по С-волокнам к кашлевому центру (ядру солитарного пути, расположенному в стволе мозга), активирует другие нервные окончания, чья чувствительность к этим раздражителям, вероятно, повышается за счет синаптическая пластичность в кашлевом контуре15; это имеет синергетический эффект и вызывает кашель. 9В одном исследовании на животных после стимуляции С-волокон в местах, где нет волокон Aδ, таких как периферия легких или слизистая оболочка пищевода, наблюдалось увеличение входного сигнала от волокон Aδ в слизистой оболочке гортани, трахеи и бронхов. наблюдаемый; затем совместное действие волокон Aδ и C-волокон приводит к увеличению центральной чувствительности.8 В контексте хронической боли возникает идентичное явление, известное как вторичная гипералгезия16; при кашле это состояние известно как вторичная гиперкашель, которая относится к тому, как сенсибилизация, возникающая в определенной соматической области, воспринимается как более распространенная, чем она есть на самом деле; например, периферическая стимуляция кислоты в пищеводе может быть воспринята ЦНС как вызванная рецепторами в других местах, таких как гортань или дыхательные пути.
9В одном исследовании на животных после стимуляции С-волокон в местах, где нет волокон Aδ, таких как периферия легких или слизистая оболочка пищевода, наблюдалось увеличение входного сигнала от волокон Aδ в слизистой оболочке гортани, трахеи и бронхов. наблюдаемый; затем совместное действие волокон Aδ и C-волокон приводит к увеличению центральной чувствительности.8 В контексте хронической боли возникает идентичное явление, известное как вторичная гипералгезия16; при кашле это состояние известно как вторичная гиперкашель, которая относится к тому, как сенсибилизация, возникающая в определенной соматической области, воспринимается как более распространенная, чем она есть на самом деле; например, периферическая стимуляция кислоты в пищеводе может быть воспринята ЦНС как вызванная рецепторами в других местах, таких как гортань или дыхательные пути.
Вторым потенциальным влиянием периферических раздражителей на ЦНС является эффект, оказываемый на первый нейрон кашлевой цепи микроглией, набором клеток костного мозга, которые участвуют в первичном иммунитете и активируются при хронической боли, продуцируя фактор некроза опухоли. α и интерлейкин-1b; возможно, его модуляция влияет на степень возбудимости спинного мозга в ответ на кашлевые раздражители.17 Последний фактор, о котором следует помнить, — это нисходящий контроль ядра одиночного пути из коры головного мозга (стимулирующий и тормозной), как в патофизиология хронической боли; в свою очередь, на этот контроль влияют синапсы в проводящих путях через периакведуктальный серый и лимбический мозг, в результате чего тревога и депрессия могут модулировать конечный эфферентный двигательный импульс.0005
α и интерлейкин-1b; возможно, его модуляция влияет на степень возбудимости спинного мозга в ответ на кашлевые раздражители.17 Последний фактор, о котором следует помнить, — это нисходящий контроль ядра одиночного пути из коры головного мозга (стимулирующий и тормозной), как в патофизиология хронической боли; в свою очередь, на этот контроль влияют синапсы в проводящих путях через периакведуктальный серый и лимбический мозг, в результате чего тревога и депрессия могут модулировать конечный эфферентный двигательный импульс.0005
Сенсибилизация классических участков диагностической триады РШМ — бронхов (эозинофильное или нейтрофильное воспаление), пищевода (кислота) и верхних дыхательных путей — может затем вызвать сенсибилизацию за счет конвергенции и синергизма в ЦНС участков, где присутствует кашлевых рецепторов максимально, например, гортани. Действительно, это может быть объяснением общих симптомов со стороны гортани и трахеи у пациентов с ВК всех видов, таких как зуд, покалывание, застой слизи, охриплость, стеснение в груди и т. разговор или пение вызывают кашель. Это состояние называется гиперкашелью (сенсибилизация к слабым раздражителям) или аллотассивностью (сенсибилизация к банальным раздражителям). Гортанные симптомы и триггеры РХ настолько важны, что некоторые авторы ввели понятие ларингеальной гиперчувствительности при РХ и считают его фундаментальным для клинического понимания состояния; на самом деле, они применяют его к нескольким связанным проблемам, таким как дисфункция голосовых связок, дисфония мышечного напряжения и даже тяжелая астма.18 В исследованиях гиперчувствительности гортани междисциплинарные действия, включая лечение патологии речи, позволили снизить гиперчувствительность С-волокон к капсаицину, возможно, за счет уменьшая чрезмерный вход от гортани и, следовательно, гиперчувствительность в центральной области.19
разговор или пение вызывают кашель. Это состояние называется гиперкашелью (сенсибилизация к слабым раздражителям) или аллотассивностью (сенсибилизация к банальным раздражителям). Гортанные симптомы и триггеры РХ настолько важны, что некоторые авторы ввели понятие ларингеальной гиперчувствительности при РХ и считают его фундаментальным для клинического понимания состояния; на самом деле, они применяют его к нескольким связанным проблемам, таким как дисфункция голосовых связок, дисфония мышечного напряжения и даже тяжелая астма.18 В исследованиях гиперчувствительности гортани междисциплинарные действия, включая лечение патологии речи, позволили снизить гиперчувствительность С-волокон к капсаицину, возможно, за счет уменьшая чрезмерный вход от гортани и, следовательно, гиперчувствительность в центральной области.19
Таким образом, периферическая и центральная гиперчувствительность могут быть связаны друг с другом сложным образом при возникновении кашля. Первое может быть причиной кашля, второе — следствием; альтернативно, со временем центральная гиперчувствительность может увеличить возбудимость различных периферических терминальных волокон, как в петле обратной связи; (рисунок 1) или оба типа гиперчувствительности могут даже развиваться независимо друг от друга с образованием CC. Действительно, было обнаружено, что пациенты с хроническим идиопатическим кашлем имеют относительно нормальную чувствительность к кашлевым агентам, но у них развивается аллокашель 20, клиническое проявление, присущее центральной гиперчувствительности. Важный вопрос заключается в том, существуют ли люди, особенно женщины в большей степени, чем мужчины,21 с генетической предрасположенностью к развитию центральной сенсибилизации, и способствует ли это (как в случае хронической боли) развитию ЦК, состоянию гиперчувствительности, которое усложняет проблема еще больше, с точки зрения достижения точного диагноза причины кашля и применения соответствующего лечения. Это лечение может быть основано на уменьшении периферического воздействия или на изменении реакции ЦНС либо с помощью лекарств, либо с помощью психологических вмешательств, таких как обучение и тренировка осознанности.18,22,
Действительно, было обнаружено, что пациенты с хроническим идиопатическим кашлем имеют относительно нормальную чувствительность к кашлевым агентам, но у них развивается аллокашель 20, клиническое проявление, присущее центральной гиперчувствительности. Важный вопрос заключается в том, существуют ли люди, особенно женщины в большей степени, чем мужчины,21 с генетической предрасположенностью к развитию центральной сенсибилизации, и способствует ли это (как в случае хронической боли) развитию ЦК, состоянию гиперчувствительности, которое усложняет проблема еще больше, с точки зрения достижения точного диагноза причины кашля и применения соответствующего лечения. Это лечение может быть основано на уменьшении периферического воздействия или на изменении реакции ЦНС либо с помощью лекарств, либо с помощью психологических вмешательств, таких как обучение и тренировка осознанности.18,22,
Рисунок 1
Неврологическая цепь обратной связи хронического кашля.
Ссылки
- ↵
- Chung KF,
- Pavord ID
. Распространенность, патогенез и причины хронического кашля. The Lancet 2008; 371:1364–74.
- ↵
- Вальдшнеп А.,
- Янг ЕС,
- Смит Дж.А.
. Новые взгляды на кашель. Br Med Bull 2010; 96:61–73.
- ↵
- ÓNeill J,
- McMahon SB,
- Undem BJ
. Хронический кашель и боль: лица Януса в сенсорной нейробиологии? Легочная фармакология α Therapeutics 2013;26:476–85.
- ↵
- Morice AH,
- Millqvist E,
- Belvisi MG,
- и др.
. Экспертное мнение о синдроме кашлевой гиперчувствительности в респираторной медицине. EUR Respir J В печати.

- ↵
- Canning BJ,
- Mazzone SB,
- Meeker SN,
- и др.
. Идентификация афферентных нейронов трахеи и гортани, опосредующих кашель, у анестезированных морских свинок. J Physiol 2004;557:543–58.
- ↵
- Coudry NB,
- Fuller RW,
- Pride NB
. Чувствительность кашлевого рефлекса человека: действие медиаторов воспаления простагландина Е2, брадикинина и гистамина. Am Rev Respir Dis 1989; 140: 137–41.
- ↵
- Riccio MM,
- Myers AC,
- Undem BJ
. Иммуномодуляция афферентных нейронов изолированных дыхательных путей морской свинки. J Physiol 1996;491(Pt 2):499–509.
- ↵
- Mazzone SB,
- Mori N,
- Canning BJ
.
 Синергические взаимодействия между подтипами афферентных нервов дыхательных путей, регулирующих кашлевой рефлекс у морских свинок. J Physiol 2005;569:559–73.
Синергические взаимодействия между подтипами афферентных нервов дыхательных путей, регулирующих кашлевой рефлекс у морских свинок. J Physiol 2005;569:559–73. - ↵
- Консервы BJ
. Афферентные нервы, регулирующие кашлевой рефлекс: механизмы и медиаторы кашля при заболеваниях. Otolaryngol Clin North Am 2010; 43:15–25.
- ↵
- Ву Д.Н.,
- Ямаути К.,
- Кобаяши Х.,
- и др.
. Влияние перфузии пищевода кислотой на кашлевую реакцию у больных бронхиальной астмой. Сундук 2002; 122: 505–9.
- ↵
- Яворкова Н.,
- Варехова С.,
- Пекова Р.,
- и др.
. Закисление пищевода резко повышает кашлевую чувствительность у больных с гастроэзофагеальным рефлюксом и хроническим кашлем.
 Нейрогастроэнтерол Мотил 2008;20:119–24.
Нейрогастроэнтерол Мотил 2008;20:119–24. - ↵
- Плевкова Ю.,
- Антосевич Ю.,
- Варехова С.,
- и др.
. Конвергенция носовых и трахеальных нервных путей в модулировании кашлевой реакции у морских свинок. J Physiol Pharmacol 2009;60:89–93.
- ↵
- Пачеко А,
- Фару В,
- Кобета I,
- и др.
. Гастроэзофагеальный рефлюкс, эозинофильное воспаление дыхательных путей и хронический кашель. Респирология 2011;16:994–9.
- ↵
- Сандкюлер Й,
- Грубер-Шоффнеггер D
. Гипералгезия синаптической долгосрочной потенциации (LTP): обновление. Curr Opin Pharmacol 2012; 12:18–27.
- ↵
- Карр М,
- Ундем Б
.
 Воспалительно-индуцированная пластичность афферентной иннервации дыхательных путей. Environ Health Perspect 2001;109(Приложение 4):567–71.
Воспалительно-индуцированная пластичность афферентной иннервации дыхательных путей. Environ Health Perspect 2001;109(Приложение 4):567–71. - ↵
- Раджа С.,
- Кэмпбелл Дж. Н.,
- Мейер Р.А.
. Доказательства различных механизмов первичной и вторичной гипералгезии после повреждения голой кожи сердца. Мозг 1984;107:1179–88.
- ↵
- McMahon SB,
- Malcangio M
. Текущие проблемы в биологии глиальной боли. Нейрон 2009; 64:46–54.
- ↵
- Гибсон П.Г.,
- Симпсон Д.Л.,
- Райан Н.М.,
- и др.
. Механизмы кашля. Curr Opin Allergy Clin Immunol 2014;14:55–61.
- ↵
- Райан Н.М.,
- Вертиган А,
- Боун С,
- и др.

. Чувствительность кашлевого рефлекса улучшается при лечении речевой патологии рефрактерного хронического персистирующего кашля. Кашель 2010;6:5.
- ↵
- Морис А.Х.,
- Фонтана Г.А.,
- Belvisi MG,
- и др.
. Рекомендации ERS по оценке кашля. Eur Respir J 2007; 29:1256–76.
- ↵
- Kelsall A,
- Decalmer S,
- McGuinness K,
- и др.
. Половые различия и предикторы объективной частоты кашля при хроническом кашле. Грудная клетка 2009;64:393–8.
- ↵
- Young EC,
- Brammer C,
- Оуэн Э.,
- и др.
. Влияние медитации осознанности на чувствительность кашлевого рефлекса. Грудная клетка 2009;64:993–8.

