Ингаляции при ангине: небулайзер для детей, ингаляции при гнойной ангине
Можно ли делать ингаляцию при ангине? Этот метод лечения оправдан, поскольку помогает быстрее избавиться от налета и снять воспаление. Применять его следует в составе комплексной терапии, то есть вместе с антибиотиками и полосканиями.
Преимуществом ингаляции является то, что больной может провести процедуру самостоятельно в домашних условиях. Однако без назначения врача прибегать к данному методу не следует.
Способы проведения процедуры
Ингаляции при ангине делают разными методами, самый простой из которых — дышать паром, накрыв голову полотенцем. Заваренные лекарственные растения при этом помещаются в обычную кастрюлю.
Можно использовать и специальный ингалятор при ангине. С ним процедура становится более комфортной.
Небулайзер при ангине
Небулайзер представляет собой специальный аппарат для вдыхания лекарственных средств. Он позволяет делать так называемые влажные ингаляции, которые, в отличие от прочих (паровых, сухих, масляных), абсолютно безопасны.
При ангине можно дышать данным ингалятором при помощи трубки или мундштука. Раствор распыляется непосредственно на очаг инфекции и охватывает все пораженные болезнью участки. Есть несколько видов небулайзеров:
- компрессорный;
- ультразвуковой;
- меш-небулайзер.
Средства для ингаляций
Лучше дышать над свежеприготовленным лечебным средством, поскольку его активные вещества в этом случае будут действовать более эффективно. Ингаляции при тонзиллите можно делать с использованием шалфея, ромашки, зверобоя, мази «Звездочка», а также эфирных масел.
Смягчить боли в горле позволит и простая вода с добавлением соды. Традиционный способ лечения при ангине — дышать над вареной картошкой. Ее варить нужно до тех пор, пока вода не приобретет характерный картофельный запах. Для усиления эффекта можно добавить корицу или пихтовое масло.
Традиционный способ лечения при ангине — дышать над вареной картошкой. Ее варить нужно до тех пор, пока вода не приобретет характерный картофельный запах. Для усиления эффекта можно добавить корицу или пихтовое масло.
При ангине хороший эффект дают ингаляции с луковым соком. Его необходимо развести раствором хлорида натрия в пропорции 1:2.
Для ингаляций с помощью небулайзера следует использовать медикаментозные средства — антибиотики, антисептики, препараты для укрепления иммунитета. Они при этом дают не менее выраженный эффект, чем при традиционных полосканиях. Если лечащий врач назначил определенные препараты из этой группы, проверить наличие лекарств в аптеках Киева можно через наш ресурс.
Ингаляции при гнойной ангине
Обычно именно данная форма заболевания причиняет наибольшее беспокойство. Ингаляции при гнойной ангине в острой форме делать нельзя. Направленный тепловой поток может спровоцировать прорыв гнойного содержимого, которое в результате разнесется по кровотоку.
Лучшее средство от гнойной ангины — это антибиотики, которые воздействуют непосредственно на причину болезни. Они уничтожают патогенные микроорганизмы и предотвращают осложнения.
Хорошо использовать лекарство от гнойной ангины, которое действует местно, но в острый период это могут быть полоскания либо таблетки для рассасывания. Если гнойники прорвались либо их рост остановился, что сопровождается снижением температуры, то ингаляции уже безопасны. И все же лучше проконсультироваться с врачом прежде, чем начинать их применять.
Ингаляции при ангине у детей
Горячий пар маленьким детям противопоказан, так как он может травмировать нежные ткани слизистой оболочки. Лучше всего делать ингаляции при ангине у детей небулайзером.
Растворы с антибиотиками или гормональными средствами при лечении ребенка следует применять осторожно. Можно использовать для ингаляции при ангине небулайзером препараты Ротокан и Тонзилгон-Н, а также календулу, настойку эвкалипта или прополиса. Ингаляции с обычной минеральной водой очень хорошо увлажняют и убирают воспаление.
Ингаляции с обычной минеральной водой очень хорошо увлажняют и убирают воспаление.
Ингаляции небулайзером при ангине у детей до 6 месяцев без контроля специалиста применять нельзя. Для ребенка постарше длительность процедуры не должна превышать 5 минут.
Ингаляционная терапия
Лечение и профилактика заболеваний путем вдыхания искусственно распыляемых лекарственных веществ или воздуха, насыщенного солями, эфирными маслами .
Основными задачами ингаляционной терапии считаются: улучшение дренажной функции дыхательных путей; санация верхних дыхательных путей и бронхиального дерева; уменьшение отека и стимуляция регенерации; снижение активности воспалительного процесса; купирование бронхоспазма; воздействие на местные иммунные реакции респираторного тракта; улучшение микроциркуляции слизистой оболочки дыхательных путей; защита слизистой оболочки от действия производственных аэрозолей и поллютантов.
Наиболее распространенными видами ингаляций являются паровые, тепловлажные, влажные, масляные, воздушные, ультразвуковые и инсуффуляции.
Инсффуляция – или вдыхание сухих лекарственных веществ.
Показаны
при остром и хроническом насморке, гриппе, синуситах, аденоидитах, ангинах, хронических тонзиллитах, острых ларингитах, трахеитах, фарингитах, а так же легочном туберкулезе.Паровые ингаляции являются наиболее доступным видом ингаляции. Их проводят с помощью паровых ингаляторов.
Показаны: при острых и хронических заболеваниях носовой полости, среднего уха, горла, острых и хронических заболеваниях трахеи и бронхов, гриппе и острых респираторных заболеваниях, профессиональных заболеваниях органов дыхания.
Противопоказаны при тяжелых формах туберкулеза, при острой пневмонии, плеврите, кровохрканье, артериальной гипертензии, ишемической болезни сердца, гипертрофии и полипозе слизистых дыхательных путей.
Влажные ингаляции- лекарственное вещество с помощью портативного ингалятора распыляется и вводится в дыхательные пути без предварительного подогрева.
Показания: предупреждение высыхания слизистой оболочки трахеобронхиального дерева в условиях длительной искусственной вентиляции; гигиены дыхательных путей при наличии трахеостомы; предупреждения бронхоспастической реакции, связанной с физической нагрузкой, купирования отека дыхательных путей; симптоматическое лечения заболеваний верхних дыхательных путей.
Тепловлажные ингаляции — вызывают гиперемию слизистой оболочки дыхательных путей, разжижают мокроту и стимулируют мукоцилиарный клиренс, ускоряют эвакуацию слизи, подавляют упорный кашель, улучшают дренирующую функцию бронхов . Показаны при подострых и хронических заболеваниях носа, среднего уха и горла, острых и хронических заболеваниях трахеи и бронхов, абсцессе легкого, пневмосклерозе, бронхиальной астме, гриппе и острых респираторных заболеваниях, профессиональных заболеваниях органов дыхания .
Масляные ингаляции основаны на распылении с профилактическими и лечебными целями подогретых различных масел, которые обладают трофическим, репаративным, регенераторным и бронхопротективным действием.
Масляные ингаляции показаны при остром воспалении слизистых дыхательных путей, при набухании и гипертрофии слизистых оболочек, при неприятных ощущениях сухости в носу или гортани, а также с профилактическими целями.
Противопоказаны при нарушении дренажной функции бронхов и на производствах с большим количеством мелкой пыли.
Воздушные ингаляции проводятся путем распыления находящихся в баллончике лекарственных веществ легко испаряющимся газом (пропеллентом) или сжатым воздухом.
Показаны при подострых и хронических заболеваниях трахеи и бронхов, выраженном отеке, острой пневмонии в стадии реконваленсценции, бронхиальной астме, профессиональных заболеваниях бронхов и легких, при состояниях после операции на легких, сопровождающихся осложнениями нагноительного характера.
Ультразвуковые ингаляции основаны на разбиении жидкости при помощи механических колебаний ультравысокой частоты или ультразвука.
Ультразвуковые ингаляции показаны при абсцессе легкого, пневмосклерозе, пневмонии в фазе реконвалесценции, профессиональных заболеваниях легких.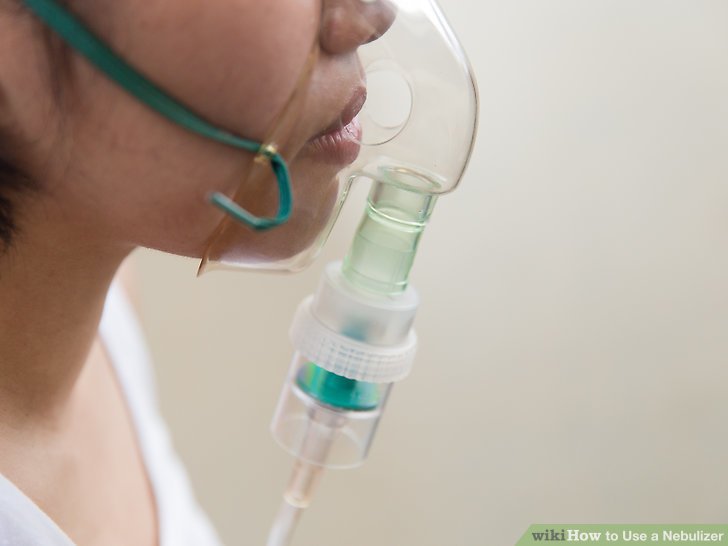
пульмонолог — о лечении COVID-19 оксидом азота и гелием — РТ на русском
Метод лечения тяжелобольных пациентов с COVID-19 ингаляциями гелия и оксида азота может эффективно сочетаться с искусственной вентиляцией лёгких. Об этом в беседе с RT рассказал профессор РНИМУ им. Пирогова, врач-пульмонолог Александр Карабиненко. Специалист частично поддержал высказанное ранее заведующим кафедрой Российского национального исследовательского медицинского университета имени Пирогова, председателем Российского респираторного общества Александром Чучалиным мнение о целесообразности лечения COVID-19 с помощью газовых смесей. Вместе с тем Карабиненко отметил, что этот метод технологически сложный и потребует серьёзных ресурсов, специальной аппаратуры и квалифицированных специалистов. Также врач подчеркнул, что применение гелия и оксида азота имеет ряд противопоказаний.
Ингаляции гелия и оксида азота могут применяться для лечения коронавирусной инфекции нового типа у тяжелобольных пациентов, однако этот метод технологически сложен и имеет противопоказания. Об этом в интервью RT заявил заслуженный врач России, профессор РНИМУ им. Пирогова, врач-пульмонолог Александр Карабиненко.
Об этом в интервью RT заявил заслуженный врач России, профессор РНИМУ им. Пирогова, врач-пульмонолог Александр Карабиненко.
Так он прокомментировал слова академика РАН, директора НИИ пульмонологии ФМБА Александра Чучалина о целесообразности лечения COVID-19 с помощью газовых смесей — гелия и окиси азота. Такую точку зрения Чучалин высказал в ходе онлайн-совещания по противодействию COVID-19, которое провёл президент России Владимир Путин.
- Онлайн-совещание по противодействию COVID-19
- © Sputnik/Alexei Druzhinin/Kremlin via REUTERS
Также академик Чучалин рассказал, что в НИИ им. Склифосовского уже получены положительные результаты лечения пациентов такой смесью — оксид азота улучшает микроциркуляцию крови и предотвращает тромбообразование, а нагретый гелий убивает вирусы.
Также по теме
«Начнём лечить на ранней стадии»: российский диагност — о компьютерной томографии и других методах определения COVID-19
Компьютерная томография становится главным инструментом диагностики COVID-19, так как точность этого метода составляет 97—98%. Об этом…
Об этом…
Для использования газовых смесей разработан российский аппарат «Тианокс», который, по информации специалиста, начнут выпускать серийно по госзаказу.
По словам Александра Карабиненко, лечение газовыми смесями действительно может быть весьма эффективным для тяжелобольных коронавирусной инфекцией, особенно вместе с применением аппаратов искусственной вентиляции лёгких (ИВЛ).
«Оба метода, как ИВЛ, так и лечение гелиевыми смесями с оксидом азота, эффективны при тяжёлой дыхательной недостаточности»,— подтвердил профессор Карабиненко.
Однако, по мнению специалиста, предложенная методика имеет ряд ограничений. «Этот метод лечения известен давно, его активно применяют последние 20 лет. Однако получение таких газовых смесей — дело непростое. Их заказывают заранее, изготавливают на специальных предприятиях», — отметил собеседник RT.
«Нужна особая аппаратура и специалисты, обученные методике. К тому же есть противопоказания. Нельзя просто так дать дышать человеку инертным газом», — объяснил Карабиненко.

Специалист добавил, что быстро обеспечить всю страну оборудованием для таких ингаляций непросто — даже в обычных столичных стационарах его пока нет. По словам пульмонолога, система здравоохранения испытывает повышенную нагрузку, в связи с этим специалист отметил, что обеспечение больниц приборами для ингаляций будет «материально накладно для медицины».
Компания
Но и не только ему: при каждом «акте» чихания или кашля всё пространство вокруг активно «насыщается» вирусами, что способствует дальнейшему распространению заболевания. И тем, кто «героически» переносит ОРВИ и даже грипп на ногах – стоит помнить об этом. Не хотите думать о себе – подумайте хотя бы об окружающих!
Решать эту проблему медикаментозным образом можно с помощью современного препарата Эргоферон. Именно он, обладая противовирусной активностью, борется с самим источником неприятностей. Но, разумеется, возможны и дополнительные методы, способные заметно «облегчить муки» пациента. И одна из таких процедур, не требующих особых условий и усилий – это ингаляция, то есть вдыхание целебных паров.
И одна из таких процедур, не требующих особых условий и усилий – это ингаляция, то есть вдыхание целебных паров.
На самом деле, прогулка в хвойном лесу или вдоль морского берега – это тоже ингаляция, просто «естественного происхождения»! Давно отмечено, что «морские» или «лесные» жители страдают от простуд гораздо реже «городских». Увы, одно лишь желание не перенесет нас в сосновый бор или на побережье – но воссоздать их атмосферу «в миниатюре» вполне возможно и в домашних условиях.
К счастью, Природа позаботилась и об обитателях «каменных джунглей», и перечень весьма полезных растений более чем обширен. При насморке отлично подойдут эвкалипт, пихта, сосна, прополис, календула и мята. При этом «распаривать» всё лицо целиком необязательно: «сбор» можно заварить в чайнике и аккуратно вдыхать через носик.
А кого в детстве бабушка не заставляла «дышать над картошкой» в целях скорейшего устранения кашля? Отличное средство, лучше всего – незадолго до сна, да и «ингредиент» затем можно использовать по прямому «питательному» назначению!
А еще – шалфей, ромашка, «липовый цвет», лаванда, крапива и листья черной смородины. А еще – мед, лук и чеснок. А еще… в общем, обязательно найдется что-то не только полезное, но и приятное «на вкус и цвет» и улучшающее настроение именно вам. И тогда ваши воспаленные слизистые оболочки придут «в порядок» намного быстрее!
А еще – мед, лук и чеснок. А еще… в общем, обязательно найдется что-то не только полезное, но и приятное «на вкус и цвет» и улучшающее настроение именно вам. И тогда ваши воспаленные слизистые оболочки придут «в порядок» намного быстрее!
Важное замечание. При всей полезности ингаляций их нельзя делать при высокой температуре, при воспалении легких и малышам до года. А после процедуры какое-то время не стоит выходить на свежий воздух и вообще охлаждаться. Лучше просто отдохнуть и продолжить свое мысленное пребывание на морском берегу или на цветущем летнем лугу!
Инновационный препарат комплексного действия Эргоферон – это противовирусное средство, способствующее уменьшению всех основных проявлений простуды и гриппа. Препарат может назначаться и детям, начиная с 6-месячного возраста. Еще одно важное его достоинство – препарат сочетается со средствами «народной медицины», используемыми в том числе и для «целебного дыхания».
Ингаляции при кашле
Ингаляции считаются одним из древнейших методов лечения кашля.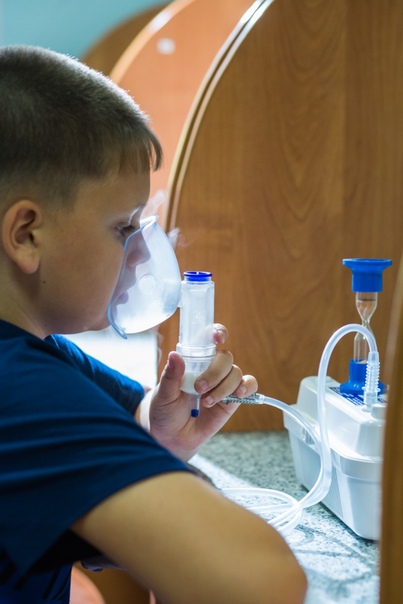 Их легко проводить в домашних условиях, склонившись над широкой кастрюлей и накрыв голову махровым полотенцем.
Их легко проводить в домашних условиях, склонившись над широкой кастрюлей и накрыв голову махровым полотенцем.
Не забывайте! Ингаляции нельзя делать при высокой температуре. К тому же лучше не дышать паром после приема пищи, подождите час-другой и смело приступайте к процедурам. Во время ингаляций надо правильно дышать — вдыхать пар ртом, а выдыхать носом. Слишком долго проводить ингаляцию не стоит – для лечебного эффекта достаточно десяти минут. Также не надо очень низко наклоняться над миской или кастрюлей, чтобы не обжечь лицо. И самое главное, после ингаляции нельзя выходить на улицу или переходить в более прохладное помещение, нельзя курить – эффект от такого «лечения» будет противоположным. Лучше всего сразу же лечь в постель. В день можно делать по 3-6 ингаляций, в зависимости от самочувствия.
Ингаляции помогут смягчить сухой кашель и поспособствовать отхождению мокроты при влажном кашле. Существует множество рецептов для ингаляций, самый распространенный – подышать над свежесваренной картошкой.
При сухом кашле подойдут размягчающие ингаляции с мятой, душицей или ромашкой. Отличным средством станут хвойные ингаляции, лучше всего запарить свежесрезанные молодые веточки ели, а потом подышать над ними. Отличный эффект дает и морская соль, ее можно купить в аптеке. В соляной раствор можно добавить несколько капель эвкалипта или пихтового масла.
Вместо картошки можно разварить репчатый лук и также использовать его в качестве ингаляции. Лук обладает отличными противовоспалительными свойствами.
Для ингаляций широко применяются различные лекарственные травы, их надо немножко проварить, а потом подышать над травяным отваром. Популярными травами считаются шалфей, ромашка, календула, душица.
В аптеке можно купить готовые грудные сборы, которые можно использовать для ингаляций. В грудной сбор входит целый набор целебных трав, размягчающих сухой кашель и разжижающих мокроту при влажном кашле.
В грудной сбор могут входить чабрец, солодка, липа, мята, сосновые почки, календула и другие лекарственные средства, оказывающие прекрасное противомикробное действие. Помните! Травяные сборы надо с осторожностью применять при наличии аллергии, поэтому лучше всего предварительно посоветоваться с врачом. При беременности также необходимо проконсультироваться у врача, так как некоторые травы беременным противопоказаны.
Помните! Травяные сборы надо с осторожностью применять при наличии аллергии, поэтому лучше всего предварительно посоветоваться с врачом. При беременности также необходимо проконсультироваться у врача, так как некоторые травы беременным противопоказаны.
Если после ингаляций не происходит улучшения, надо обратиться к врачу, возможно кашель вызван более серьезным заболеванием, чем обычная простуда и одними травами тут не обойтись. Главное, не заниматься самолечением длительное время, чтобы не вызвать серьезных осложнений.
Читайте также:
Кашель
Сухой кашель
Средство от кашля
Сильный кашель
Как лечить кашель
Народное лечение кашля
Кашель с температурой
Кашель без температуры
Кашель при беременности
Насморк и кашель
Ингаляции при кашле
Мокрый кашель
Кашель с мокротой
Если не проходит кашель
Причины кашля
Лающий кашель
Боли в теле при кашле
Кашель после операции
Аллергический кашель
Виды кашля
Таблетки от кашля
Отхаркивающий кашель
Антибиотики при кашле
Лечение сухого кашля
Сухое горло и кашель
Боли в горле при сильном кашле
Как лечить сильный кашель
Как лечить аллергический кашель
Клиника лечения кашля
Куда обращаться при кашле
Противопоказания при кашле
Горчичники при кашле
Небулайзер при кашле
Кровь при кашле
Кашель с кровью, причины
Хронический кашель, причины
Лечение хронического кашля
Тяжело дышать
Почему тяжело дышать
Не хватает воздуха
Тяжело стало дышать
Тяжело дышать, причины
Ночью тяжело дышать
БЕЗДОКАЗАТЕЛЬНО: Лидокаин эффективен в лечении COVID-19
Проверка фейков в рамках партнерства с Facebook
В сети распространяют информацию о том, что лидокаин эффективен в лечении COVID-19. В этом видео человек, которого называют врачом-терапевтом по фамилии Узденов, рассказывает о «лучшем способе лечения больных за 2 дня». При этом он ссылается не на научные исследования, а собственный опыт.
В этом видео человек, которого называют врачом-терапевтом по фамилии Узденов, рассказывает о «лучшем способе лечения больных за 2 дня». При этом он ссылается не на научные исследования, а собственный опыт.
Со слов мужчины, он самостоятельно провел опыт. Группе из 17 больных COVID-19 он назначил ингаляции с лидокаином: раствор 2% лидокаина разбавленный 0,9% хлорида натрия. Другая группа из 5 человек получала «стандартное лечение согласно клиническим рекомендациям». По словам Узденова, на вторые сутки 12 пациентов уже полностью выздоровели. А те, кто лечился по стандартному протоколу, в течение 3 дней не имели положительной динамики.
Однако опыт, самостоятельно проведен Узденовым, не может считаться показательным научным исследованиям, результаты которого можно применять массово. Это «исследование» не было опубликовано ни в одном научном издании и не прошло независимого научного оценивания (рецензирования). К тому же, если этот опыт был проведен одним человеком, невозможно говорить об объективности и беспристрастности результатов.
Свое предположение об эффективности лидокаина Узденов решил проверить на пациентах без научных подтверждений действенности такого метода. На видео он предполагает, что ряд лекарственных средств, которые якобы показали эффективность в лечении COVID-19, не имеют ничего общего, кроме того, что их вводят вместе с лидокаином. Поэтому Узденов предполагает, что дело вроде бы именно в лидокаине.
Однако эффективность препаратов, о которых говорит Узденов, никогда не была доказана. Например, VoxCheck уже неоднократно писал о том, что не существует доказательств действенности гидроксихлорохина. Узденов также называет эффективным комбинированный препарат от ВИЧ лопинавир-ритонавир. Тогда как несколько клинических исследований опровергли это утверждение (например, это и это), а ВОЗ даже остановила исследования этого препарата из-за нехватки доказательств его эффективности.
По поводу лидокаина, то существуют предположения эффективности лидокаинових ингаляций при лечении COVID-19 (это и это). Однако клинические исследования никогда не проводились, поэтому утверждать об эффективности лидокаина пока нет оснований.
Однако клинические исследования никогда не проводились, поэтому утверждать об эффективности лидокаина пока нет оснований.
Что такое физраствор? Польза физиологического раствора при ингаляциях
У большинства людей такой препарат, как физиологический раствор, ассоциируется исключительно лишь с капельницей или внутримышечной инъекцией. Это неудивительно, так как чаще всего многие сталкиваются с ним именно после операции или во время болезни. Но польза и область применения физраствора этим не ограничиваются.
Для начала стоит разобраться, что такое физраствор и почему он вообще так называется. Физиологический раствор – это не что иное, как раствор обычной поваренной соли. В аптеке чаще всего продается именно 0,9-процентный раствор хлорида натрия (той самой соли). Отсюда возникает вопрос: раз это простая соль, которая есть дома у каждого человека, значит можно приготовить физиологический раствор самому? Конечно, можно: для этого десять грамм соли следует развести в одном литре кипяченой воды, довести до кипения и остудить. Но полученный таким способом раствор можно хранить в холодильнике не более суток – ведь приготовлен он не в стерильных условиях. Да и объем на выходе достаточно большой, что не всегда необходимо. Поэтому проще и безопаснее приобрести такой раствор в аптеке – тем более, что стоит он «копейки». Выпускается физраствор как в ампулах (по пять, десять, двадцать миллилитров), так и во флаконах (по сто, двести, четыреста и тысячи миллилитров).
Но полученный таким способом раствор можно хранить в холодильнике не более суток – ведь приготовлен он не в стерильных условиях. Да и объем на выходе достаточно большой, что не всегда необходимо. Поэтому проще и безопаснее приобрести такой раствор в аптеке – тем более, что стоит он «копейки». Выпускается физраствор как в ампулах (по пять, десять, двадцать миллилитров), так и во флаконах (по сто, двести, четыреста и тысячи миллилитров).
Называется данный раствор физиологическим потому, что по своему составу, то есть концентрации в нем поваренной соли, почти соответствует ее же концентрации в плазме крови человека. Таким образом, этот раствор физиологичен, то есть естественен для человеческого организма. Именно по этой причине его вводят после операций, а также разбавляют им многие лекарства.
Но у физраствора есть еще очень полезная функция, о которой и пойдет дальше речь.
Он применяется для ингаляций в борьбе с заболеваниями дыхательных путей. Чтобы такие ингаляции были эффективны, необходимо приобрести небулайзер — специальный прибор, с помощью которого раствор распыляется на более мелкие частицы и позволяет проникнуть им глубже в дыхательные пути (что позволяет достичь быстрого результата).
Чтобы такие ингаляции были эффективны, необходимо приобрести небулайзер — специальный прибор, с помощью которого раствор распыляется на более мелкие частицы и позволяет проникнуть им глубже в дыхательные пути (что позволяет достичь быстрого результата).
Стоит также обратить внимание, что обычные паровые процедуры и использованием физраствора не имеют никакого смысла: при кипении раствора образуется водяной пар, а полезная соль превращается в осадок.
Польза именно физиологического раствора при ингаляциях обусловлена, во-первых, его способностью увлажнять – что облегчает отхождение мокроты при кашле. Во-вторых, входящая в его состав соль способна уничтожать болезнетворные бактерии и является естественным антисептиком. Кроме того, физраствор не способен вызвать аллергию, поэтому особенно часто используется для ингаляций детям.
К физиологическому раствору можно также добавлять другие лекарственные средства для усиления эффекта лечения, но только согласно назначениям врача! Даже к безобидным, на первый взгляд, эфирным маслам следует относиться с осторожностью, так они при распылении в дыхательные пути образуют масляную пленку, которая препятствует отхождению мокроты и последующему выздоровлению.
Для самой процедуры ингаляции требуется около трех-четырех миллилитров физраствора (плюс лекарство, если таковое назначил доктор). Раствор заливается в специальную емкость небулайзера согласно инструкции по пользованию прибором. Ингаляция заключается во вдыхании пара через трубку небулайзера. Длительность процедуры зависит от возраста: детям по 1-2 минуты не больше двух раз в день, взрослым – по 4-5 минут три раза в день.
Продолжительность общего курса лечения такими ингаляциями определяется в зависимости от улучшения состояния. Но так как вреда данная процедура точно принести не может (при соблюдении выше описанных рекомендаций), ингаляции физраствором можно продолжать до достижения необходимого результата.
Вдыхание дыма
Обзор вдыхания дыма
Причина номер один смерти, связанная с пожарами, — это вдыхание дыма.
Вдыхание дыма происходит при вдыхании продуктов сгорания во время пожара. Возгорание происходит в результате быстрого разложения вещества под действием тепла (чаще называемого горением). Дым — это смесь нагретых частиц и газов. Невозможно предсказать точный состав дыма от пожара. Сжигаемые продукты, температура огня и количество кислорода, доступного для огня, — все это влияет на тип производимого дыма.
Дым — это смесь нагретых частиц и газов. Невозможно предсказать точный состав дыма от пожара. Сжигаемые продукты, температура огня и количество кислорода, доступного для огня, — все это влияет на тип производимого дыма.
Причины вдыхания дыма
Вдыхание дыма наносит вред организму в результате простого удушья (недостатка кислорода), химического или термического раздражения, химического удушья или их комбинации.
Простые удушающие вещества
- Горение может привести к израсходованию кислорода возле огня и смерти, когда кислорода не осталось для дыхания
- Сам по себе дым может содержать продукты, которые не причиняют вам прямого вреда, но которые поглощают пространство, необходимое для кислорода.Так действует, например, углекислый газ.
Раздражающие соединения
Горение может привести к образованию химикатов, которые могут вызвать прямые травмы при контакте с вашей кожей и слизистыми оболочками. Эти вещества нарушают нормальную работу дыхательных путей. Это нарушение может потенциально вызвать отек, коллапс дыхательных путей и респираторный дистресс. Примеры химических раздражителей, обнаруженных в дыме, включают диоксид серы, аммиак, хлористый водород и хлор.
Это нарушение может потенциально вызвать отек, коллапс дыхательных путей и респираторный дистресс. Примеры химических раздражителей, обнаруженных в дыме, включают диоксид серы, аммиак, хлористый водород и хлор.
Кроме того, высокая температура дыма может вызвать термическое повреждение дыхательных путей.
Химические вещества, удушающие
В результате пожара могут образовываться соединения, которые наносят ущерб, нарушая потребление кислорода вашим телом на клеточном уровне. Окись углерода, цианистый водород и сероводород — все это примеры химических веществ, образующихся при пожарах, которые мешают использованию кислорода клеткой.
Если подача кислорода или его использование запрещены, клетки погибнут.Установлено, что угарный газ является основной причиной смерти при вдыхании дыма.
Симптомы отравления дымом
Могут развиться многочисленные признаки и симптомы отравления дымом. Симптомы могут включать кашель, одышку, охриплость голоса, головную боль и резкие изменения психического статуса.
Такие признаки, как сажа в дыхательных путях или изменение цвета кожи, могут быть полезны для определения степени травмы.
- Кашель: Когда слизистые оболочки дыхательных путей раздражаются, они выделяют больше слизи.Бронхоспазм и увеличение слизи приводят к рефлекторному кашлю. Слизь может быть прозрачной или черной в зависимости от степени отложения сожженных частиц в легких и трахее.
- Одышка: Это может быть вызвано прямым повреждением дыхательных путей, приводящим к снижению поступления кислорода в кровь. Сама кровь могла иметь пониженную способность переносить кислород. Это может быть результатом химикатов в дыме или неспособности клеток использовать кислород.
Это может привести к учащенному дыханию в результате попытки компенсировать эти травмы.
- Охриплость или шумное дыхание: Это может быть признаком скопления жидкости в верхних дыхательных путях, где они могут вызвать закупорку. Кроме того, химические вещества могут раздражать голосовые связки, вызывая спазм, отек и сужение верхних дыхательных путей.

- Глаза: Глаза могут покраснеть и появиться раздражение от дыма. На роговице также могут быть ожоги.
- Цвет кожи : Цвет кожи может варьироваться от бледного до голубоватого до вишнево-красного.
- Сажа: Сажа в ноздрях или горле может указывать на степень вдыхания дыма. Вдыхание может вызвать отек ноздрей и носовых ходов.
- Головная боль: При всех пожарах люди подвергаются воздействию различных количеств окиси углерода. Даже при отсутствии респираторных проблем окись углерода все равно может быть вдохнута. Головная боль, тошнота и рвота — все это симптомы отравления угарным газом.
- Изменения психического статуса: Химические удушающие средства и низкий уровень кислорода могут привести к изменениям психического статуса.Путаница, обмороки, судороги и кома — все это потенциальные осложнения после вдыхания дыма.
Когда обращаться за медицинской помощью
Каждый, кто пострадал от отравления дымом, должен пройти проверку «A. B.C’s». Это дыхательные пути, дыхание и кровообращение. Позвоните своему врачу или обратитесь в местное отделение неотложной помощи за советом. Если у вас нет признаков или симптомов, может быть рекомендовано домашнее наблюдение.
B.C’s». Это дыхательные пути, дыхание и кровообращение. Позвоните своему врачу или обратитесь в местное отделение неотложной помощи за советом. Если у вас нет признаков или симптомов, может быть рекомендовано домашнее наблюдение.
Позвоните 911, если вы испытываете следующие симптомы отравления дымом:
- Хриплый голос
- Затрудненное дыхание
- Затяжные приступы кашля
- Психическое замешательство
У кого-то при вдыхании дыма может быстро ухудшиться состояние.Если бы такого человека перевозили на частном автомобиле, по дороге могли бы произойти серьезные травмы или смерть, которых можно было бы избежать, если бы этого человека доставили службы экстренной медицинской помощи.
Экзамены и тесты
Можно выполнить ряд тестов и процедур. Какие тесты зависят от серьезности признаков и симптомов.
- Рентген грудной клетки: Респираторные жалобы, такие как постоянный кашель и одышка, указывают на необходимость рентгенографии грудной клетки.
 Первоначальный рентген может быть нормальным, несмотря на значительные признаки и симптомы. Во время периода наблюдения может потребоваться повторный рентген, чтобы определить, есть ли отсроченное повреждение легких.
Первоначальный рентген может быть нормальным, несмотря на значительные признаки и симптомы. Во время периода наблюдения может потребоваться повторный рентген, чтобы определить, есть ли отсроченное повреждение легких. - Пульсоксиметрия: Световой датчик обычно прикрепляется к пальцу, пальцу ноги или мочке уха для определения уровня кислорода в крови человека. Пульсоксиметрия имеет ограничения. Например, низкое кровяное давление может сделать его неточным, если недостаточно крови поступает к частям тела, к которым прикреплен зонд.
- Анализы крови
- Общий анализ крови : Этот тест определяет, достаточно ли эритроцитов для переноса кислорода, достаточно ли лейкоцитов для борьбы с инфекцией и достаточно тромбоцитов для обеспечения свертывания крови.
- Химический состав (также называемый основным метаболическим профилем) : Можно контролировать электролиты сыворотки (натрий, калий и хлорид). Также контролируются функциональные тесты почек (почек) (креатинин и азот мочевины крови).

- Газ артериальной крови : Для людей со значительным респираторным дистресс-синдромом, острыми изменениями психического статуса или шоком можно получить газ артериальной крови.Этот тест показывает pH крови и может помочь врачу определить степень нехватки кислорода.
- Уровни карбоксигемоглобина и метгемоглобина : Этот уровень должен быть получен у всех жертв вдыхания дыма с респираторной недостаточностью, измененным психическим статусом, низким кровяным давлением, судорогами, обмороком и изменениями pH крови. В настоящее время во многих больницах это обычно делается при оценке газов артериальной крови.
Средство от вдыхания дыма
Самостоятельный уход на дому
Уберите человека с отравленным дымом с места происшествия в место с чистым воздухом.
Убедитесь, что вы не подвергаете себя опасности, прежде чем пытаться вытащить кого-нибудь из задымленного помещения. Если вы серьезно рискуете, чтобы помочь человеку, дождитесь прибытия квалифицированных специалистов на место происшествия./boy-with-inhalation-mask-663759243-5980c21bd963ac00114f8bbe.jpg)
При необходимости, обученные прохожие должны начать СЛР до прибытия неотложной медицинской помощи.
Медицинская помощь
При вдыхании дыма может проводиться ряд процедур.
- Кислород: Кислород — это основа лечения.Его можно наносить с помощью носовой трубки или маски или через трубку, помещенную в горло. Если есть признаки проблем с верхними дыхательными путями, например охриплость голоса, человеку может потребоваться интубация. Для этого врач помещает трубку в горло человека, чтобы дыхательные пути не закрывались из-за отека. Если есть респираторный дистресс или изменения психического статуса, человека могут интубировать, чтобы позволить персоналу помочь с дыханием, отсосать слизь и не дать человеку вдохнуть содержимое собственного желудка.
- Бронхоскопия: Бронхоскопия — это процедура, выполняемая для оценки степени повреждения дыхательных путей с помощью небольшого прицела и для отсасывания секрета и инородных тел. Обычно это делается через эндотрахеальную трубку (тонкую трубку с прикрепленной камерой) после того, как пациенту дали успокоительное и болеутоляющее.
 Процедура может потребоваться, если наблюдается нарастание дыхательной недостаточности, отсутствие клинического улучшения или при коллапсе сегмента легкого.
Процедура может потребоваться, если наблюдается нарастание дыхательной недостаточности, отсутствие клинического улучшения или при коллапсе сегмента легкого. - Гипербарическая оксигенация (HBO): Если человек отравлен угарным газом, можно рассмотреть возможность гипербарической оксигенации.Гипербарическая оксигенация — это лечение, при котором человеку дают кислород в камере сжатия. Некоторые исследования показали, что гипербарическая оксигенация снижает симптомы нервной системы. В случае отравления угарным газом он может ускорить выздоровление. Показания и доступность этого лечения различаются в зависимости от учреждения и региона, в котором человек госпитализирован.
Дальнейшие действия
Последующее наблюдение
После выписки пациента из больницы обычно назначается последующее наблюдение.Если состояние ухудшается или не улучшается так, как ожидалось, после выписки, человек должен немедленно вернуться в отделение неотложной помощи.
Могут быть прописаны лекарства, такие как ингаляторы и обезболивающие. При минимальных усилиях может сохраняться одышка. Для полного заживления легких может потребоваться время, и у некоторых людей могут быть рубцы и одышка на всю оставшуюся жизнь. Важно избегать таких провоцирующих факторов, как сигаретный дым.
Стойкая охриплость может возникнуть у людей, получивших ожоги, травмы от вдыхания дыма или и то, и другое. Своевременное внимание к этим проблемам, многие из которых поддаются хирургическому, поведенческому или и тому, и другому лечению, может привести к улучшению голоса.
Профилактика
Профилактика является ключевым моментом при обсуждении вдыхания дыма. Чтобы избежать воздействия дыма, можно использовать многочисленные стратегии профилактики.
- Детекторы дыма следует размещать в каждой комнате жилого здания.Это должно обеспечить раннее обнаружение дыма и время для эвакуации.
- Детекторы окиси углерода следует размещать в местах, подверженных риску воздействия окиси углерода (например, возле печей или гаражей).

- Пути эвакуации и планы эвакуации должны быть разработаны до возникновения пожара и периодически пересматриваться.
- Номера полиции, пожарной части и местного токсикологического центра следует хранить на видном месте на случай чрезвычайной ситуации. Найдите токсикологический центр прямо сейчас, проверив веб-сайт Американской ассоциации токсикологических центров.
Мультимедиа
Медиа-файл 1: Пострадавший от вдыхания дыма. Обратите внимание на сажу в ноздрях и степень отечности лица. По прибытии его голос был хриплым. Ему была проведена эндотрахеальная интубация (трубка была помещена в их дыхательные пути, чтобы помочь ему дышать) из-за опасений по поводу значительного отека дыхательных путей (опухоли) и возможности обструкции дыхательных путей.
Тип носителя: Фотография
Медиа-файл 2: Современная гипербарическая кислородная камера от HyperTec.
Тип носителя: Фотография
Медиа-файл 3: Современная камера для одного человека от HyperTec.
Тип носителя: Фотография
Вдыхание инородного тела у взрослого населения: опыт 25 998 бронхоскопий и систематический обзор литературы
Реферат
ИСТОРИЯ: Вдыхание инородного тела у взрослых — редкость. Здесь мы описываем наш опыт гибкой бронхоскопии при удалении трахеобронхиальных инородных тел у взрослых.Мы также провели систематический обзор литературы по теме вдыхания инородных тел у взрослых, которым проводилась гибкая бронхоскопия.
МЕТОДЫ: База данных бронхоскопии (с 1979 по 2014 год) была проанализирована для пациентов старше 12 лет, у которых в анамнезе была аспирация инородного тела, управляемая с помощью гибкой бронхоскопии. Были собраны и проанализированы демографические, клинические данные и данные бронхоскопии. PubMed был рассмотрен на предмет исследований, описывающих использование гибкой бронхоскопии для извлечения инородного тела у взрослых.
РЕЗУЛЬТАТЫ: За период исследования было выполнено 25 998 гибких бронхоскопий. Из них 65 человек (средний возраст 32,8 года, 49 мужчин) были идентифицированы, которым была сделана бронхоскопия по поводу аспирации инородного тела. Неизлечимая пневмония (30,6%), прямая визуализация инородного тела (24,6%) и сегментарный коллапс (18,4%) были наиболее частыми радиологическими аномалиями. Инородные тела при бронхоскопии были выявлены в 49 случаях и успешно удалены в 45 (91.8%) субъектов без серьезных осложнений. Чаще всего встречались металлические (41%) и органические (25,6%) инородные тела. Зуб акулы (44,9%) и аллигатор (32,6%) были наиболее часто используемыми щипцами для извлечения инородных тел. В систематический обзор было включено 18 исследований (1554 пациента с вдыханием инородных тел). У взрослых доля гибкой бронхоскопии (6 исследований, 354/159 074 процедуры), выполненных для выявления инородных тел среди всех гибких бронхоскопий, составила 0,24% (95% ДИ 0.18–0,31). Общий успех гибкой бронхоскопии (18 исследований, 1185 субъектов) для удаления инородного тела составил 89,6% (95% ДИ 86,1–93,2).
Из них 65 человек (средний возраст 32,8 года, 49 мужчин) были идентифицированы, которым была сделана бронхоскопия по поводу аспирации инородного тела. Неизлечимая пневмония (30,6%), прямая визуализация инородного тела (24,6%) и сегментарный коллапс (18,4%) были наиболее частыми радиологическими аномалиями. Инородные тела при бронхоскопии были выявлены в 49 случаях и успешно удалены в 45 (91.8%) субъектов без серьезных осложнений. Чаще всего встречались металлические (41%) и органические (25,6%) инородные тела. Зуб акулы (44,9%) и аллигатор (32,6%) были наиболее часто используемыми щипцами для извлечения инородных тел. В систематический обзор было включено 18 исследований (1554 пациента с вдыханием инородных тел). У взрослых доля гибкой бронхоскопии (6 исследований, 354/159 074 процедуры), выполненных для выявления инородных тел среди всех гибких бронхоскопий, составила 0,24% (95% ДИ 0.18–0,31). Общий успех гибкой бронхоскопии (18 исследований, 1185 субъектов) для удаления инородного тела составил 89,6% (95% ДИ 86,1–93,2).
ВЫВОДЫ: Аспирация инородного тела — редкое показание для гибкой бронхоскопии у взрослых. Гибкая бронхоскопия имеет высокий уровень успешности при удалении вдыхаемого инородного тела и может считаться предпочтительной начальной процедурой для лечения инородных тел в дыхательных путях у взрослых.
Введение
Аспирация инородного тела — необычное клиническое явление у взрослых. 1 На детей приходится подавляющее большинство всех заявленных стремлений к инородному телу. 2 Инородные тела могут быть органическими (например, арахис, горох) или неорганическими (например, пластиковые колпачки, булавки, винты, гвозди, зубы). Клинически пациенты могут иметь острую дыхательную недостаточность, требующую срочного вмешательства, или недавнее появление респираторных симптомов, включая одышку, хрипы, кашель и отхаркивание. 1,3,4 Выявление аспирации инородного тела требует высокого показателя клинической подозрительности, особенно у тех, кто поступает без аспирации в анамнезе.Иногда забытое инородное тело может быть обнаружено на рентгенограмме грудной клетки, полученной по несвязанным причинам, или во время бронхоскопии.
Радиологические проявления аспирации инородного тела включают либо прямую визуализацию инородного тела в случае рентгеноконтрастных инородных тел, либо косвенные признаки (представляющие обструкцию дыхательных путей) в виде неразрешимой пневмонии, ателектаза, односторонней гиперинфляции или локализованных бронхоэктазов, особенно при с органическими инородными телами. 4,5 Во время бронхоскопии можно непосредственно визуализировать инородное тело или могут присутствовать грануляционная ткань, эндобронхиальный стеноз или отек — все признаки реакции ткани на аспирированное инородное тело. 3,6 У детей жесткая бронхоскопия является предпочтительной процедурой для удаления инородного тела из-за ее способности защищать дыхательные пути, тогда как у взрослых гибкая бронхоскопия может использоваться как для подтверждения диагноза, так и для удаления инородного тела. 7–9 Кроме того, у детей инородные тела оседают в проксимальном трахеобронхиальном дереве, к которому можно легко получить доступ с помощью жесткого бронхоскопа, но у взрослых инородные тела оседают в дистальном трахеобронхиальном дереве. 3,10–12
Большая часть опубликованной литературы по аспирации инородных тел у взрослых представлена в форме отчетов о случаях, и имеется лишь несколько серий случаев. 4,13,14 Здесь мы сообщаем о нашем более чем 35-летнем опыте использования гибкой бронхоскопии для удаления инородных тел у взрослых в центре третичной медицинской помощи. Также был проведен систематический обзор литературы по извлечению инородного тела с помощью гибкой бронхоскопии у взрослого населения.
БЫСТРЫЙ ВЗГЛЯД
Текущие знания
Аспирация инородного тела — необычная клиническая находка у взрослых.На детей приходится подавляющее большинство всех заявленных стремлений к инородному телу. Жесткая бронхоскопия — стандартная практика у педиатрических пациентов. Сообщалось о жестких и гибких бронхоскопиях для удаления инородных тел у взрослых.
Чем эта статья пополняет наши знания
Аспирация инородного тела была редким показанием для гибкой волоконно-оптической бронхоскопии у взрослых. Гибкая бронхоскопия показала высокий уровень успешности при удалении вдыхаемых инородных тел и может считаться предпочтительной начальной процедурой для диагностики и удаления инородных тел из дыхательных путей у взрослых.
Методы
Это был ретроспективный анализ всех гибких бронхоскопий, выполненных с сентября 1979 года по апрель 2014 года в Институте последипломного медицинского образования и исследований в Чандигархе, Индия. Протокол исследования был одобрен комитетом по этике. Письменное информированное согласие было получено от всех субъектов, участвовавших в этом исследовании. В базе данных бронхоскопии (Отделение легочной медицины, Институт последипломного медицинского образования и исследований) был проведен поиск по удалению инородного тела как показания к бронхоскопии у взрослого населения (старше 12 лет).Для каждого субъекта были извлечены следующие данные: демографический профиль, симптомы, рентгенологические данные, результаты бронхоскопии, а также тип, природа и расположение инородного тела. Тип инородного тела классифицировался как органический, металлический, зубной, пластиковый или таблеточный. Также регистрировались ведение (амбулаторное или стационарное), тип щипцов, используемых для извлечения инородного тела, результат процедуры (успех или неудача) и осложнения, возникшие во время процедуры.
Гибкая бронхоскопия (бронхоскоп BF-P20, BF-1T20, BF-1T150 или BF-XT40 с наружным диаметром от 4.9–6,2 мм, Olympus, Токио, Япония) проводилась в кабинете для бронхоскопии или иногда у постели больного пациентам, госпитализированным в больницу. Прикроватная бронхоскопия проводилась у пациентов, которым была выполнена вентиляция легких и которым была выполнена аспирация инородного тела. Процедура проводилась либо консультантом, либо научным сотрудником под непосредственным руководством консультанта. Гибкая бронхоскопия выполнялась перорально пациентам, находящимся в положении лежа на спине, с подозрением на аспирирование инородного тела. Все пациенты получали лидокаин в небулайзере (4% раствор) непосредственно перед процедурой.Актуальный спрей с 10% лидокаином использовался непосредственно перед процедурой, при необходимости добавляя 2% лидокаина через голосовые связки и во время бронхоскопии. Во время или до бронхоскопии седативный эффект не применялся. Во время процедуры контролировались показатели жизнедеятельности (частота пульса, частота дыхания, артериальное давление, Sp O2 ). Пациенты были выписаны в тот же день через 2–3 часа наблюдения.
Было проведено систематическое обследование дыхательных путей, и как только инородное тело было обнаружено, его зафиксировали подходящими щипцами, которые затем извлекли до кончика бронхоскопа.После того, как был обеспечен надежный захват, весь узел (щипцы с зажатым инородным телом и гибкий бронхоскоп) был удален как единое целое. В случае острых предметов инородное тело удерживали острым краем, обращенным к щипцам, чтобы избежать повреждения слизистой оболочки дыхательных путей или голосовых связок.
Systematic Review
В PubMed был произведен поиск исследований, написанных на английском языке с участием субъектов старше 12 лет, с использованием терминов «аспирация инородного тела», «вдыхание инородного тела», «инородное тело в легком», «инородное тело в эндобронхиальном теле», «инородное тело в дыхательных путях», «инородное тело в трахеобронхиальном теле».Кроме того, мы просмотрели наши личные файлы. Обзоры, отчеты о случаях, исследования с участием <10 субъектов и данные, представленные только в виде резюме, были исключены.
Первоначальный обзор исследований.
База данных, созданная таким образом в результате электронного поиска, была включена в пакет менеджера ссылок Endnote X7 (Thomson-Reuters, Нью-Йорк, Нью-Йорк), и все повторяющиеся цитаты были отброшены. Два автора (ISS и RA) проверили эти цитаты, проанализировав названия и аннотации, чтобы определить соответствующие исследования.Любые разногласия разрешались путем обсуждения между авторами. Затем база данных была тщательно изучена, чтобы включить только те исследования, которые описывают не менее 10 субъектов с аспирированными инородными телами, которым проводилась гибкая бронхоскопия. Был получен и детально проанализирован полный текст каждого из этих исследований. В форму для извлечения данных записывались следующие элементы: (1) сведения о публикации (авторы, год и другие сведения о цитировании), (2) тип исследования (проспективное или ретроспективное), (3) количество субъектов, (4) тип использованных щипцов, (5) характер и расположение извлеченного инородного тела, (6) степень успешности удаления инородного тела с помощью гибкой бронхоскопии и (7) осложнения, связанные с процедурой.
Мета-анализ.
Для проведения статистического анализа использовался пакет статистических программ StatsDirect 2.7.8 (StatsDirect, Чешир, Великобритания) и Open MetaAnalyst 5.26.14 15 . Метаанализ был проведен для (1) распространенности гибкой бронхоскопии, выполняемой для выявления инородных тел у взрослых среди тотальных гибких бронхоскопий, и (2) успеха гибкой бронхоскопии при извлечении инородного тела. Пропорция (вариант Фримена-Тьюки для пропорции, преобразованной в квадратный корень арксинуса) с 95% доверительным интервалом была рассчитана для каждого исследования, и данные были объединены с использованием модели случайных эффектов для получения объединенной доли с 95% доверительным интервалом. 16–18 Неоднородность оценивалась с помощью теста I 2 со значением> 50%, указывающим на значительную неоднородность. 19 Систематическая ошибка публикации была оценена с использованием воронкообразного графика 20 и 3 статистических методов (тест Эггера, 21 , тест Харборда, 22 и тест Бегга-Мазумдара 23 ).
Результаты
Всего за период исследования было выполнено 25 998 гибких бронхоскопий. Шестьдесят пять (0,25%) пациентов прошли гибкую бронхоскопию по поводу клинического подозрения на вдыхание инородного тела.Средний возраст (± стандартное отклонение) этих 65 человек составил 32,8 ± 17,9 года; 49 (75,3%) были мужчинами. Из них 60 субъектов вспомнили, что вдыхали инородное тело, а 5 субъектов имели ненормальные рентгенограммы грудной клетки с инородным телом, обнаруженным во время бронхоскопической оценки. Время до презентации было <7 дней у 16 субъектов, а у остальных субъектов прошло> 7 дней после аспирации. У одного пациента была проведена прикроватная гибкая бронхоскопия для удаления инородного тела. Субъект получил травму головы и аспирировал зуб во время интубации (аспирационная пневмония).Через эндотрахеальную трубку был введен гибкий бронхоскоп, и зуб был идентифицирован в правом промежуточном бронхе. Использовались щипцы с зубьями акулы, и щипцы, зуб и гибкий бронхоскоп были удалены вместе, как единое целое. Рентгенологические (рентгенограмма грудной клетки или компьютерная томография грудной клетки) отклонения наблюдались у большинства пациентов (56/65, 86,2%) при обращении, включая в основном неразрешенные помутнения, сегментарный ателектаз / долевой коллапс, бронхоэктазы или гиперинфляцию (Таблица 1).Рентгенограмма грудной клетки была диагностической у 16 (24,6%) из этих 65 субъектов (булавки [ n = 4], зубы [ n = 5], колпачки для ручек [ n = 3], кнопки [ n = 1] ], гвозди [ n = 1] и винты [ n = 2]), тогда как у 9 пациентов это было нормально.
Таблица 1.Демографический профиль, радиология, местоположение и тип инородного тела, обнаруженного во время бронхоскопии, выполненной у субъектов с историей вдыхания инородных тел
Во время бронхоскопии инородное тело было обнаружено у 49 (75.3%) предметы. Информация о типе инородного тела была доступна для 39 субъектов, тогда как эта информация не была записана для 10 субъектов. У 16 (25%) субъектов не удалось идентифицировать инородное тело (эти субъекты были исключены из анализа, и их данные использовались только для расчета аспирации инородного тела в качестве показания для выполнения гибкой бронхоскопии). Металлические инородные тела были наиболее распространенным типом, за ними следовали органические. Обнаруженные металлические инородные тела: штифты ( n = 7), свистки ( n = 5), винты ( n = 2), пружины ( n = 1) и гвозди ( n = 1).Органические инородные тела включали: орехи бетель ( n = 2), арахис ( n = 1), горох ( n = 1), ватные палочки ( n = 1), семена чечевицы ( n ). = 2), рис ( n = 1), луковицы чеснока ( n = 1) и палочки корицы ( n = 1). Пластиковые предметы были обнаружены у 4 человек (колпачки для ручек [ n = 3] и кнопки [ n = 1]), а зубы были обнаружены у 8 человек. Один субъект аспирировал таблетку, что было связано с окружающим отеком и гиперемией.Во время гибкой бронхоскопии инородное тело было удалено у 45 (91,8%) человек. У 41 пациента инородное тело было удалено с первой попытки, тогда как у 4 пациентов оно было удалено частично, и потребовалась повторная процедура. Из оставшихся 4 пациентов инородное тело было успешно удалено с помощью жесткой бронхоскопии у 2 пациентов, а 2 пациента были потеряны для последующего наблюдения. Грануляционная ткань присутствовала у 11 пациентов, отек слизистой оболочки у 8 пациентов и стеноз бронхов у 3 пациентов. Субъекты с грануляционной тканью и отеком слизистой оболочки положительно ответили на пероральные кортикостероиды (0.5 мг / кг преднизолона снижалось в течение 3 недель), тогда как пациенты со стенозом бронхов лечились с помощью повторной баллонной дилатации. У двоих из трех пациентов, перенесших баллонную дилатацию, при контрольной бронхоскопии был минимальный остаточный стеноз (окклюзия 15–20%), тогда как у одного пациента был стойкий стеноз (80%) правого среднедолевого бронха. При последующем наблюдении только у одного пациента была рентгенологическая аномалия (стойкий коллапс правой средней доли). Большинство субъектов ( n = 58, 89,2%) лечились в амбулаторных условиях и были выписаны в тот же день.
Правый нижнедолевой бронх ( n = 15, 30,6%) был наиболее частым местом расположения инородных тел (см. Таблицу 1). У одного пациента были двусторонние инородные тела (металлические винты): по одному в правом промежуточном и левом главном бронхах (рис. 1). Чаще всего для удаления инородных тел использовались щипцы типа «акульи зубы» ( n = 22, 44,9%), за которыми следовали щипцы из крокодиловой кожи ( n = 16, 32,6%). Для извлечения инородного тела у одного пациента использовались корзина Dormia и магнитные щипцы.Осложнения встречались у 4 (6,1%) пациентов, в том числе ссадина слизистой оболочки у одного пациента. У 3 пациентов инородное тело было извлечено из дыхательных путей, но проскользнуло в пищеварительный тракт. Все 4 пациента лечились консервативно, и ни один из них не потребовал дальнейшего вмешательства.
Рис. 1.Рентгенограмма грудной клетки, показывающая 2 инородных тела (металлических винта): одно в правом промежуточном бронхе, а другое — в главном левом бронхе.
Систематический обзор
Всего при поиске литературы было найдено 1314 исследований, из которых 18 исследований (1554 взрослых пациента с трахеобронхиальными инородными телами) были включены (рис.2). 3,4,6,10–12,14,24–34 Об этих исследованиях сообщалось в развитых и развивающихся странах (таблица 2). Был небольшой преобладание мужчин (16 исследований: 536 мужчин, 443 женщины). Правое бронхиальное дерево было наиболее частым местом расположения инородного тела. Был обнаружен широкий спектр инородных тел, тип которых зависит от географического положения.
Рис. 2.Блок-схема исследований, включенных в систематический обзор.
Таблица 2.Исследования с использованием гибкой бронхоскопии для удаления инородного тела
В шести исследованиях сообщалось о доле бронхоскопий, выполненных для указания на удаление инородного тела, от общего числа выполненных бронхоскопий.Доля варьировала от 0,16 до 0,33% с совокупной долей 0,24% (95% ДИ 0,18–0,31) (рис. 3). 11,26,31–33,35 В общей сложности 1185 субъектов (включая текущее исследование) прошли гибкую бронхоскопию для удаления инородных тел. Степень успеха гибкой бронхоскопии для удаления инородного тела варьировалась от 61 до 100%, с совокупной частотой успеха 89,6% (95% ДИ 86,1–93,2) (рис. 4). У остальных пациентов инородные тела были успешно извлечены методом ригидной бронхоскопии ( n = 39, 3.3%) или торакотомия ( n = 26, 2,2%). Четыре (0,3%) пациента отказались от дальнейшего лечения, а 5 человек после процедуры откашлялись от инородного тела. Три субъекта были потеряны для последующего наблюдения, а 2 субъекта выздоровели без дальнейшего лечения. Осложнения, обнаруженные при гибкой бронхоскопии, включали кровотечение ( n = 18), гипоксию ( n = 2), миграцию в другой сегмент бронха ( n = 4), проскальзывание в желудочно-кишечный тракт ( n = 5) , преходящая гипотензия и субфебрильная температура (см. Таблицу 2).Клиническая неоднородность отражалась в разном возрасте субъектов, а также в разных географических регионах и типах инородных тел.
Рис. 3.Распространенность инородных тел при гибкой бронхоскопии у взрослых (модель случайных эффектов). Распространенность в отдельных исследованиях представлена квадратом (процент), через который проходит горизонтальная линия (95% ДИ). Ромб внизу представляет собой совокупную распространенность по данным исследований.
Рис. 4.Успех гибкой бронхоскопии при удалении инородного тела у взрослых (модель случайных эффектов).Распространенность в отдельных исследованиях представлена квадратом (процент), через который проходит горизонтальная линия (95% ДИ). Ромб внизу представляет собой совокупную распространенность по данным исследований.
Наблюдалась значительная неоднородность как в результатах (I 2 > 80%), так и в свидетельствах систематической ошибки публикации на воронкообразном графике (рис. 5). Также были доказательства систематической ошибки публикации во всех статистических тестах (Бегг-Мазумдар: тау Кендалла = -0,532, P = 0,008; Эггер: систематическая ошибка = -2.625, P = 0,009; Харборд: смещение = -3,163, P = 0,046).
Рис. 5.Графики-воронки, сравнивающие пропорцию и стандартную ошибку пропорции для результатов успеха (A) и распространенности инородных тел (B) во время гибкой бронхоскопии. Кружками обозначены испытания, включенные в метаанализ. Линии в центре указывают итоговую пропорцию. Угловые линии представляют 95% ДИ. Были доказательства предвзятости публикации.
Обсуждение
Результаты этого исследования и систематического обзора показывают, что вдыхание инородных тел у взрослых — редкое явление.Кроме того, гибкая бронхоскопия является безопасным и эффективным средством удаления инородных тел из дыхательных путей у взрослого населения. В этом исследовании, охватывающем более трех десятилетий, только 1 из 400 бронхоскопий выполнялась для удаления инородного тела (примерно столько же, сколько в систематическом обзоре). Успешность гибкой бронхоскопии при удалении инородных тел в этом исследовании составила 92%, что аналогично таковому в систематическом обзоре (89,6%).
Жесткая бронхоскопия требуется в большом количестве случаев удаления инородного тела у детей. 12 Однако у взрослых гибкая бронхоскопия в большинстве случаев позволяет избежать необходимости жесткой бронхоскопии (~ 90% согласно систематическому обзору). Гибкая бронхоскопия также имеет несколько преимуществ по сравнению с жесткой бронхоскопией: ее можно проводить в амбулаторных условиях, она более экономична и широко доступна, а также позволяет избежать необходимости в анестезии и седативных средствах. Кроме того, использование гибкой бронхоскопии было связано с более низкой смертностью и заболеваемостью по сравнению с жесткой бронхоскопией (1% против 12%) в исследовании с участием 300 человек, возможно, из-за избегания общей анестезии. 24 В настоящем исследовании гибкая бронхоскопия была связана с минимальными осложнениями (4 пациента), тогда как в систематическом обзоре осложнения включали незначительное кровотечение, гипоксемию, проскальзывание инородного тела в желудочно-кишечный тракт и миграцию инородного тела. в другой сегмент бронха. 3,6,10,28,30,35–37 Однако бывают ситуации, в которых гибкая бронхоскопия оказывается безуспешной при извлечении инородного тела, включая инородные тела, пораженные обширной грануляционной тканью, или чрезмерное рубцевание ткани, большое инородное тело которые нельзя захватить гибкими щипцами, удушающие инородные тела, инородные тела с гладкими краями, острые инородные тела и несколько неудачных попыток гибкой бронхоскопии извлечь инородное тело. 38 В этих случаях жесткая бронхоскопия остается процедурой выбора (Таблица 3). 3,4,6,10,14,22,23,25,35
Таблица 3.Подробные сведения об исследованиях, сообщающих о неудачных попытках удаления инородных тел при гибкой бронхоскопии
Во время гибкой бронхоскопии для извлечения инородных тел используются различные инструменты. тело, например захватывающие щипцы или корзина Дормия, в зависимости от природы инородного тела. Захватывающие или зубные щипцы (зуб аллигатора, зуб акулы и зуб крысы) следует использовать для удаления плоских или тонких неорганических или твердых органических инородных тел, выбор зависит от формы инородного тела. 1 Рыболовная сеть или корзина Dormia используются для извлечения мягких инородных тел, поскольку захват щипцами может вызвать фрагментацию. Чаще всего в этом исследовании использовались щипцы из акульих зубов и аллигатора, поскольку чаще всего встречались металлические или твердые инородные тела. У одного пациента магнитные щипцы и рентгеноскопия использовались для извлечения металлического инородного тела (швейной булавки), застрявшего в дистальном сегменте, не видимом при бронхоскопии. Как только он был извлечен до главного бронха, его удалили щипцами из крокодиловой кожи.
Диагноз аспирации инородного тела трудно установить у взрослых субъектов, не поступавших в анамнезе. 1,3 Большинство субъектов с историей аспирации инородных тел поздно обращаются в медицинское учреждение (только 25% пациентов поступили в течение 7 дней после аспирации в этом исследовании). Это связано с безобидным характером симптомов, которые инородные тела вызывают у взрослого населения, и спонтанным исчезновением симптомов, которое происходит из-за попадания инородного тела в более периферические дыхательные пути. 14,34 Напротив, у детей инородные тела обычно обнаруживаются в проксимальных отделах дыхательных путей и вызывают более серьезные симптомы, в том числе в некоторых случаях дыхательную недостаточность, требующую раннего вмешательства. 3,10–12
Многие взрослые субъекты с трахеобронхиальными инородными телами, описанными в предыдущих исследованиях, имели основной фактор риска, такой как нервно-мышечные заболевания, травмы головы, алкогольная интоксикация или измененные сенсориумы. 4,24,32,35 Напротив, все субъекты (кроме одного с травмой головы) в настоящем исследовании были здоровы и не имели каких-либо специфических факторов риска аспирации инородного тела.Помимо традиционных факторов риска, пищевые привычки, местные обычаи и занятия не только предрасполагают людей к аспирации инородных тел, но также определяют тип инородных тел, встречающихся в конкретной группе населения. В исследовании, проведенном в Хорватии, аспирация костей животных и вишневых косточек была обычным явлением из-за диетических привычек. 32 У здорового китайского населения аспирацию инородного тела связывали с приемом пищи палочками, что увеличивает риск вдыхания инородного тела. 10 В нескольких исследованиях, проведенных на Ближнем Востоке, штифты для тюрбана были наиболее распространенным типом аспирации инородных тел, поскольку их удерживают между зубами при завязывании традиционного тюрбана. 27,28,39,40
Наиболее частым местом расположения инородного тела в дыхательных путях является правое бронхиальное дерево, особенно правые нижние и промежуточные бронхи, из-за вертикальной ориентации правого главного бронха. 1,2,4,14 Двусторонние инородные тела присутствовали только у одного пациента и встречаются редко. 2,32,41,42 Инородные тела не могли быть идентифицированы у 25% субъектов, возможно, из-за спонтанного изгнания инородного тела, растворения органического инородного тела или попадания небольшого инородного тела в грануляционную ткань или отечная слизистая. 43
В центре авторов первым шагом в лечении аспирации инородного тела у взрослых является гибкая бронхоскопия, которая в большинстве случаев является одновременно диагностической и терапевтической. Пациентам, у которых гибкая бронхоскопия не удалась, выполняется жесткая бронхоскопия (рис. 6). Пациентам с грануляционной тканью после извлечения инородного тела назначается короткий курс глюкокортикоидов (0,5 мг / кг преднизолона с постепенным снижением дозы в течение 21 дня). В случае неудачи пациентам проводят криотерапию или коагуляцию аргоновой плазмы; баллонная бронхопластика используется при лечении бронхостеноза.
Рис. 6.Алгоритм лечения инородных тел в дыхательных путях взрослых, использованный в авторском центре.
Это исследование имеет несколько ограничений. Поскольку исследование было ретроспективным, исчерпывающая информация о продолжительности процедуры и другие подробности недоступны. В метаанализе наблюдалась значительная неоднородность и предвзятость публикации, возможно, из-за разницы в профилях субъектов и опыте операторов.
Выводы
Таким образом, вдыхание инородного тела является необычным клиническим явлением у взрослых и требует высокого показателя клинической подозрительности для постановки диагноза, особенно у тех, у кого в анамнезе не было аспирации инородных тел.У взрослых гибкая бронхоскопия безопасна и имеет высокий процент успеха при выявлении и удалении инородных тел.
- Авторские права © 2015 by Daedalus Enterprises
Альбутерол и ипратропий Устные ингаляции: MedlinePlus Информация о лекарствах
Комбинация альбутерола и ипратропия представляет собой раствор (жидкость), который можно вдыхать через рот с помощью небулайзера (устройства, которое превращает лекарство в лекарство). туман, который можно вдыхать) и в виде спрея для вдыхания через рот с помощью ингалятора.Обычно его вдыхают четыре раза в день. Тщательно следуйте инструкциям на этикетке рецепта и попросите своего врача или фармацевта объяснить любую часть, которую вы не понимаете. Используйте альбутерол и ипратропиум точно так, как указано. Не используйте его больше или меньше и не используйте его чаще, чем предписано вашим доктором.
Ваш врач может посоветовать вам использовать дополнительные дозы альбутерола и ипратропия при вдыхании, если вы испытываете такие симптомы, как хрипы, затрудненное дыхание или стеснение в груди. Тщательно следуйте этим указаниям и не используйте дополнительные дозы лекарств, если только ваш врач не скажет вам, что это необходимо.Не используйте более 2 дополнительных доз раствора небулайзера в день. Не используйте спрей для ингаляций более шести раз за 24 часа.
Позвоните своему врачу, если ваши симптомы ухудшатся, если вы чувствуете, что вдыхание альбутерола и ипратропия больше не контролирует ваши симптомы, или если вы обнаружите, что вам нужно чаще использовать дополнительные дозы лекарства.
Если вы используете ингалятор, ваше лекарство будет поставляться в картриджах. Каждый картридж ингаляционного спрея альбутерола и ипратропия рассчитан на 120 ингаляций.Этого лекарства хватит на один месяц, если вы будете делать одну ингаляцию четыре раза в день. После того, как вы используете все 120 доз, ингалятор заблокируется и больше не будет выпускать лекарство. На боковой стороне ингалятора есть индикатор дозы, который отслеживает, сколько лекарства осталось в картридже. Время от времени проверяйте индикатор дозы, чтобы узнать, сколько лекарства осталось. Когда указатель на индикаторе дозы переходит в красную область, в картридже содержится достаточно лекарства на 7 дней, и пора пополнить рецепт, чтобы у вас не закончились лекарства.
Будьте осторожны, чтобы не вдыхать альбутерол и ипратропий в глаза. Если вы попали в глаза альбутеролом и ипратропием, у вас может развиться узкоугольная глаукома (серьезное заболевание глаз, которое может вызвать потерю зрения). Если у вас уже есть узкоугольная глаукома, ваше состояние может ухудшиться. У вас могут быть расширенные зрачки (черные круги в центре глаз), боль или покраснение в глазах, нечеткое зрение и изменения зрения, такие как появление ореолов вокруг огней или появление необычных цветов. Если вы попали в глаза альбутерол и ипратропий, позвоните своему врачу. или если у вас появятся эти симптомы.
Ингалятор, который поставляется с альбутеролом и ипратропиумом в виде спрея, предназначен для использования только с картриджем с альбутеролом и ипратропием. Никогда не используйте его для вдыхания каких-либо других лекарств и не используйте другие ингаляторы для вдыхания лекарства в картридже с альбутеролом и ипратропием.
Перед тем, как использовать ингаляцию альбутерола и ипратропия в первый раз, прочтите письменные инструкции, прилагаемые к ингалятору или небулайзеру. Попросите вашего врача, фармацевта или респираторного терапевта показать вам, как его использовать.Потренируйтесь пользоваться ингалятором или небулайзером, пока он или она смотрит.
Чтобы подготовить ингалятор к использованию, выполните следующие действия:
- Соберите ингалятор перед его первым использованием. Для начала достаньте ингалятор из коробки и держите оранжевый колпачок закрытым. Нажмите на предохранитель и снимите прозрачное основание ингалятора. Будьте осторожны, чтобы не прикасаться к прокалывающему элементу внутри основания.
- Ингалятор необходимо выбросить через три месяца после того, как вы его собрали.Напишите эту дату на этикетке ингалятора, чтобы не забыть, когда вам нужно выбросить ингалятор.
- Достаньте картридж из коробки и вставьте узкий конец в ингалятор. Вы можете прижать ингалятор к твердой поверхности, чтобы убедиться, что он вставлен правильно. Замените прозрачную пластиковую основу на ингаляторе.
- Держите ингалятор вертикально с закрытым оранжевым колпачком. Поверните прозрачную основу в направлении белых стрелок до щелчка.
- Откиньте оранжевую крышку так, чтобы она полностью открылась.Направьте ингалятор на землю.
- Нажать кнопку сброса дозы. Закройте оранжевую крышку.
- Повторяйте шаги 4-6, пока не увидите, как из ингалятора выходит спрей. Затем повторите эти действия еще три раза.
- Ингалятор заправлен и готов к использованию. Вам не нужно будет повторно заправлять ингалятор, если вы не используете его дольше 3 дней. Если вы не используете ингалятор более 3 дней, вам нужно будет выпустить один спрей на землю, прежде чем вы начнете использовать его снова.Если вы не используете ингалятор более 21 дня, вам нужно будет выполнить шаги 4-7, чтобы снова заправить ингалятор.
Чтобы вдохнуть спрей с помощью ингалятора, выполните следующие действия:
- Держите ингалятор вертикально с закрытым оранжевым колпачком. Поверните прозрачную основу в направлении белых стрелок до щелчка.
- Открыть оранжевую крышку.
- Выдохните медленно и полностью.
- Поместите мундштук в рот и сомкните вокруг него губы.Будьте осторожны, не закрывайте губами вентиляционные отверстия.
- Направьте ингалятор в сторону задней стенки горла и вдохните медленно и глубоко.
- На вдохе нажмите кнопку сброса дозы. Продолжайте дышать, пока спрей попадет в ваш рот.
- Задержите дыхание на 10 секунд или столько, сколько вам удобно.
- Выньте ингалятор изо рта и закройте оранжевый колпачок. Держите колпачок закрытым, пока не будете готовы снова использовать ингалятор.
Чтобы вдохнуть раствор с помощью небулайзера, выполните следующие действия:
- Извлеките один флакон с лекарством из пакета из фольги. Положите остальные флаконы обратно в пакет, пока не будете готовы их использовать.
- Открутите верхнюю часть флакона и выжмите всю жидкость в резервуар небулайзера.
- Подсоедините резервуар небулайзера к мундштуку или лицевой маске.
- Подсоедините бачок небулайзера к компрессору.
- Положите мундштук в рот или наденьте лицевую маску.Сядьте в удобное вертикальное положение и включите компрессор.
- Дышите спокойно, глубоко и равномерно через рот в течение 5–15 минут, пока в камере небулайзера не перестанет образовываться туман.
Регулярно очищайте ингалятор или небулайзер. Тщательно следуйте инструкциям производителя и спросите своего врача или фармацевта, если у вас есть какие-либо вопросы о чистке ингалятора или небулайзера.
Респираторный импедансный ответ на глубокий вдох у детей-астматиков со спонтанной обструкцией дыхательных путей
Реферат
Целью исследования было определить, можно ли обнаружить бронхомоторный эффект глубокого вдоха (ДВ) во время приливного дыхания у детей-астматиков со спонтанной обструкцией дыхательных путей (АО).
Обследованы две группы детей в возрасте 5–15 лет. АО была легкой в группе 1 (n = 12, объем форсированного выдоха за одну секунду (ОФВ 1 ) ≥75% от прогнозируемого) и от средней до тяжелой в группе 2 (n = 9, ОФВ 1 ≤70% от прогнозируемого). ). Техника принудительных колебаний при 12 Гц с использованием генератора головы позволила определить респираторное сопротивление на вдохе ( R rsi ) и выдохе ( R rse ) до и после DI, на исходном уровне и после сальбутамола.
На исходном уровне R rsi , но не R rse , как было обнаружено, значительно уменьшалось после DI в группе 1, но не в группе 2. Изменение, вызванное DI, значительно различалось в группе 1 (−1,5 ± 0,5). гПа · с · л -1 ) по сравнению с группой 2 (0,5 ± 0,5 гПа · с · л -1 ) и продемонстрировал значительную отрицательную корреляцию с ОФВ 1 % пред. После сальбутамола ДИ не действовал.
В заключение, у детей-астматиков наблюдается бронхомоторная реакция на глубокий вдох, которая зависит от степени обструкции дыхательных путей.Эффект легче проявляется на вдохе, чем на выдохе.
Это исследование было поддержано EA 3450 «Взаимодействие систем регуляции дыхания с детьми и взрослыми».
Эффект глубокого вдоха (DI) может иметь особое значение для изучения функции дыхания у субъектов с пораженными дыхательными путями, так как он может служить указанием на механизмы обструкции дыхательных путей (AO) 1, 2. Последствия DI для Механика дыхательных путей, по-видимому, определяется главным образом гистерезисом проводящих дыхательных путей по сравнению с тканями легких 3.Гистерезис — это зацикливание трансмурального отношения давления к объему, механическая характеристика структур с несовершенной эластичностью. Согласно Froeb и Mead 3, бронходилатация произойдет после DI, если преобладает бронхиальный гистерезис. Тонус гладкой мускулатуры дыхательных путей является основным фактором, определяющим эффект DI, и было показано, что острый бронхоспазм увеличивает бронхиальный гистерезис 4. Таким образом, нормальные субъекты или астматики с нормальной функцией легких сталкиваются с метахолином, обычно бронходилатом, в ответ на DI 5.И наоборот, у астматиков со спонтанной обструкцией дыхательных путей могут наблюдаться более сложные механические изменения. В результате различных факторов, таких как воспаление дыхательных путей или легких, закрытие дыхательных путей и / или сужение мелких дыхательных путей, паренхиматозный гистерезис может преобладать над гистерезисом дыхательных путей 1. Таким образом, эти пациенты часто демонстрируют бронхоконстрикторный ответ на DI 1,2.
В отличие от большого количества исследований влияния истории объема на механику легких у взрослых субъектов 6, 7, у детей имеется мало данных.У взрослых эффект обычно оценивается по последовательному частичному и максимальному форсированному выдоху. Навык, необходимый для выполнения этого маневра, часто исключает его использование у детей. Альтернативой является метод принудительных колебаний, который можно использовать для измерения сопротивления дыхания ( R RS ) во время приливного дыхания. Таким образом, бронхорасширяющий эффект ДИ был продемонстрирован у детей, которым вводили метахолин 8, 9. Симптоматическая астма может быть ответственной за различную респираторную реакцию на ДИ, но у детей этой гипотезе уделялось мало внимания.Целью этого исследования было описать влияние DI на респираторный импеданс у детей-астматиков со спонтанной АО.
Материалы и методы
Пациенты
Двадцать один астматический ребенок (13 мужчин) в возрасте 5–15 лет, направленный в лабораторию для проверки функции легких, был включен в исследование на основании спонтанной АО. Пациенты были разделены на две группы по степени тяжести АО. В 1-ю группу вошли 12 детей с легкой степенью АО, у.е.е. Исходный объем форсированного выдоха за одну секунду (ОФВ 1 ) был ≥75% от прогнозируемого 10. Пятеро из них принимали ингаляционные стероиды. В группу 2 вошли девять детей с АО средней и тяжелой степени, , то есть , их исходный ОФВ 1 был ≥70% от пред. Пять субъектов принимали ингаляционные стероиды. Прием β-агонистов был прекращен за ≥12 ч до измерений. Эти две группы имели схожие антропометрические характеристики. Исходный уровень ОФВ -1 и максимальный средний поток экспирации (MMEF), очевидно, были значительно больше в группе 1, чем в группе 2 (p <0.001, таблица 1⇓).
Таблица 1—Характеристика детей с легкой (группа 1) и средне-тяжелой (группа 2) обструкцией дыхательных путей
Измерение респираторного импеданса
Аппарат для измерения респираторного импеданса ( Z rs ) (Pulmosfor, SEFAM, Vandoeuvre les Nancy, Франция) был подробно описан ранее 11, за исключением значительной модификации программного обеспечения для более удобного использования и улучшенного обращения. данных.Вкратце, входное давление подавалось через громкоговоритель вокруг головы субъекта, заключенного в навес (техника генератора головы). Таким образом, значительно уменьшились перепад давления и, следовательно, поток через верхнюю стенку дыхательных путей. Период сбора данных длился 30–50 с, в течение которого применялось синусоидальное давление с частотой 12 Гц. Дети носили зажимы для носа и дышали через мундштук, подключенный к пневмотахографу Fleisch № 1 (Metabo, Hepalinges, Швейцария), прикрепленному к датчику дифференциального давления (Micro 176PC14HD2, Honeywell ± 35 гПа; Скарборо, Онтарио, Канада).Коэффициент подавления синфазного сигнала в проточном канале составлял> 60 дБ при 12 Гц. Входное давление измерялось идентичным датчиком, согласованным с первым в пределах 1% амплитуды и 2 ° фазы ≤32 Гц. Сигналы давления и потока фильтровались нижними частотами с частотой 32 Гц с использованием аналоговых фильтров и оцифровывались с частотой дискретизации 192 Гц. Компонент дыхания в сигналах был устранен с помощью фильтра верхних частот Баттерворта 4-го порядка с угловой частотой 6 Гц. Сигналы анализировали колебательный цикл за колебательный цикл, обеспечивая 12 измерений в секунду.Коэффициенты Фурье давления и потока при 12 Гц были вычислены и объединены для получения R RS и респираторного реактивного сопротивления ( X RS ). Была применена поправка для постоянной времени пневмотахографа 2,1 мс. Зашумленные данные были окончательно устранены путем фильтрации значений Z rs , лежащих за пределами 99% доверительного интервала, т.е. , т.е. ниже или выше среднего значения ± 3sd. Процедуру повторяли 3 раза. После каждого сбора данных на экране компьютера отображались временные характеристики приливного потока и объема, R RS и X RS .Записи, показывающие выраженное нерегулярное дыхание или свидетельство закрытия голосовой щели, были отброшены.
Измерение объема форсированного выдоха за одну секунду
FEV 1 измеряли с помощью электронного расходомера (Masterscope Erich Jaeger GmbH, Вюрцбург, Германия). Маневры форсированного выдоха повторялись до пяти раз, и кривая поток / объем с максимальной суммой форсированной жизненной емкости легких + FEV 1 была сохранена. Чтобы избежать изменения истории объема непосредственно перед изучением эффекта DI, измерения FEV 1 во всех случаях были получены после Z rs .
Администрация лекарств
Обратимость АО вызывали введением двух вдохов сальбутамола (Ventoline®, 100 мкг на вдох -1 ) через неэлектростатическую ингаляционную камеру (Nes-Spacer, AstraZeneca, Lund, Sweden). Система доставки лекарства сработала, когда ребенок начал медленно вдыхать из камеры. Затем испытуемого просили задержать дыхание на 5 секунд после окончания вдоха. Нормальное дыхание возобновилось на несколько секунд, и вторая затяжка была произведена таким же образом. Z rs и FEV 1 измерения были повторены через 10 минут после этого.
Анализ данных
Исходно и после сальбутамола был получен первый период приобретения. Сразу же последовало второе наблюдение, во время которого ребенка попросили сделать глубокий вдох. Данные сохранялись, когда соответствующий объем был как минимум вдвое больше среднего дыхательного объема. Были проанализированы три дыхательных цикла до (preDI) и три после DI (postDI).Визуальный осмотр трассировки потока и объема позволил выбрать дыхательные циклы, обычно пропуская первый вдох сразу после DI. В периоды preDI и postDI было рассчитано среднее значение R rs на вдохе ( R rsi ) и выдохе ( R rse ), а также среднее значение X rs для всего респираторного цикл. Величина ответа Rrs на DI выражалась разницей между post и preDI R rsi (Δ R rsi ).
Для оценки влияния степени обструкции дыхательных путей, DI и бронходилатации использовался дизайн дисперсионного анализа (ANOVA) с двумя повторениями (DI и сальбутамол) и одним фактором (FEV 1 ≤70% или ≥75%). Когда соотношение F указывало на значительный эффект, для более точного определения разницы использовался парный t-критерий. Стандартный линейный регрессионный анализ использовали для оценки взаимосвязи между степенью обструкции дыхательных путей и изменением R rsi , вызванным DI.Значение p <0,05 использовалось для определения статистической значимости. Данные выражены как среднее ± средн.
Результаты
ANOVA показал, что: 1) R rsi , R rse и X rs все были значительно изменены сальбутамолом (p <0,002), 2) X rs значимо отличался между группами пациентов (p = 0,005) и 3) значимое взаимодействие на R rsi было продемонстрировано для групп пациентов ( i.е. степени АО), ДИ и сальбутамола (р <0,04).
На исходном уровне не было значимой разницы в R rsi или R rse между группами 1 и 2 (таблица 2 и 3⇓⇓), в то время как X RS было значительно ниже в группе 2 чем в 1-й группе (р <0,02, таблица 4⇓). Образцы реакции на DI показаны на рисунках 1 и 2⇓⇓. Записи были сделаны у одного пациента в каждой группе. DI вызвал значительное снижение R RSI в группе 1 (p = 0.01, таблица 2⇓), тогда как изменение R rse не достигло статистической значимости (p = 0,08, таблица 3⇓). Не было значительных изменений в X RS (таблица 4⇓). В группе 2 ни R rsi , R rse , ни X rs существенно не различались до и после DI (таблица 2–4⇓⇓⇓). Интересно, что также было обнаружено, что, в отличие от значения preDI, postDI R rsi был значительно ниже в группе 1, чем в группе 2 (p = 0.05, таблица 2⇓).
Рис. 1.—Динамика а) респираторного сопротивления ( R RS ) и б) дыхательного объема ( V T) во время глубокого вдоха (DI) у ребенка-астматика с легкой обструкцией дыхательных путей (исходный объем форсированного выдоха за одну секунду 87% прогноз). Каждая точка на графике R rs соответствует одному циклу колебаний. Большинство мгновенных изменений R rs связаны с дыхательным потоком. Непрерывная линия соответствует сглаженным данным и показывает, что DI связан с кратковременным падением R rs , которое затем постепенно возвращается к исходному уровню в течение 30 с.
Рис. 2.—Динамика а) респираторного сопротивления ( R RS ) и б) дыхательного объема ( V T) во время глубокого вдоха (DI) у астматического ребенка с тяжелой обструкцией дыхательных путей (исходный объем форсированного выдоха за одну секунду 34% прогноз). За глубоким вдохом следует увеличение R rs , которое затем постепенно уменьшается к исходному уровню.
Таблица 2-Респираторное сопротивление при вдохе ( R rsi ) у детей с легкой (группа 1) и средне-тяжелой (группа 2) обструкцией дыхательных путей до (до) и после (после) глубокой ингаляции (DI)
Таблица 3—Респираторное сопротивление на выдохе ( R rse ) у детей с легкой (группа 1) и средне-тяжелой (группа 2) обструкцией дыхательных путей до (до) и после (после) глубокого вдоха (DI)
Таблица 4—Респираторное реактивное сопротивление ( X rs ) у детей с легкой (группа 1) и от умеренной до тяжелой (группа 2) обструкцией дыхательных путей до (до) и после (после) глубокой ингаляции (DI)
Было обнаружено, чтоΔ R rsi значительно различается между группами i.е. отрицательно в группе 1 (-1,5 ± 0,5 гПа · с · л -1 ), но не во 2 группе (0,5 ± 0,5 гПа · с · л -1 , p = 0,02). Изучение взаимосвязи между степенью АО и реакцией на DI во время АО выявило значительную корреляцию между FEV 1 % pred и Δ R rsi (p = 0,02, рис. 3). Аналогичная взаимосвязь была обнаружена между Δ R rsi и MMEF% pred (p = 0,06), но это не достигло статистической значимости.
Рис. 3.—Величина изменения сопротивления вдоху ( R rsi ), вызванного глубоким вдохом, показывает значительную корреляцию со степенью исходной обструкции дыхательных путей, выраженной как объем форсированного выдоха за одну секунду (FEV 1 )% пред (p = 0.02). Отрицательные значения Δ R rsi указывают на расширение бронхов.
После сальбутамола ОФВ 1 значительно увеличился с 1,6 ± 0,1 л до 1,9 ± 0,2 л в группе 1 (р <0,001) и с 1,1 ± 0,2 л до 1,6 ± 0,3 л в группе 2 (р <0,004). В обеих группах R rsi и R rse значительно снизились (p <0,005), тогда как X rs не изменились в группе 1 (p = 0,1) и увеличились во 2 группе (p = 0.03) (таблицы 2–4⇑⇑⇑). Ни R rsi , ни R rse не различались между группами (таблица 2 и 3⇑⇑), но X rs все еще был ниже в группе 2, чем в группе 1 после сальбутамола ( p = 0,02, таблица 4⇑). DI не вызывал значительных изменений ни по одному параметру ни в одной из групп (таблицы 2–4⇑⇑⇑).
Обсуждение
Подводя итог, в этой популяции молодых астматиков образец ответа на DI, по-видимому, зависит от тяжести спонтанной АО.У детей с легкой степенью АО наблюдается значительное снижение R rsi после DI, в то время как у детей с умеренной или тяжелой АО не наблюдается улучшения или ухудшения.
Методические вопросы
Сравнение потоков, возникающих в результате последовательных маневров частичного и максимального форсированного выдоха, рассматривается как золотой стандарт для изучения механики дыхательных путей в отношении истории объема 6, 7. Измерение Z rs не требует активного взаимодействия и поэтому особенно адаптировано для дети.Относительно высокие частоты возбуждения необходимы из-за гармоничного состава дыхательного потока у детей и, по опыту авторов, трудно получить достоверные данные <10 Гц. Исследование Z rs с использованием многочастотных входных сигналов в нормальной популяции детей показало, что функция когерентности ≥0,95 может быть получена во всех случаях ≥12 Гц 12. Недостатком высокочастотных колебаний давления является потенциальный источник ошибки, связанной с проксимальным шунтированием потока дыхательных путей, что может быть особенно значительным у детей с АО 13, 14.В этом исследовании движение стенки верхних дыхательных путей было минимизировано за счет изменения давления на дыхательных путях вокруг головы субъекта, что позволило снизить разницу давления на щеках 15.
Анализ максимальных / частичных потоков форсированного выдоха позволяет оценить влияние DI за один вдох, в то время как измерения Z rs должны выполняться на нескольких вдохах, чтобы получить достоверно интерпретируемые данные. Поскольку сообщалось, что бронхорасширяющий эффект DI ослабевает с постоянной времени около 11 с у взрослых 16, анализ был ограничен тремя вдохами, сделанными вскоре после DI, чтобы минимизировать эффект времени.Связь между ΔRrsi и ОФВ 1 у детей (рис. 3) соответствовала предыдущим сообщениям о маневрах максимального / частичного выдоха у взрослых, где величина бронхолитического эффекта DI была обратно пропорциональна тяжести спонтанной АО 2. Таким образом, авторы считают, что условия измерения в этом исследовании были оптимальными для обнаружения респираторных механических событий, непосредственно связанных с DI.
Функция легких в группах 1 и 2
Может показаться удивительным, что в двух группах пациентов с разным ОФВ 1 исходный уровень R rs существенно не отличался.В обеих группах было заметное падение R rs после сальбутамола, что указывает на то, что исходные значения были явно ненормальными. Форсированный выдох и приливное дыхание — это два разных паттерна, во время которых результаты, относящиеся к АО, могут не совпадать. Во время маневра форсированного выдоха, в отличие от приливного дыхания, рефлекторное отведение гортани сводит к минимуму вклад верхних дыхательных путей 17, а снижение ОФВ 1 обычно рассматривается как показатель ограничения потока во внутригрудных дыхательных путях.Это не обязательно может отражать увеличение сопротивления всего дерева дыхательных путей, в котором глотка и гортань вносят значительный вклад, с последующим воздействием на R rs . Тем не менее, стоит отметить, что после DI между двумя группами наблюдалась значительная разница в исходном уровне R rs . Имеются дополнительные указания, в соответствии с более низким ОФВ -1 , что аномалии внутригрудных дыхательных путей были более значительными в группе 2, чем в группе 1. X rs был явно ненормальным в группе с тяжелой АО по сравнению с нормативными значениями у детей (около +1 гПа · с · л -1 при 12 Гц) 12, а также был значительно ниже, чем в группе 1. Отрицательный результат X rs может отражать повышенную очевидную респираторную эластичность, вызванную, например, неоднородным поведением дыхательной системы 18, и было значительно увеличено по сравнению с исходным уровнем после сальбутамола. В группе 1 X rs был положительным, выражая доминирующую инертность дыхательных путей на этой частоте, и на него не влиял сальбутамол.В результате X rs все еще было значительно ниже в группе 2, чем в группе 1 после ингаляции бронходилататора. Таким образом, результаты в группе 2 согласуются с умеренной или тяжелой АО, связанной с увеличением кажущейся респираторной эластичности, частично отменяемой бронходилататором.
Последствия глубокого вдоха
Было обнаружено, что снижение R rs после DI в группе 1 было значительным на вдохе, но не на выдохе.На людях было показано, что во время приливного выдоха прогрессирующее закрытие голосовой щели обычно происходит параллельно с уменьшением объема 19. Закрытие голосовой щели, связанное с бронхостенозом 20–22, также более заметно при выдохе, чем при вдохе 22. Кроме того, имеются доказательства. при условии, что сопротивление гортани может быть изменено DI, направление изменения зависит от наличия AO. После DI сопротивление гортани снижалось у здоровых субъектов и стабильных астматиков и увеличивалось у здоровых субъектов с бронхоспазмом, вызванным метахолином, а также у астматиков во время приступа астмы 23.Такое увеличение сопротивления гортани в ответ на DI было бы более эффективным для увеличения R rs на выдохе, чем на вдохе, тем самым минимизируя экспрессию в R rse бронхорасширяющего эффекта DI.
Результаты, полученные в группе 1, согласуются с исследованием Milanese et al . 8, где спонтанная АО была заподозрена у девяти дошкольников на основании снижения R rs > 30% после приема сальбутамола.Milanese et al. 8 показал значительное снижение R rs после DI и отсутствие изменения резонансной частоты на исходном уровне. Хотя ОФВ 1 не измерялся, реакция похожа на ту, что наблюдалась у субъектов из группы 1 настоящего исследования, где R RSI значительно снизился после DI, но X RS не изменился. Однако данные по сальбутамолу в двух исследованиях различаются: Milanese et al. 8 описал значительное увеличение R rs после DI, в то время как в настоящем исследовании не было обнаружено значительных изменений (таблицы 2–4⇑⇑⇑). Следует отметить, что характеристики двух популяций были разными. Первое исследование включало только детей дошкольного возраста, в то время как настоящее исследование включало детей как дошкольного, так и школьного возраста. Это может иметь особое значение, поскольку недавний отчет о реакции бронходилататоров на DI у астматиков с различной степенью АО описал значительную обратную зависимость между величиной этого ответа и возрастом 24 года.Кроме того, Milanese et al. 8 изучали детей с рецидивирующим свистящим дыханием, которым при необходимости требовались только β-агонисты короткого действия 8, в то время как некоторым детям-астматикам в настоящем исследовании требовались ингаляционные стероиды и / или у них были серьезные респираторные заболевания. В этой связи стоит отметить, что после сальбутамола X rs все же было значительно ниже в группе 2, чем в группе 1.
В группе 2 данные явно отличаются от предыдущих наблюдений у детей, у которых АО была остро вызвана ингаляцией метахолина 8, 9 и где было обнаружено как увеличение R rs , так и снижение X rs быть значительно отмененным DI 9.Интерпретация заключалась в том, что в контексте острого сужения бронхов гистерезис дыхательных путей, вероятно, будет увеличиваться, а DI будет способствовать бронходилатации 3, 6, 7. И наоборот, отсутствие увеличения R rs и уменьшение X rs у субъектов в настоящем исследовании может указывать на то, что эффекту DI на гистерезис дыхательных путей противодействовало увеличение паренхиматозного гистерезиса. Гиперинфляция легких является частым признаком хронической астмы 25. Это может быть важно для определения ответа на DI, так как оно может быть связано с повышенным гистерезисом тканей легких, который способствует бронхоконстрикторной реакции на DI.В настоящем исследовании отсутствовала систематическая оценка общей емкости легких для оценки вклада этого механизма. Также возможно, что сужение, происходящее дистальнее респираторных бронхиол, может вызвать усиление паренхиматозного гистерезиса 1. Другое возможное объяснение состоит в том, что воспаление и отек в стенке дыхательных путей снижает эластическую нагрузку на внутрипаренхиматозные дыхательные пути, что приводит к меньшей взаимозависимости между этими дыхательными путями и тканями легких. 26. Однако фигура 2⇑, которая указывает на сужение бронхов после DI, не поддерживает эту гипотезу, поскольку значительное снижение R rs происходит во время инспираторного маневра, что предполагает некоторую степень взаимозависимости между паренхимой легкого и проводящими дыхательными путями.
В заключение, в этой популяции детей-астматиков бронхомоторный эффект глубокого вдоха может быть продемонстрирован путем измерения сопротивления дыхания с помощью техники принудительных колебаний. Бронходилатация, по-видимому, легче обнаруживается на вдохе, чем на выдохе у субъектов с легкой обструкцией дыхательных путей, но не у пациентов с умеренной или тяжелой обструкцией дыхательных путей. Величина изменения респираторного сопротивления при вдохе, вызванного глубоким вдохом, обратно пропорциональна степени исходной обструкции дыхательных путей.Глубокое вдыхание не влияет на респираторную реактивность, которая, тем не менее, позволяет дифференцировать легкую обструкцию дыхательных путей от умеренной до тяжелой обструкции дыхательных путей и легко чувствительна к сальбутамолу в последней группе. Необходимы дальнейшие исследования для оценки полезности реакции респираторного сопротивления на глубокий вдох для характеристики заболевания дыхательных путей у детей.
Благодарности
Авторы признательны Б. Шалону, К. Шоне, Г. Колину и С.Мелин за техническую помощь, Н. Бертен и К. Креза за секретарскую помощь и Р. Песлину за плодотворное обсуждение.
- Получено 6 июля 2001 г.
- Принято 12 января 2002 г.
Ссылки
- ↵
Бернс С.Б., Тейлор В.Р., Ингрэм Р. Эффекты глубокого вдоха при астме: относительный гистерезис дыхательных путей и паренхимы. J. Appl Physiol 1985; 59: 1590–1596.
- ↵
Lim TK, Pride NB, Ingram RH.Эффекты объемного анамнеза во время спонтанной и острой обструкции воздушного потока при астме. Am Rev Respir Dis 1987; 135: 591–596.
- ↵
Froeb HF, Mead J. Относительный гистерезис мертвого пространства и легких in vivo . J Appl Physiol 1968; 25: 244–248.
- ↵
Сасаки Х., Хоппин Ф.Г. Гистерезис сокращенных гладких мышц дыхательных путей. J Appl Physiol 1979; 47: 1251–1262.
- ↵
Fish JE, Анкин М.Г., Келли Дж.Ф., Петерман VI.Регулирование бронхомоторного тонуса за счет раздувания легких у астматиков и неастматиков. J Appl Physiol 1981; 50: 1079–1086.
- ↵
Инграм Р. Взаимосвязь между паренхиматозными и дыхательными взаимодействиями, реактивностью легких и воспалением при астме. Сундук 1995; 107: 148с – 152с.
- ↵
Pellegrino R, Sterk PJ, Sont JK, Brusasco V. Оценка влияния глубокого вдоха на калибр дыхательных путей: новый подход к функции легких при бронхиальной астме и ХОБЛ.Eur Respir J 1998; 12: 1219–1227.
- ↵
Milanese M, Mondino C, Tosca M, Canonica GW, Brusasco V. Модуляция калибра дыхательных путей у детей путем глубокого вдоха. J Appl Physiol 2000; 88: 1259–1264.
- ↵
Маршал Ф., Швейцер С., Моро-Колсон С. Ответ респираторного импеданса на глубокий вдох у детей. Педиатр Пульмонол 2002; (под давлением).
- ↵
Knudson RJ, Lebowitz MD, Holberg CJ, Берроуз Б.Изменения нормальной кривой максимального выдоха потока-объема с ростом и старением. Am Rev Respir Dis 1983; 127: 725–734.
- ↵
Peslin R, Marchal F, Duvivier C, Ying Y, Gallina C. Оценка модифицированного генератора головы для измерения респираторного импеданса. Eur Respir Rev 1991; 1: 140–145.
- ↵
Mazurek H, Willim G, Marchal F, Haluszka J, Tomalak W. Входное сопротивление дыхания, измеренное генератором головы у детей дошкольного возраста.Педиатр Пульмонол 2000; 30: 47–55.
- ↵
Cauberghs M, van de Woestijne KP. Влияние шунта верхних дыхательных путей и свойств серий на измерения импеданса дыхательных путей. J. Appl Physiol 1989; 66: 2274–2279.
- ↵
Marchal F, Mazurek H, Habib M, Duvivier C, Derelle J, Peslin R. Входное респираторное сопротивление для оценки гиперреактивности дыхательных путей у детей: стандартный метод по сравнению с генератором головы .Eur Respir J 1994; 7: 601–607.
- ↵
Peslin R, Duvivier C, Didelon J, Gallina C. Дыхательный импеданс измеряется с помощью генератора головы для минимизации шунта верхних дыхательных путей. J Appl Physiol 1985; 59: 1790–1795.
- ↵
Пархэм В.М., Шепард Р.Х., Норман П.С., Фиш Дж. Анализ динамики и величины влияния инфляции легких на тонус дыхательных путей: связь с реактивностью дыхательных путей. Am Rev Respir Crit Care Med 1983; 128: 240–245.
- ↵
Clément J, Stanescu DC, van de Woestijne KP. Открытие Glottis и зависящая от усилия часть кривых давления-расхода изобома. J Appl Physiol 1973; 34: 18–22.
- ↵
Peslin R, Fredberg JJ. Колебательная механика дыхательной системы В : Фишман П.А., Маклем П.Т., Мид Дж., Редакторы. Справочник по физиологии. Дыхательная система. Механика дыхания Балтимор, Уильям и Уилкинс, 1986; стр.145–177.
- ↵
Brancatisano T, Dodd D, Engel LA. Факторы, влияющие на размеры голосовой щели при форсированном выдохе. J Appl Physiol 1983; 55: 1825–1829.
- ↵
England SJ, Ho V, Zamel N. Сужение гортани у нормальных людей во время экспериментально вызванного сужения бронхов. J. Appl Physiol 1985; 58: 352–356.
-
Хиггенботтам Т.Сужение голосовой щели у людей, связанное с экспериментально индуцированным бронхоспазмом. J Appl Physiol 1980; 49: 403-407.
- ↵
Collett PW, Brancatisano T, Engel LA. Изменения голосовой щели при бронхиальной астме. Am Rev Respir Dis 1983; 128: 719–723.
- ↵
Секизава К., Янал М., Сасаки Х., Такисима Т. Влияние предыдущего произвольного глубокого вдоха на сопротивление гортани у здоровых и астматических субъектов.J Appl Physiol 1987; 63: 1406–1412.
- ↵
Pacini F, Filippelli M, Duranti R, et al. Уменьшение бронходилатации после глубокого вдоха плохо связано с воспалением дыхательных путей при астме. Eur Respir J 1999; 14: 1055–1060.
- ↵
Pellegrino R, Brusasco V. О причинах гиперинфляции легких при бронхоспазме. Eur Respir J 1997; 10: 468–475.
- ↵
Macklem PT.Теоретический анализ влияния нагрузки гладких мышц дыхательных путей на сужение дыхательных путей. Am J Respir Crit Care Med 1996; 153: 83–89.
Оральная ингаляция для доставки белков и пептидов в легкие
https://doi.org/10.1016/j.ejpb.2021.04.003Получить права и контентОсновные моменты
- •
-
Основное применение при обструктивных заболеваниях легких и острый респираторный дистресс-синдром.
- •
-
Аэрозолизация жидких составов является наиболее распространенным методом введения.
- •
-
На более поздних этапах клинической стадии: AIR ДНКаза, ингибитор α1-протеиназы, нейраминидаза, гепарин.
Реферат
Пероральные ингаляции являются предпочтительным путем доставки небольших молекул в легкие, поскольку высокие уровни в тканях могут быть достигнуты вскоре после нанесения. Биопрепараты в основном вводятся путем внутривенной инъекции, но ингаляция может быть полезной для лечения заболеваний легких (например, астмы). В этом обзоре обсуждаются биологические и фармацевтические проблемы доставки биопрепаратов и описываются многообещающие кандидаты.Недостаточная стабильность белков во время аэрозолизации и биологическая среда легких являются основными препятствиями для доставки биопрепаратов в легкие. Новые небулайзеры улучшат доставку за счет уменьшения напряжения сдвига и введения, поскольку сухой порошок кажется подходящим для доставки биопрепаратов. Другие многообещающие стратегии включают пегилирование и разработку фрагментов антител, в то время как инкапсулированные в носители системы в настоящее время не играют важной роли в доставке биопрепаратов в легкие при заболеваниях легких.В то время как разработка различных биопрепаратов была остановлена или продемонстрировала незначительный эффект, AIR-ДНКаза, ингибитор альфа1-протеиназы, рекомбинантная нейраминидаза и гепарин в настоящее время оцениваются в фазе III испытаний. Несколько биопрепаратов проходят испытания для лечения коронавирусной болезни (COVID) -19, и ожидается, что эти испытания приведут к улучшению доставки биопрепаратов в легкие.
Ключевые слова
Вдыхание
Биопрепараты
Доставка лекарств
Небулайзеры
Заболевания легких
Доставка белка
Лечение ОРДС
Рекомендуемые статьиЦитирующие статьи (0)
© 2021 Автор (s).Опубликовано Elsevier B.V.
Рекомендуемые статьи
Цитирующие статьи
Нарушения при вдыхании | IOSH
Расстройства дыхания — это нарушения функций, связанные с вдыханием вещества, которое может быть в форме пыли, дыма, тумана, газа или пара.
Фон
Воздух на многих рабочих местах содержит опасные вещества в виде пыли, дыма, тумана, газов и паров. Эти вещества могут быть химическими или биологическими агентами, например, аллергенами животных, спорами грибов и бактериями.Когда рабочие их вдыхают, они могут повредить легкие и другие части дыхательных путей. В некоторых случаях опасные агенты перемещаются через легкие в другие части тела, нанося вред другим органам.
Дыхательная система делится на три области:
- Верхние дыхательные пути или дыхательные пути, включая рот, нос, пазухи, глотку и гортань
- Средние дыхательные пути, включая трахею и бронхи
- Нижние дыхательные пути, включая бронхиолы и альвеолы.
Многие люди имеют генетическую предрасположенность к аллергическим заболеваниям. После воздействия химических или биологических агентов у них с большей вероятностью разовьются такие заболевания, как ринит и астма. Многие заболевания, описанные в этом разделе веб-сайта, могут возникать без профессионального воздействия.
Типы ингаляционных проблем: определения и симптомы
- Раздражение
- Астма
- Ринит
- Хроническая обструктивная болезнь легких (ХОБЛ)
- Биссиноз
- Пневмокониоз
- Внешний аллергический альвеолит
- Вдыхание лихорадки
- Рак (включая мезотелиому)
- Инфекции
- Удушье
Раздражение дыхательных путей может быть вызвано пылью, газами, парами и парами.Эти газы также могут раздражать глаза. Часть дыхательных путей, пораженная газом или дымом, определяется их растворимостью. Легко растворимые газы, такие как аммиак, немедленно воздействуют на верхние дыхательные пути (и глаза). Обычно, если кто-то подвергается воздействию раздражителя, он отходит от источника, ограничивая любой ущерб. Очень сильное воздействие или постоянное воздействие опасного вещества может привести к поражению более мелких дыхательных путей, что приведет к воспалению и отеку бронхиолярной и альвеолярной стенок (отеку легких), что может привести к летальному исходу, если не лечить.Другие растворимые газы включают хлор и диоксид серы. Относительно нерастворимые газы, такие как фосген, могут не иметь немедленного эффекта, но могут вызвать отек легких через несколько часов после воздействия. Азотная кислота, фтор и озон также могут вызывать замедленную реакцию.
Некоторые раздражители могут также вызвать необратимое повреждение легких, особенно если воздействие очень сильное или происходит часто. Другие могут предрасполагать людей к таким состояниям, как хроническая обструктивная болезнь легких (ХОБЛ) или пневмония.
Астма — наиболее часто регистрируемое профессиональное респираторное заболевание в Великобритании.Это хроническое заболевание, характеризующееся периодическим воспалением бронхов и напряжением окружающих их мышц. Это происходит в ответ на один или несколько триггеров. Типичные симптомы включают хрипы, кашель, стеснение в груди и одышку.
Астму, вызванную работой, можно разделить на две категории: профессиональная астма и астма, усугубляемая работой. Профессиональная астма может быть вызвана широким спектром агентов, известных как астмагены. К ним относятся химические вещества, такие как изоцианаты и ангидриды кислот, а также биологические материалы, такие как мучная пыль и некоторые белки, и аллергены лабораторных животных, такие как кожа, моча, мех или слюна крыс и мышей.
Обычно состояние сотрудников, страдающих профессиональной астмой, ухудшается в течение рабочей недели и улучшается в выходные дни или во время отсутствия на работе.
Астма, усугубляемая работой, — это уже существующая астма, которая усугубляется чем-то на рабочем месте. Иногда это называют астмой, связанной с работой.
Опасные вещества, раздражающие дыхательные пути, могут вызывать приступы астмы у людей с профессиональной астмой, а также у людей с астмой, связанной с работой.
Чтобы узнать больше о причинах астмы, ознакомьтесь со списком сотрудников HSE, которые обычно страдают, и веществами, вызывающими профессиональную астму, и справочником астмагенов.
Ринит — это воспаление клеток, выстилающих нос. Симптомы включают заложенность носа, зуд, чихание и выделения из носа. Астма и ринит часто сосуществуют. С астмой и ринитом связан конъюнктивит, который характеризуется зудом, слезотечением и воспалением глаз. Важно, чтобы работодатели и сотрудники серьезно относились к риниту, поскольку он может перерасти в профессиональную астму.
Хроническая обструктивная болезнь легких (ХОБЛ) — заболевание легких, при котором со временем дыхательные пути сужаются, что затрудняет дыхание. Другие симптомы включают кашель, хрипы и увеличение выделения мокроты. Хронический бронхит и эмфизема — это разновидности ХОБЛ.
Основной причиной ХОБЛ является курение, хотя воздействие различных типов опасных веществ может вызывать или способствовать его развитию.
Биссиноз вызывается вдыханием необработанной хлопковой пыли.Сейчас это очень редко в Великобритании и других развитых странах. Симптомы включают одышку, кашель и непроходимость дыхательных путей. Симптомы обычно возникают в первый день рабочей недели и проходят в более поздние дни. Если сотрудник подвергается воздействию хлопковой пыли в течение длительного времени, его симптомы могут стать хроническими.
Пневмокониоз охватывает группу заболеваний легких, вызываемых вдыханием нерастворимой пыли, в основном минеральной пыли, от которой легкие не могут избавиться. Наиболее распространенными заболеваниями этой группы являются силикоз, шахтерский пневмокониоз и асбестоз.
- Силикоз вызывается вдыханием пыли кристаллического кремнезема (кварца). Обычно это происходит у людей, работающих в карьерах, горных выработках и пескоструйных работах, а также у тех, кто работает в гончарной промышленности и на металлургических заводах. Это «прогрессирующее» заболевание — оно ухудшается даже после прекращения воздействия — и для него характерно возрастающее затруднение дыхания, иногда приводящее к смерти.
- Пневмокониоз шахтеров возникает при вдыхании угольной пыли.Он характеризуется легким кашлем и выделением черной мокроты. У некоторых людей это приводит к прогрессирующему массивному фиброзу, инвалидности и смерти. С упадком горнодобывающей промышленности в Великобритании это заболевание стало менее распространенным.
- Асбестоз характеризуется рубцеванием или фиброзом легких в результате длительного воздействия асбеста. Симптомы включают одышку, непродуктивный кашель и «удары пальцами» — деформацию пальцев и ногтей.Обычно это прогрессирующее заболевание, которое неизменно приводит к смерти. Это также связано с мезотелиомой и раком бронхов (см. Ниже).
Внешний аллергический альвеолит вызывается вдыханием определенных органических материалов, обычно спор грибов. Альвеолит — это воспаление альвеол аллергеном. Симптомы обычно появляются через несколько часов после контакта с гриппом: лихорадка, усталость и дрожь. По мере прогрессирования болезни у больного появляется одышка и появляется кашель.Продолжительное воздействие может привести к хроническим симптомам и фиброзу легких. «Легкое фермера» — это тип внешнего аллергического альвеолита, который вызывается вдыханием пыли или спор заплесневелого сена, зерна или соломы.
Ингаляционная лихорадка включает лихорадку от полимерного дыма и лихорадку от дыма от металла. Лихорадка от полимерного дыма вызывается вдыханием дыма, который выделяется при нагревании политетрафторэтилена до высокой температуры. Симптомы напоминают грипп и включают жар, кашель, боли или стеснение в груди.
Металлический дым возникает при вдыхании дыма, содержащего некоторые типы оксидов металлов, например оксида цинка и оксида магния, или вдыхания дыма, выделяющегося при нагревании или плавлении металлов. Больной испытывает симптомы, похожие на грипп, включая жар, кашель, боли или стеснение в груди. Обычно он встречается у сварщиков и литейщиков.
Рак может возникнуть в любом месте дыхательных путей, от носа до легких. Хотя основной причиной рака легких и других видов рака дыхательных путей является курение, опасные вещества, обнаруженные на некоторых рабочих местах, также могут вызывать рак, например кристаллический кремнезем, частицы выхлопных газов дизельных двигателей и газ радон.
Воздействие асбеста может вызвать рак легких или мезотелиому — рак слизистой оболочки легких или кишечника. Относительно низкий уровень или кратковременное воздействие асбеста может вызвать оба типа рака. Люди, которые обычно подвергаются воздействию асбеста и, следовательно, подвергаются более высокому риску, — это сантехники, плотники и другие строительные и ремонтные рабочие. Обычно между первым контактом и появлением симптомов проходит длительный промежуток времени (до 50 лет). Если рабочие подвергаются воздействию асбеста и также курят, у них гораздо выше риск развития рака легких, чем у тех, кто подвергается воздействию только асбеста или только курит.Дополнительную информацию можно найти в справочнике НИУ ВШЭ по заболеваниям, связанным с асбестом.
Люди, подвергающиеся воздействию полициклических ароматических углеводородов, например работники коксовой промышленности, подвергаются более высокому риску развития рака легких. Другие легочные канцерогены включают мышьяк, кадмий, хром и никель.
Люди, работающие с деревом или кожей и находящиеся в пыльных условиях, подвергаются повышенному риску рака носовых пазух.
Вы можете получить информацию о влиянии рака легких, мезотелиомы и носа / носовых пазух в Бремя профессионального рака в Великобритании.
Инфекции , вызываемые агентами на рабочем месте, составляют очень небольшую долю более серьезных проблем, связанных с вдыханием на работе. В 2006 году в THOR был зарегистрирован 51 случай профессиональных респираторных инфекционных заболеваний.
К профессионально связанным инфекциям относятся сибирская язва, орнитологический орнитоз, болезнь легионеров и птичий грипп (птичий грипп). Подробнее читайте в отчете НИУ ВШЭ «Инфекции на работе: управление рисками».
Удушье представляет опасность для людей, работающих в ограниченном пространстве, например сварщиков.Когда кислород вытесняется газом или паром, людям может быть трудно или даже невозможно дышать. Удушающие средства можно разделить на простые и химические удушающие. Простые удушающие агенты — это инертные газы или пары, такие как азот, углекислый газ, водород и метан, которые вытесняют кислород из воздуха, когда они находятся в высоких концентрациях. К химическим удушающим агентам относятся окись углерода, которая в сочетании с гемоглобином предотвращает доставку кислорода к клеткам, а также цианистый водород и сероводород, которые нарушают дыхание на клеточном уровне.
Статистика
Приблизительно 12 000 человек умирают каждый год из-за профессиональных респираторных заболеваний и около двух третей из них из-за болезней, связанных с асбестом, или ХОБЛ.
Согласно Обзору рабочей силы, около 33 000 рабочих, которые работали в 2014/15 году, страдали проблемами дыхания или легких, которые, по их мнению, были вызваны или усугублены их работой. Эта оценка включает респираторные заболевания, помимо профессиональной астмы. Исследование также пришло к выводу, что в том же году из-за проблем с дыханием или легкими было потеряно 664 000 рабочих дней, что в среднем составляет 12 рабочих дней.5 рабочих дней потеряно по каждому делу.
По оценкам программы THOR, финансируемой HSE, в 2014 году было зарегистрировано 1 550 новых случаев респираторных заболеваний, связанных с работой. Однако система THOR не подлежит отчетности, и другие данные свидетельствуют о том, что истинный уровень заболеваемости может быть намного выше.
В HSE есть страницы с последней доступной статистикой по профессиональной астме, ХОБЛ, пневмокониозу и силикозу.
Разработано в сотрудничестве с:
Индекс клиренса легких для определения эффективности ингаляции лизина азтреонама у пациентов с муковисцидозом и близкой к нормальной спирометрии — Одноцентровое технико-экономическое обоснование
Abstract
Сравнение эффективности ингаляционных антибиотиков может быть затруднено в небольших группах пациентов с муковисцидозом и легкой болезнью легких.В технико-экономическом исследовании мы сравнили азтреонам лизин для ингаляционного раствора (AZLI; Cayston ® ) со стандартной ингаляционной антибактериальной терапией у пациентов с муковисцидозом и близкой к нормальной спирометрии . Для определения реакции на лечение мы использовали как индекс клиренса легких (LCI), так и объем форсированного выдоха за одну секунду (FEV 1 ). Исходно медиана ОФВ –1 составляла 87% от пред. а медиана LCI составила 8,6 (верхний предел нормы: 7,0). Через 4 недели после AZLI индекс LCI улучшился на -0,36 и ухудшился на +0.12 после лечения тобрамицином (p = 0,039). Никаких существенных различий между видами лечения (p = 0,195) не наблюдалось при использовании FEV 1 . Эти результаты предполагают, что индекс клиренса легких можно использовать для обнаружения изменений, вызванных лечением, у субъектов с легким заболеванием легких.
Образец цитирования: Ellemunter H, Steinkamp G (2019) Индекс клиренса легких для определения эффективности ингаляции азтреонама лизина у пациентов с муковисцидозом и спирометрией, близкой к нормальной — одноцентровое технико-экономическое обоснование.PLoS ONE 14 (9): e0221673. https://doi.org/10.1371/journal.pone.0221673
Редактор: Иратче Пуэбла, Публичная научная библиотека, СОЕДИНЕННОЕ КОРОЛЕВСТВО
Поступила: 27 марта 2018 г .; Одобрена: 10 августа 2019 г .; Опубликовано: 9 сентября 2019 г.
Авторские права: © 2019 Ellemunter, Steinkamp. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Это исследование было поддержано исследовательским грантом компании Gilead Sciences Inc. Wagramerstrasse 19, 1220 Вена, Австрия (www.gilead.com). Кроме того, AZLI, использованный в исследовании, был предоставлен компанией Gilead Sciences, производителем AZLI. Мы также благодарим CF-TEAM FORSCHUNG за финансовую поддержку, Инсбрук, Австрия (www.cf-team.at) в GS. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Мы ознакомились с политикой журнала, и у авторов этой рукописи есть следующие конкурирующие интересы: Автор Гельмут Эллемюнтер получил грант на исследования, спонсируемый исследователем, от Gilead Sciences Inc. и был членом Консультативного совета Gilead. ALZI, использованный в исследовании, был предоставлен компанией Gilead Sciences, производителем AZLI.Автор Gratiana Steinkamp при финансовой поддержке CF-TEAM FORSCHUNG, Инсбрук, Австрия. Это не влияет на нашу приверженность политике PLOS ONE в отношении обмена данными и материалами.
Введение
Ингаляционные антибиотики важны для подавления хронической P . aeruginosa (PA) у пациентов с муковисцидозом (CF). Азтреонам лизин (AZLI, Cayston ® ) для ингаляционного раствора был лицензирован в Европе в 2009 году для подавляющей терапии хронических легочных инфекций, вызванных Pseudomonas aeruginosa , у пациентов с МВ в возрасте от 6 лет и старше.Основные клинические испытания проводились у пациентов с нарушением функции легких, т.е. объем форсированного выдоха за одну секунду (ОФВ 1 ) ≤75% от прогнозируемого нормального значения [1–3]. У пациентов с умеренным и тяжелым заболеванием легких Азтреонам превосходил ингаляционный тобрамицин.
Из-за улучшения общего состояния нынешних популяций МВ у многих пациентов ОФВ нормальный или близкий к норме 1 , несмотря на хронический P . Инфекция aeruginosa [4].Доступно лишь немного информации об эффективности ингаляционных антипсевдомонадных антибиотиков у этих субъектов. В целом, с небольшими когортами пациентов до 20 пациентов трудно обнаружить изменения после лечения, используя FEV 1 в качестве конечной точки [5,6]. Это особенно актуально, если нужно сравнить два активных соединения или если ингаляционный антибиотик заменен обычным лекарством на новое. В Центре CF в Инсбруке мы уже много лет используем методику множественного вымывания дыханием (MBW) для измерения индекса клиренса легких (LCI) [7].Аномальный ИАП ассоциируется с ранним структурным заболеванием легких, обнаруживаемым с помощью компьютерной томографии высокого разрешения (КТВР), когда ОФВ 1 может оставаться нормальным.
Для настоящего технико-экономического обоснования у пациентов с легким заболеванием легких мы предположили, что LCI может лучше выявлять улучшения после ингаляционных антибиотиков, чем FEV 1 . Когда планировалось исследование, AZLI еще не был стандартным лечением в нашем центре. На тот момент больных хроническим заболеванием Р . aeruginosa инфекция вдыхала тобрамицин или колистин в течение длительного времени. Мы провели пилотное исследование, сравнивающее AZLI со стандартными ингаляционными антибиотиками в небольшой группе пациентов с нормальным ОФВ 1 (≥75% от прогнозируемого нормального значения).
Методы
В этом одноцентровом, наблюдательном, открытом, технико-экономическом исследовании сравнивались две фазы лечения, каждая из которых состояла из 4-недельных циклов включения / выключения с помощью ингаляционных антибиотиков: Фаза 1, недели с 0 по 8: стандартный ингаляционный антибиотик (тобрамицин). / TOBI ® 300 мг / 5 мл два раза в день или TOBI Podhaler ® 112 мг два раза в день), и фаза 2, недели с 8 по 16: AZLI 75 мг три раза в день.ALZI был предоставлен компанией Gilead Sciences, производителем AZLI. Для каждого пациента исследование начиналось в конце 4-недельного перерыва без стандартного ингаляционного антибиотика («вымывание»). Период набора пациентов — с июня 2014 г. по январь 2016 г.
Основными критериями включения были: клинически стабильные пациенты в возрасте ≥12 лет с МВ, ОФВ 1 ≥75% от прогнозируемого нормального значения, хронические P . aeruginosa легочная инфекция [8], и, по крайней мере, два предыдущих цикла включения / выключения или> 8 недель непрерывного лечения ингаляционными антибиотиками с тобрамицином.Основными критериями исключения были возраст ≥ 50 лет, острые инфекции верхних или нижних дыхательных путей или легочные обострения.
Первичной конечной точкой был индекс клиренса легких (LCI), измеренный путем вымывания нескольких вдохов азота с использованием 100% кислорода (EasyOne Pro ® LAB MBW Module, ndd Medical Technologies, Цюрих, Швейцария) с верхним пределом нормы 7,0 [9 ]. Тестирование MBW и спирометрия проводились перед сеансом стандартной физиотерапии. Вторичными конечными точками были пребронходилататор FEV 1 с использованием эталонных значений из Глобальной инициативы по легким (GLI) [10].Респираторные симптомы определялись с помощью опросника по муковисцидозу — пересмотренной шкалы респираторных симптомов [11]. Нежелательные явления регистрировались при каждом посещении исследования.
При первоначальной разработке исследования мы выполнили расчет размера выборки. За пять лет работы с измерениями LCI мы наблюдали стандартное отклонение LCI 1,25 у относительно здоровых пациентов с МВ. Для настоящего исследования мы предположили, что ИМТ улучшится после приема AZLI, по крайней мере, на ту же величину, что и после гипертонического раствора [12], а возможно, и больше.Используя эти цифры, размер выборки из 10 имел 80% мощности для обнаружения разницы между средними значениями 0,85 с уровнем значимости (альфа) 0,05 (двусторонний) в парном t-тесте.
Данные выражены в виде медианы и диапазона, если не указано иное. Для каждого параметра были определены относительные изменения от начала до конца двух периодов лечения. Непараметрический знаковый ранговый критерий Вилкоксона использовался для сравнения относительных изменений во время фазы AZLI и стандартной фазы лечения. Протокол исследования (протокол S1) был одобрен этическим комитетом Медицинского университета Инсбрука (номер ЕС: UN 2013–0014_LEK Sitzungsnummer: 330/2.5), номер EudraCT: 2013-004295-35, отклонений от этого протокола исследования (протокол S1) не было. Письменное информированное согласие было получено от всех отдельных участников, включенных в исследование.
Результаты
Всего обратились к 12 пациентам, у трех пациентов было слишком мало времени для участия в исследовании из-за большой рабочей нагрузки, и один субъект не соответствовал критериям включения. В исследовании приняли участие восемь пациентов с МВ в возрасте от 15 до 49 лет (в среднем 28 лет) (рис. 1). Они были хронически инфицированы P . aeruginosa в течение 6,5 лет и получал ингаляционные антипсевдомонадные антибиотики в течение 4,2 года. ОФВ 1 находился в диапазоне от 76,3 до 123,8% от прогнозируемого (медиана 87,0%), а z-показатель ОФВ 1 GLI от -2,20 до 2,04 (медиана -1,24). Средний индекс массы тела был нормальным (21,5 кг / м 2 ), а средняя шкала респираторных симптомов CFQ-R 83,3 (диапазон от 78 до 94) показала лишь несколько ограничений. Несмотря на почти нормальную спирометрию, средний индекс клиренса легких 8,59 (диапазон от 6,4 до 11,4) был выше верхней границы нормы (7.0), и только два пациента показали нормальные значения в начале исследования. Стандартным ингаляционным антибиотиком был тобрамицин для всех субъектов, при этом n = 5 субъектов использовали TOBI Podhaler ® 112 мг BID и n = 3 пациента вдыхали TOBI ® 300 мг / 5 мл раствора небулайзера BID. Поскольку предыдущие авторы сообщили о сопоставимых профилях безопасности и эффективности двух препаратов тобрамицина [13,14], мы проанализировали комбинированные результаты обоих препаратов.
После 4 недель лечения AZLI первичная конечная точка LCI улучшилась (т.е. снизилась) у 7 из 8 пациентов, в то время как только 4 из 8 пациентов показали лучшие результаты после ингаляции тобрамицина (рис. 2).
Ответы на лечение, определенные с помощью LCI, были более благоприятными после AZLI, чем после тобрамицина (-0,365 против +0,120, p = 0,039, рис. 3).
Напротив, не наблюдалось статистически значимых различий между AZLI и стандартным лечением с ОФВ 1 в качестве конечной точки (ОФВ 1 z-балл: +0,05 против -0,15, p = 0,195; ОФВ 1 % прогноз: + 0.50 против -1,80, p = 0,195), таблицы S1 и S2.
Респираторные симптомы показали клинически важные улучшения после лечения AZLI (медиана изменения +8,5) и лучшие результаты (p = 0,031), чем после лечения тобрамицином (медиана -3,0). Лечение хорошо переносилось, о побочных эффектах не сообщалось.
Обсуждение
В небольшой группе пациентов с муковисцидозом и легкой болезнью легких после 4-недельного курса AZLI наблюдалось большее улучшение индекса клиренса легких и респираторных симптомов по сравнению со стандартным ингаляционным антибиотиком тобрамицином.Напротив, ОФВ 1 не обнаружил значительных различий между двумя периодами лечения. Результаты этого небольшого технико-экономического обоснования согласуются с предыдущими выводами о том, что использование ОФВ -1 в качестве критерия исхода требует больших групп пациентов с преимущественно умеренным и тяжелым заболеванием легких и большим потенциалом для улучшения [15–18].
Это первое сравнение ингаляций AZLI и тобрамицина у пациентов с легкими заболеваниями легкой степени, на что указывает ОФВ 1 > 75% от прогнозируемого нормального значения.О превосходстве AZLI над тобрамицином пока сообщалось только у пациентов с более поздними стадиями заболевания легких. После 4 недель ингаляции AZLI наблюдалось среднее относительное улучшение на 8,4% от исходного уровня ОФВ 1 % от прогнозируемого, в то время как изменения после приема тобрамицина (+ 0,6% от исходного уровня) были значительно меньше [19]. В нескольких исследованиях с участием относительно здоровых пациентов с легкими заболеваниями легких АЗЛИ сравнивали с плацебо. У 76 пациентов с легким заболеванием легкой степени ОФВ 1 значительно улучшился после приема АЗЛИ только у пациентов с исходным ОФВ 1 <90% от прогнозируемого [20].Кроме того, исследование фазы 2 AZLI не показало большего улучшения ОФВ 1 после 14 дней лечения AZLI по сравнению с плацебо в подгруппе из 32 пациентов с прогнозируемым ОФВ 1 > 75% [1]. Таким образом, исследователи не смогли показать большего улучшения функции легких после приема AZLI по сравнению с ингаляцией тобрамицина у пациентов с легкой степенью поражения, когда ОФВ -1 использовался в качестве первичного параметра исхода [20].
У исследования было несколько ограничений. Во-первых, когорта пациентов в этом одноцентровом исследовании была небольшой по сравнению с международными многоцентровыми базовыми исследованиями.Во-вторых, мы не смогли набрать желаемое количество из 10 пациентов в разумные сроки. Это ограничивает возможности исследования.
До сих пор не определено минимальное клинически важное различие для LCI [18]. Комитеты экспертов заявили, что LCI является ценным параметром потенциального результата у пациентов с нормальным FEV 1 , поскольку LCI может обнаруживать различия в лечении даже в небольших группах пациентов [15,17].
Результаты этого технико-экономического обоснования согласуются с приведенными выше утверждениями и предполагают, что LCI следует рассматривать как клиническую конечную точку для испытаний у пациентов с ранними заболеваниями легких.
Благодарности
Мы благодарим Йоханнеса Эдера, доктора медицины, и Катарину Нидермайр, доктора медицины, за мониторинг сбора данных и помощь в уходе за пациентами.
Катарина Шюллер (STAT-UP – Statistical Consulting & Data Service GmbH, Мюнхен) предоставила статистические консультации.
Мы благодарим пациентов и их семьи.
Ссылки
- 1. Retsch-Bogart GZ, Burns JL, Otto KL, Liou TG, McCoy K, Oermann C et al.(2008) Исследование фазы 2 азтреонам лизина для ингаляции для лечения пациентов с муковисцидозом и инфекцией Pseudomonas aeruginosa. Детская пульмонология 43 (1): 47–58. pmid: 18041081
- 2. Retsch-Bogart GZ, Quittner AL, Gibson RL, Oermann CM, McCoy KS, Montgomery AB et al. (2009) Эффективность и безопасность ингаляционного азтреонам-лизина для лечения псевдомонад дыхательных путей при муковисцидозе. Сундук 135 (5): 1223–1232. pmid: 19420195
- 3. Hutchinson D, Barclay M, Prescott WA, Brown J (2013) Вдыхал азтреонам лизин.Обзор, основанный на фактах. Мнение экспертов по фармакотерапии 14 (15): 2115–2124. pmid: 23992352
- 4. О’Нил К., Танни М.М., Джонстон Э., Роуэн С., Дауни Д.Г., Рендалл Дж. И др. (2016) Индекс клиренса легких у взрослых и детей с муковисцидозом. Грудь.
- 5. Амин Р., Суббарао П., Джабар А., Балковец С., Дженсен Р., Керриган и др. (2010) Гипертонический раствор улучшает ИЖК у педиатрических пациентов с МВ с нормальной функцией легких. Грудь 65 (5): 379–383. pmid: 20435858
- 6.Амин Р., Суббарао П., Лу В., Джабар А., Балковец С., Дженсен Р. и др. (2010) Влияние дорназы альфа на неоднородность вентиляции у пациентов с муковисцидозом. Eur Respir J.
- 7. Ellemunter H, Fuchs SI, Unsinn KM, Freund MC, Waltner-Romen M, Steinkamp G et al. (2010) Чувствительность индекса клиренса легких и компьютерной томографии грудной клетки на ранних стадиях заболевания легких. Respir Med 104 (12): 1834–1842. pmid: 20637585
- 8. Ли Т.В., Браунли К.Г., Конвей С.П., Дентон М., Литтлвуд Дж. М. (2003) Оценка нового определения хронической инфекции Pseudomonas aeruginosa у пациентов с муковисцидозом.J Cyst.Fibros. 2 (1): 29–34. pmid: 15463843
- 9. Fuchs SI, Eder J, Ellemunter H, Gappa M (2009) Индекс клиренса легких: нормальные значения, повторяемость и воспроизводимость у здоровых детей и подростков. Педиатр Пульмонол 44 (12): 1180–1185. pmid: 190
- 10. Quanjer PH, Stanojevic S, Cole TJ, Baur X, Hall GL, Culver BH et al. (2012) Многоэтнические эталонные значения спирометрии для возрастного диапазона от 3 до 95 лет: уравнения глобальной функции легких 2012. Eur Respir J 40 (6): 1324–1343.pmid: 22743675
- 11. Schmidt A, Wenninger K, Niemann N, Wahn U, Staab D (2009) Качество жизни, связанное со здоровьем у детей с муковисцидозом: проверка немецкого CFQ-R. Health Qual.Life Outcomes. 7: 97. pmid: 19954541
- 12. Суббарао П., Станоевич С., Браун М., Йенсен Р., Розенфельд М., Дэвис и др. (2013) Индекс клиренса легких как показатель результатов клинических испытаний у детей раннего возраста с муковисцидозом. Пилотное исследование с использованием ингаляционного гипертонического раствора.Am J Respir Crit Care Med 188 (4): 456–460. pmid: 23742699
- 13. Konstan MW, Flume PA, Kappler M, Chiron R, Higgins M, Brockhaus F et al. (2011) Безопасность, эффективность и удобство ингаляционного порошка тобрамицина у пациентов с муковисцидозом. Судебный процесс EAGER. Журнал муковисцидоза: официальный журнал Европейского общества муковисцидоза 10 (1): 54–61.
- 14. Vandevanter DR, Geller DE (2011) Тобрамицин, вводимый TOBI ((R)) Podhaler ((R)) для людей с муковисцидозом.Обзор. Медицинские приборы (Окленд, Нью-Зе) 4: 179–188.
- 15. Kent L, Reix P, Innes JA, Zielen S, Le Bourgeois M, Braggion C et al. (2014) Индекс клиренса легких: доказательства для использования в клинических испытаниях при муковисцидозе. J Cyst Fibros 13 (2): 123–138. pmid: 24315208
- 16. Ratjen F, Sheridan H, Lee P, Song T, Stone A, Davies JC et al. (2011) Индекс клиренса легких как показатель результатов в клинических испытаниях муковисцидоза [Abstract 201]. Pediatr Pulmonol Suppl.
- 17. Суббарао П., Милла С., Аврора П., Дэвис Дж. К., Дэвис С. Д., Холл Г. Л. и др. (2015) Множественное дыхание как тест функции легких при муковисцидозе. Отчет о семинаре Фонда кистозного фиброза. Анналы Американского торакального общества 12 (6): 932–939. pmid: 26075554
- 18. Tiddens HAWM, Puderbach M, Venegas JG, Ratjen F, Donaldson SH, Davis SD et al. (2015) Новые критерии результатов клинических исследований муковисцидоза. Детская пульмонология 50 (3): 302–315.pmid: 25641878
- 19. Ассаэль Б.М., Пресслер Т., Билтон Д., Фейон М., Фишер Р., Хирон Р. и др. (2013) Ингаляционный азтреонам лизин по сравнению с ингаляционным тобрамицином при муковисцидозе. Сравнительное испытание эффективности. Журнал муковисцидоза: официальный журнал Европейского общества муковисцидоза 12 (2): 130–140.
- 20. Wainwright CE, Quittner AL, Geller DE, Nakamura C, Wooldridge JL, Gibson RL et al. (2011) Азтреонам для ингаляционного раствора (AZLI) у пациентов с муковисцидозом, легким поражением легких и P.
