Биологическая роль серы в организме
библиотека
материалов
Содержание слайдов
Номер слайда 1
Биологическая роль серы в организме человека
Номер слайда 3
По степени распространённости в природе соединения серы занимают 16-е место, в организме содержится около 0,25% минерала. Располагается в VI группе таблицы Менделеева. Ромбическая сера. Моноклинная сера
Располагается в VI группе таблицы Менделеева. Ромбическая сера. Моноклинная сера
Сера в организме
Номер слайда 5
Функции серы в организме
Стабилизирует структуру белка на молекулярном уровне – дисульфидный мостик.
Инсулин. Входит в состав инсулина, служит для нормализации уровня глюкозы в крови. Является составной частью различных ферментов,.
Номер слайда 8
«Минерал красоты»
Энергетический транспорт клетки
Номер слайда 10
Входит в состав витаминов группы B – биотина, тиамина, пантотеновой и липоевой кислоты.
Соединения серы – мощные антиоксиданты
Номер слайда 12
Выделение желчи
Коллаген
Номер слайда 14
Составная часть незаменимой аминокислоты метионина
Номер слайда 15
Передача генетической информации
Номер слайда 16
Номер слайда 17
Гепарин
Номер слайда 18
В чем заключается биологическая роль серы в организме человека? / Справочник :: Бингоскул
Сера – макроэлемент, который составляет 0,16% человеческого организма. Ее можно встретить в белках, гормонах, некоторых витаминах. Сера содержится в костях, нервах, волосах и др. В день взрослому человеку необходимо потреблять около 4 г серы. Источником этого макроэлемента могут быть растительные ткани.
Ее можно встретить в белках, гормонах, некоторых витаминах. Сера содержится в костях, нервах, волосах и др. В день взрослому человеку необходимо потреблять около 4 г серы. Источником этого макроэлемента могут быть растительные ткани.
Биологическая роль серы
Отдельные молекулы серы не приносят пользы живым организмам. Серу включают такие аминокислоты, как цистеин и метионин, которые выполняют ряд полезных функций:- с помощью дисульфидных мостиков придают нужную пространственную форму белкам;
- входят в состав инсулина и биотина;
- играют роль активного центра многих ферментов;
- помогают транспортировать энергию внутри клетки.
Биологическая роль серы в организме заключается в поддержании его нормальной жизнедеятельности. Человек может получать макроэлементы с помощью сбалансированного питания.
Чтобы восполнить недостаток серы, необязательно приобретать в аптеках специальные препараты. Для поддержания здорового образа жизни необходимо изменить рацион питания. Серу содержат многие продукты, такие как:
Серу содержат многие продукты, такие как:
- яйца;
- кунжут;
- курица;
- фасоль;
- крыжовник;
- капуста;
- молоко и др.
Чтобы сера хорошо усваивалась, недостаточно только употреблять продукты, содержащие этот макроэлемент. Фтор и железо подчеркивают полезные свойства серы, а мышьяк, свинец, молибден, барий, селен наоборот их гасят.
Значение серы в организме
Живым организмам может не хватать макроэлемента из-за нарушенного обмена веществ. Симптомами дефицита серы могут служить боли в суставах, тахикардия, аллергия, выпадение волос. Если не восполнять недостаток серы, то появляется риск нарушения метаболизма серосодержащих молекул.
Редко встречается избыток какого-либо макроэлемента. Перенасыщение организма серой ведет за собой негативные последствия:
- анемию;
- заболевания верхних дыхательных путей;
- «песок» в глазах;
- слабость;
- дефицит массы тела.
Во многих продуктах присутствуют добавки, которые человек ежедневно употребляет. Сульфиты – консерванты, которые, по мнению некоторых исследователей, приводят к бронхиальной астме. Для поддержания здорового образа жизни необходимо внимательно читать состав продуктов.
Сера может играть негативную роль в живых организмах. Например, сероводород токсичен. Им можно отравиться при выбросах веществ в воздух при авариях или пожарах на химических производствах.
В организме человека сера окисляется с образованием серной кислоты, которая обезвреживает яды в кишечнике. Этот макроэлемент также обладает противомикробным и противовоспалительным действием, поэтому часто используется в дерматологии при лечении прыщей и воспалений.
Чистая сера представляет собой порошок желтого цвета. У нее неприятный запах. Серу называют обязательным компонентом для здоровых волос, ногтей и кожи. В культурах некоторых народов считается, что именно серой пахнет в преисподней. В реальном мире серосодержащими веществами пахнут лук и чеснок.
характеристика элемента с фото и потребность в нем для организма
Сера, как микроэлемент, находится в пятерке самых необходимых биоэлементов, без участия которых невозможен ни один обмен веществ в организме. Она содержится в структуре аминокислот (метионин и цистин), витамина тиамина (В1) и в инсулине.
Она содержится в структуре аминокислот (метионин и цистин), витамина тиамина (В1) и в инсулине.
Сера – микроэлемент, постоянно присутствующий в организме. За свои качества сохранять женскую привлекательность получила название «минерал красоты».
Интересный факт: содержание серы в организме в пересчете на массу составляет 0,25%.
Действие серы и ее биологическая роль в организме человека
Действие серы на организм дало возможность назвать ее царицей микроэлементов, благодаря свойству притормаживать процессы старения, вырабатывать коллаген и кератин, и влиять на кровообращение.
Сера защищает органы и ткани от влияния радиации и прочих токсичных отходов в окружающей среде, что очень важно в условиях проживания и работы в больших промышленных городах, переполненных техникой и электроприборами.
Такие важные составляющие показателя женской привлекательности, как волосы, кожа и ногти, поддерживают свое здоровье, в основном, благодаря присутствию серы. Также она находится в структуре пигмента меланина, который придает коже ровный загар.
Кроме того сера имеет очень важную биологическую роль для организма, участвуя во многих процессах:
- оказывает защитное действие от микробов в крови, помогает нормализовать ее свертываемость;
- поддерживает нужный уровень желчи, необходимой для переваривания пищи;
- за счет содержания серы в гемоглобине, он способен транспортировать и насыщать кровь кислородом и соответственно обеспечивать организм энергией;
- является участником процесса строительства клеток организма, костной, хрящевой и нервной ткани;
- нормализует содержание сахара и выработку глюкозы в крови;
- оказывает заживляющий эффект на раны и снимает воспаления;
- значительно повышает иммунитет и способен действовать как антиаллерген.

Этот полезнейший микроэлемент поступает в организм в виде органических кислот и простых органических соединений. Сера имеет свойство проникать через кожные покровы, причем намного лучше, чем в кишечнике, потому что тут образуются соединения, которые имеют долгий период выведения. А в глубоких слоях эпидермиса, сера трансформируется в сульфаты и сульфиды, которые уже и поступают в кровь. Именно это свойство дает такой эффект для кожи.
Вот почему рекомендуются к посещению лечебные источники с высоким содержанием серы, т.к. из-за высокой концентрации сероводорода и сернистого газа в воздухе и воде, происходит более активное насыщение организма и кожи.
Самостоятельно этот уникальный микроэлемент организмом не синтезируется, получить его можно только извне.
Действие серы, как и многих других элементов и витаминов, зависит от пропорций с другими элементами. Так, помогут сере усваиваться фтор и железо, вот противниками считают такие элементы как мышьяк, свинец, селен, молибден и барий.
Суточная норма — какова потребность в элементе?
Суточная норма серы не определена с большой точностью и рекомендации колеблются от 4 до 12 грамм в день. Такое количество достаточно легко получить с едой, т.к. сера достаточно пропорционально распределена в употребляемых продуктах.В особую категорию, нуждающихся в повышении нормы, относят детей и спортсменов. Для спортсменов это легко сделать, т.к. их пища насыщена белками, которые содержат серу в большом количестве.
Недостаток (дефицит) серы в организме
Недостаток серы в организме по клиническим данным не приводит к серьезным нарушениям здоровья, но в ходе экспериментов на животных все-таки было замечено, что недостаток метионина (основного источника серы) может замедлить рост и снизить репродуктивность. Метионин участвует в синтезе многих соединений, следовательно, его недостаток и последствия можно соотнести с недостатком необходимого количества серы.
Основные признаки дефицита серы четко выражены и легко обнаруживаются:
- нездоровые, слабые и тусклые волосы;
- бледная, сухая кожа с нездоровым цветом, появление пигментных пятен;
- понижение репродуктивной функции;
- повышение содержания сахара и риск развития сахарного диабета;
- болезненное состояние суставов, проблемы с движением;
- тахикардия, гипертония;
- проблемы в функционировании печени, в особо тяжелых случаях – ее жировая дистрофия;
- нарушение «спокойствия» нервной системы, возникновение беспокойного состояния и раздражения.

Недостаток серы легко устраняется введением в пищу серосодержащих продуктов и минеральных веществ (биотин, тиамин).
Избыток серы и отравление нею — симптомы
Переизбыток серы в организме чаще всего вызванн употреблением в пищу продуктов, содержащих сульфиты, которые, в свою очередь, добавляют в качестве консервантов в безалкогольные напитки, копчености, красители. С этим явлением связывают участившиеся случаи заболевания бронхиальной астмой и других болезней органов дыхания.
Отравление серой может наступить в результате перенасыщения окружающей среды сероводородом, сероуглеродом или сернистым газом, например, из-за аварий на производствах, в результате химической реакции. Такие отравления очень опасны и чаще всего последствия необратимы. Интоксикация наступает моментально и выражается в таких признаках:
- судороги;
- остановка дыхания и потеря сознания;
- паралич;
- острая резь в глазах.
Через некоторое время, после снятия острой симптоматики, отравление может дать знать о себе головными болями, высыпаниями на коже, расстройствами нервной системы, органов дыхания и проблемами с желудком и пищеварением.
При наличии не критичного избытка сера симптомы не столь серьезны:
- зуд на коже, высыпания;
- краснота глаз, появление конъюнктивитов;
- ослабление слуха;
- заболевания органов дыхания, бронхит;
- расстройства пищеварения;
- анемия.
Сера, которая содержится в продуктах питания, таких токсичных отравлений не вызывает.
В каких пищевых источниках содержится?
Основными источниками серы для человека считают пищевые продукты органического происхождения – мясо, рыба, сыры, яйца, особенно перепелиные. Пополнить запасы серы реально с помощью овощей – капусты, бобовых, лука, чеснока, репы и пророщенных злаков.
Стоит не забывать, что потребность в сере увеличивается с возрастом и увеличивать дозу приема этого элемента.
Показания к назначению
Показания к назначению микроэлемента как лекарства следующие:
- защита организма от радио- и ионизирующего излучения;
- заболевания кожи — демодекоз, педикулез, лишай;
- снятие воспалений, борьба с паразитами, снятие аллергических проявлений;
- лечение вегето-сосудистой дистонии.

В фармакологии различают три формы, в которых выпускают серу:
- серный цвет – для наружного применения;
- очищенная сера в порошках для внутреннего употребления, как слабительного средства;
- серное молоко – употребляют внутрь для борьбы с паразитами.
Cуточная норма
Необходимая суточная норма: 500 — 3000 мг
Продукты содержащие сера
- Сыр прибалтийский
- Сыр литовский
- Сыр Голландский
- Сыр ярославский
- Сыр пошехонский
- Сыр угличский
- Сыр костромской
- Фарш из мяса индейки
|
В организмах животных и человека сера выполняет незаменимые функции: обеспечивает пространственную организацию молекул белков, необходимую для их функционирования, защищает клетки, ткани и пути биохимического синтеза от окисления, а весь организм – от токсического действия чужеродных веществ.
Суточная потребность организма человека – 0,5–3 г (по другим данным – 4–5 г).
Сера поступает в организм с пищевыми продуктами, в составе неорганических и органических соединений. Большая часть серы попадает в организм в составе аминокислот.
Содержание серы в теле взрослого человека – около 0,16% (110 г на 70 кг массы тела). Сера содержится во всех тканях человеческого организма, особенно много ее в мышцах, скелете, печени, нервной ткани, крови. Также богаты серой поверхностные слои кожи, где сера входит в состав кератина и меланина.
Сера выделяется преимущественно с мочой в виде нейтральной серы и неорганических сульфатов, меньшая часть серы выводится через кожу и легкие, а выводится в основном с мочой в виде SO42–.
Биологическая роль в организме человека. В организме человека сера – непременная составная часть клеток, ферментов, гормонов, в частности инсулина, который вырабатывается поджелудочной железой, и серосодержащих аминокислот (метионина, цистеина, таурина и глутатиона).
Сера дезинфицирует кровь, повышает сопротивляемость организма бактериям и защищает протоплазму клеток, способствует осуществлению необходимых организму окислительных реакций, усиливает секрецию желчи, предохраняет от вредного воздействия токсичных веществ, защищает организм от вредного воздействия радиации и загрязнений окружающей среды, тем самым замедляя процессы старения. Этим объясняется высокая потребность организма в данном элементе.
Признаки недостаточности серы: запоры, аллергии, тусклость и выпадение волос, ломкость ногтей, повышенное артериальное давление, боли в суставах, тахикардия, высокий уровень сахара и высокий уровень триглицеридов в крови. В запущенных случаях – жировая дистрофия печени, кровоизлияния в почки, нарушения белкового и углеводного обмена, перевозбуждение нервной системы, раздражительность.
В последние десятилетия одним из источников избыточного поступления серы в организм человека стали серосодержащие соединения (сульфиты), которые добавляются во многие пищевые продукты, алкогольные и безалкогольные напитки в качестве консервантов. Особенно много сульфитов в копченостях, картофеле, свежих овощах, пиве, сидре, готовых салатах, уксусе, красителях вина. Возможно, потребление сульфитов, которое постоянно увеличивается, частично виновно в росте заболеваемости бронхиальной астмой. Известно, например, что 10% больных бронхиальной астмой проявляют повышенную чувствительность к сульфитам (т.
Основные проявления избытка серы в организме: зуд, сыпь, фурункулез, покраснение и опухание конъюнктивы; появление мелких точечных дефектов на роговице; ломота в бровях и глазных яблоках, ощущение песка в глазах; светобоязнь, слезотечение, общая слабость, головные боли, головокружение, тошнота, катар верхних дыхательных путей, бронхит; ослабление слуха, расстройства пищеварения, поносы, снижение массы тела; анемия, психические нарушения, снижение интеллекта.
Сера необходима: при туберкулезе легких, суставном ревматизме, воспалениях, изжоге, артритах, рините, проблемах с волосами (когда количество креатина в них ниже нормы), болях в суставах, паразитарной инфекции, синдроме раздраженного кишечника, запястном сухожильном синдроме (профессиональное заболевание компьютерщиков), а также болезнях кожи и ногтей.
|
6. РОЛЬ СЕРЫ В ОРГАНИЗМЕ ЧЕЛОВЕКА. Биогенные элементы в организме человека
Похожие главы из других работ:
Биогенные элементы в организме человека
1. Содержание и биологическая роль химических элементов в организме человека
В человеческом организме непрерывно образуются невообразимое множество различных химических соединений…
Биогенные элементы в организме человека
2. РОЛЬ КИСЛОРОДА В ОРГАНИЗМЕ ЧЕЛОВЕКА
Содержание кислорода в организме взрослого человека составляет около 62% от общей массы тела (43 кг на 70 кг массы тела). Главной функцией молекулярного кислорода в организме является окисление различных соединений…
Биогенные элементы в организме человека
3. РОЛЬ УГЛЕРОДА В ОРГАНИЗМЕ ЧЕЛОВЕКА
УГЛЕРОД — важнейший биогенный элемент, составляющий основу жизни на Земле, структурная единица огромного числа органических соединений, участвующих в построении организмов и обеспечении их жизнедеятельности (биополимеры. ..
..
Биогенные элементы в организме человека
4. РОЛЬ ВОДОРОДА В ОРГАНИЗМЕ ЧЕЛОВЕКА
Вода важнейшее соединение водорода в живом организме. Основные функции воды следующие: 1. Вода, обладающая высокой удельной теплоемкостью, обеспечивает поддержание постоянства температуры тела…
Биогенные элементы в организме человека
5. РОЛЬ КАЛИЯ В ОРГАНИЗМЕ ЧЕЛОВЕКА
Калий — обязательный участник многих обменных процессов. Важное значение имеет калий в поддержании автоматизма сокращения сердечной мышцы — миокарда; обеспечивает выведение ионов натрия из клеток и замену их ионами калия…
Биогенные элементы в организме человека
7. РОЛЬ КАЛЬЦИЯ В ОРГАНИЗМЕ ЧЕЛОВЕКА
Кальций непосредственно участвует в самых сложных процессах, например, таких…
Биологическая роль йода
3. Биологическая роль в организме (нормы содержания в биологических объектах)
Рассмотрим более подробно, как, где и в каких количествах накапливается йод в нашем организме, как он перераспределяется и от чего зависит накопление этого элемента. Всего в организме человека содержится от 20 до 35 мг йода…
Всего в организме человека содержится от 20 до 35 мг йода…
Конкурс «Машина времени». Проект «Исполняющие обязанности»
Варианты замены серы.
Селен — химический элемент главной подгруппы VI группы, 4-го периода в периодической системе, имеет атомный номер 34, обозначается символом Se (лат. Selenium). Входит в состав активных центров некоторых белков в форме аминокислоты селеноцистеина…
Медико-биологическое значение соединений селена
1. Биологическая роль химических элементов в организме
Биологическая роль химических элементов в организме человека чрезвычайно разнообразна. Главная функция макроэлементов состоит в построении тканей, поддержании постоянства осмотического давления, ионного и кислотно-основного состава…
Наркотические и психотропные вещества
1.5.2 В организме человека
Выявление героина в организме человека основывается на двух основных принципах: обнаружение непосредственно действующего вещества, или обнаружение его метаболитов. Согласно приказу Минздравсоцразвития России № 40 от 27.01.2006 г…
Согласно приказу Минздравсоцразвития России № 40 от 27.01.2006 г…
Производство серной кислоты
Производство серной кислоты из серы
Технологический процесс производства серной кислоты из элементарной серы контактным способом отличается от процесса производства из колчедана рядом особенностей [1]: особая конструкция печей для получения печного газа; повышенное…
Производство серной кислоты при повышенном давлении
2.2 Материальный баланс для печи сжигания серы
По условиям задания сера сгорает полностью (100%). S + O2 = SO2 Также учтём ранее вычисленные значения для кислорода и азота: Приход Расход Статья прихода кг/ч % масс. % об. Статья расхода кг/ч % масс. м3/ч % об. Сера 16444…
Разработка технологии получения серной кислоты обжигом серного колчедана
1.5.4 Производство серной кислоты из серы
Производство серной кислоты из серы по методу двойного контактирования и двойной абсорбции состоит из следующих стадий (см. рисунок 1.4). Воздух после очистки от пыли подается газодувкой в сушильную башню…
рисунок 1.4). Воздух после очистки от пыли подается газодувкой в сушильную башню…
Реакторы процесса получения элементарной серы
3. Физико-химические свойства серы
Сера (лат. Sulfur) является широко распространенным элементом и составляет 0,05% от массы земной коры. Данный элемент относится к главной подгруппе 6-ой группы периодической системы элементов Д.И. Менделеева, в третьем периоде. Порядковый номер 16…
Синтез оксида серы VI
Синтез оксида серы VI
Оксид серы (VI) SО3) (cемрный ангидримд, треомкись cемры) SO3 — в обычных условиях легколетучая бесцветная жидкость с удушающим запахом. Температура плавления 16,9 °C, кипения 45 °C. При температурах ниже 16…
Роль серы и минеральных веществ в питании животных
Оценка питательности кормов
Корм для животных должен быть полноценным – содержать необходимые питательные вещества для правильного роста и развития, обеспечивать нормальное отправление физиологических функций организма.
Корм считается питательным, если он удовлетворяет природные потребности животного в пище. Согласно исследованиям ученых, оценка питательности корма включает следующие данные:
- Энергетическая, общая питательность.
- Количество калорий, химический состав.
- Перевариваемость веществ, входящих в состав корма.
- Содержание витаминов, минералов, протеинов.
Насколько эффективен корм для животного, можно узнать по его физиологическому состоянию в период кормления.
Для оценки питательности нужно знать химический состав корма и процессы, которые происходят во время превращения питательных веществ в продукт животноводства.
В процессе переваривания корма усваивается только часть полезных веществ, не все вещества усваиваются организмом одинаково. К примеру, в ячменных зернах и пшеничных отрубях содержится практически одинаковое количество питательных веществ, но продуктивное действие ячменя примерно на 25% выше.
Часть веществ, которая считается перевариваемой, разрушается микрофлорой. Образуются органические кислоты, метан, углекислота, другая часть питательных веществ выводится с мочой. Поэтому для объективной оценки питательности корма и рациона следует знать, какая часть полезных веществ, содержащихся в корме, усваивается и становится составной частью тела животного.
Образуются органические кислоты, метан, углекислота, другая часть питательных веществ выводится с мочой. Поэтому для объективной оценки питательности корма и рациона следует знать, какая часть полезных веществ, содержащихся в корме, усваивается и становится составной частью тела животного.
Эффективность корма оценивается как по перевариваемым питательным веществам, так и по общей калорийности.
Роль серы для нормальной жизнедеятельности организма
Для организма животных сера – необходимый компонент. Большая ее часть сосредоточивается в коже, шерсти, роговом башмаке. Серу содержат тиамин и инсулин, она входит в состав белков и аминокислот.
Большее количество серы содержат корма, богатые белком – бобовые, зерновые, люцерн, луговое сено. Если в организме животного недостаточно серы, это выражается в потере аппетита, тусклом взгляде, выпадении шерсти.
Овцам и скоту необходимо в сутки 0,25-0,4% сухого вещества в кормовом рационе. Телятам до полугода нужно 3-10 г серы в сутки, дойной корове – 25-50 г, молодняку в зависимости от массы – 13-25 г.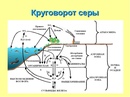 Ягнятам – 2-3 г в сутки, овцам – 3-9 г.
Ягнятам – 2-3 г в сутки, овцам – 3-9 г.
Сера действует в организме посредством белковых аминокислот, составной частью которых она является – тиамина, цистина, таурина, метионина, глутатиона.
Цистин – сильный антиоксидант, необходимый для работы печени. Усиливает проходящие в организме окислительные процессы, укрепляет соединительные ткани, уменьшает боли при воспалениях, способствует заживлению, стимулирует деятельность белых кровяных телец.
Тиамин защищает от химических токсинов, важен для состояния шерсти и кожи.
Метионин – незаменимая серосодержащая аминокислота, имеет большое значения для работы многих функций организма:
- работы нервной системы;
- выработки иммунных клеток;
- мощный антиоксидант, важен для работы печени;
- может снижать уровень холестерина, повышать уровень глютатиона;
- помогает в регенерации тканей почек, печени, выводит токсины;
- предотвращает кожные заболевания;
- эффективен при некоторых видах аллергии, так как уменьшает выделение гистамина.

Таурин — безопасная и полезная аминокислотная биодобавка, оказывающая благоприятное воздействие на работу сердечнососудистой системы, полезен при сердечных заболеваниях и болезнях глаз. Присутствует в ЦНС, сердечной мышце, сетчатке глаза, мышцах скелета.
- помогает в стабилизации клеточных мембран;
- поглощении, уничтожении жиров;
- участвует в выработке нервных импульсов.
Глутатион представляет собой смесь аминокислотных цепочек, присутствует во всех клетках животных и растений, образует ферменты. Содержится в составе добавок, которые способствуют удалению токсинов.
Тиамин (В1). Синонимы: бетаксин, бевемин, аневрил, оризанин.
Тиамин – регулятор функции нервной системы и деятельности сердца, участвует в углеводном обмене. Применяется для ускорения роста птиц, животных, при лечении полиневрита.
Этот витамин необходим всем животным. Животные, которым недостает тиамина, нередко болеют полиневритом.
Цыплятам на 1 кг корма требуется 1 мг тиамина, свиньям – 3 мг. Для лечения доза увеличивается в 3-8 раз и более.
Для лечения доза увеличивается в 3-8 раз и более.
Для подкожного и внутримышечного введения:
- Крупный рогатый скот, лошади – 0,1-0,3 г
- Свиньи, мелкий рогатый скот – 0,005-0,06 г
- Телята – 0,01-0,06 г
- Собаки – 0,001-001 г
- Гуси, куры – 10-25 мг
- Цыплята – 1-2 мг цыпленку в сутки
Внутрь:
- Поросята – 25-40 мг
- Цыплята – 3-4 мг
Обогащение рациона животных серой
Обогащенный серой рацион требуется овцам для интенсивного роста шерсти, птицам во время линьки, крупному рогатому скоту и овцам в случае применения синтетических добавок.
Добавлять в рацион жвачных животных серу нужно при кормлении сорго, льняным жмыхом, рапсом.
Соотношение азота к сере в этом случае – 10:1, в обычном рационе – 15-20:1.
Чтобы рацион был сбалансированным, используется метионин, элементарная сера, тиосульфат натрия и глауберова соль.
Элементарная сера, которая в животноводстве применяется наиболее часто, должна содержать 99,5% серы.
Тиосульфат (гипосульфат) натрия содержит 22% серы и 16% натрия. Используется в приготовлении йодированной соли. Добавка используется как антитоксин, эффективна при отравлениях животных свинцом, ртутью, мышьяком.
Наилучшим образом сера усваивается из метионина.
Жвачными лучше усваиваются неорганические серные соединения, чем элементарная сера. Количество минеральной добавки, необходимой животному, определяется потребностью в минеральных веществах и их содержанием в корме.
Важно учитывать, какова максимально допустимая норма добавки в рационе конкретной группы животных с учетом возраста.
Использование таких неорганических соединений, как глауберова соль, сульфат аммония, поможет восполнить дефицит серы в рационе. Овцам шерстного направления, крупному рогатому скоту во время откорма можно давать глауберову соль из расчета 3-4 г на кормовую единицу рациона.
Как влияет сера на мех и шерстный покров животных
Сера в рационе улучшает качество меха у лис, норок. Козам и овцам также нужны серные добавки, которые обеспечивают нормальный обмен веществ и рост животных.
Козам и овцам также нужны серные добавки, которые обеспечивают нормальный обмен веществ и рост животных.
Хотя стоят аминокислоты недешево, лучше использовать их в качестве кормовых добавок, так как они напрямую влияют на качество, а значит, и цену меха.
В большинстве видов сорго присутствует цианистый гликозид, поэтому при использовании кормов с содержанием сорго животным нужно давать серу для нейтрализации его токсичного действия. Цианиды содержатся и в злаках.
Если растения выращены на почвах, бедных серой, содержание серы в них невысокое. В сорго, сочные корма, силос можно добавлять сульфат аммония, натрия, кальция, L-, D-метионин.
Такое заболевание, как слюнотечение, нередко связано с недостатком серы и других необходимых минералов – калия, натрия, магния. Недостаток серы в организме животных может вызвать истощение, слабость, анорексию, привести к смерти. При постоянном недостатке этого микроэлемента изменяется состояние микрофлоры кишечника, у животного может ухудшиться аппетит, усвоение пищи. Для здоровья животных и красоты шерстного покрова сера в рационе необходима.
Для здоровья животных и красоты шерстного покрова сера в рационе необходима.
Биогенная роль серы Сера n
Биогенная роль серы
Сера n Се ра — элемент 6 -й группы, третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 16. Проявляет неметаллические свойства. Обозначается символом S. В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде.
n Сера является структурным макроэлементом, ее содержание в организме взрослого человека составляет около 140 г. Сера в значительных количествах также находится и в растениях, где она содержится виде неорганических и органических соединений (содержащие серу гликозиды, аминокислоты и пр. ).
Сера в виде отдельного элемента не обладает биологическим значением. Ее биологическая роль состоит в том, что она входит в структуру таких аминокислот, как цистеин и метионин, которые и выполняют в животных организмах (в том числе у человека), ряд незаменимых функций: n придает необходимую для их функционирования пространственную организацию молекулам белков за счет образования дисульфидных мостиков n является компонентом многих ферментов, гормонов (в частности в инсулина), и серосодержащих аминокислот n является компонентом таких активных веществ, как гистамин, витамина биотин, витаминоида липоевой кислоты и др.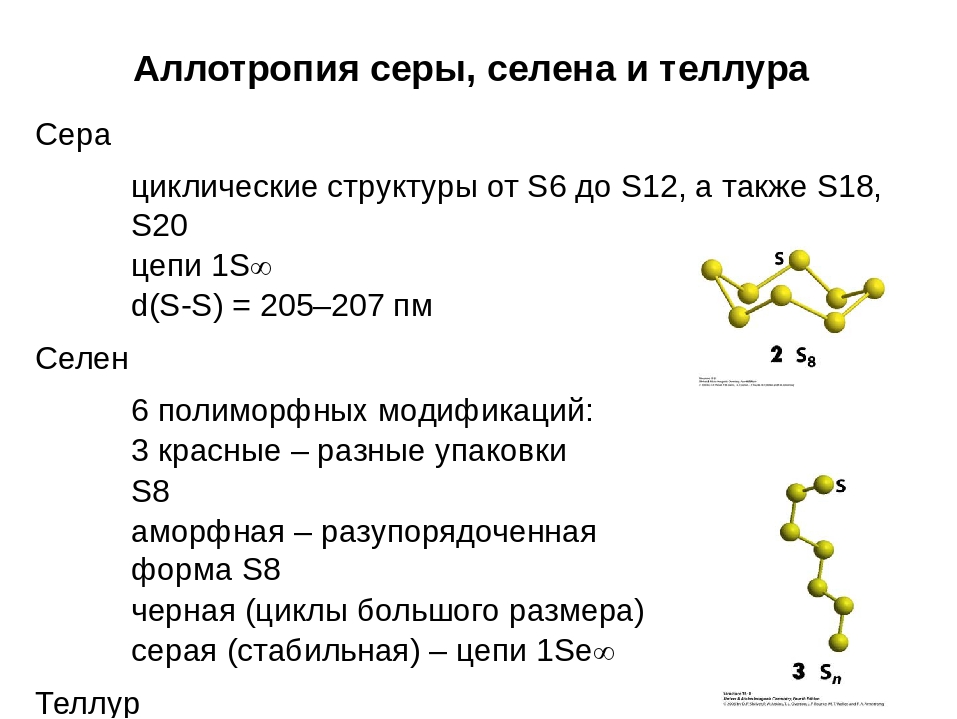 n обеспечивает передачу энергии в клетке: атом серы принимает на свободную орбиталь один из электронов кислорода n участвует в переносе метильных групп n входит в состав коэнзимов, включая коэнзим А
n обеспечивает передачу энергии в клетке: атом серы принимает на свободную орбиталь один из электронов кислорода n участвует в переносе метильных групп n входит в состав коэнзимов, включая коэнзим А
n Наиболее важными источниками серы являются: яйцо, кунжут, соя, курица, тунец, ростки пшеницы, овес, орехи, кукуруза, фасоль, капуста, чечевица, нежирная говядина, молоко, рыба, моллюски, сыры, гречневая крупа, хлебобулочные изделия.
Дефицит серы n n n Причины дефицита серы нарушение обмена Возможные последствия дефицита серы: Клинические описания специфических расстройств, вызванных недостатком серы в рационе, отсутствуют. патологии печени, суставов, кожи нарушения метаболизма серосодержащих соединений
Избыток серы n n Некоторые соединения серы обладают высокой токсичностью – сероуглерод, сероводород, оксиды серы. Отравление этими веществами происходит в результате работы во вредных условиях труда, пожаров на химических складах, неблагоприятных условиях окружающей среды. Использование серосодержащих соединений (сульфитов) в качестве консервантов в пищевых продуктах является одной из возможных причин избыточного поступления серы в организм человека. Некоторые исследователи считают, что увеличение поступления в организм сульфитов отвечает за повышение заболеваемости бронхиальной астмой. Для профилактики отрицательного влияния сульфитов рекомендуется увеличить в рационе содержание сыра, яиц, жирного мяса, птицы.
Использование серосодержащих соединений (сульфитов) в качестве консервантов в пищевых продуктах является одной из возможных причин избыточного поступления серы в организм человека. Некоторые исследователи считают, что увеличение поступления в организм сульфитов отвечает за повышение заболеваемости бронхиальной астмой. Для профилактики отрицательного влияния сульфитов рекомендуется увеличить в рационе содержание сыра, яиц, жирного мяса, птицы.
n n n Причины избытка серы: чрезмерное поступление серы или ее соединений нарушение обмена Последствия избытка серы: анемия болезни верхних дыхательных путей, бронхит кожный зуд, фурункулез боли в глазах, ощущение «песка» в глазах, появление мелких дефектов на роговице, светобоязнь, слезотечение общая слабость головные боли, головокружение, снижение слуха, психические нарушения, понижение интеллекта расстройства пищеварения, тошнота снижение массы тела.
Суточная потребность в сере: n оценивается на уровне 4 -5 грамм (Необходима не сама сера, а ее соединения) n
n Выполнили студентки 1 курса направления Биология: Зубкова Е. и Мишина Е.
и Мишина Е.
WebElements Periodic Table »Сера» биологическая информация
Сера необходима для жизни. Он является второстепенным компонентом жиров, биологических жидкостей и минералов скелета. Сера является ключевым компонентом большинства белков, поскольку она содержится в аминокислотах метионине и цистеине. Взаимодействия серы с серой важны для определения третичной структуры белка. Сероводород (H 2 S) заменяет H 2 O в фотосинтезе некоторых бактерий. У людей сероводород в очень малых концентрациях может метаболизироваться, но в более высоких концентрациях он быстро убивает, препятствуя дыханию.Он коварен в том смысле, что быстро притупляет обоняние, а это означает, что жертвы могут не знать о его присутствии. Он более токсичен, чем цианид. Примечательно, что серная кислота (H 2 SO 4 ) присутствует в пищеварительных жидкостях морских брызг (асцидий).
Уровни в организме человека
Обилие элементов в организме человека.
Сколько серы в вашем теле? Узнай здесь.
Вы можете использовать эту форму, чтобы подсчитать, сколько серы содержится в вашем организме.Введите свой вес в килограммах или фунтах и нажмите кнопку «Рассчитать». Вы должны ввести число, а не текст! Элементы, для которых нет данных, всегда будут давать нулевое значение веса, независимо от того, что вы указали в поле веса.
Изображение, показывающее периодичность логарифма содержания химических элементов в виде тепловой карты на сетке периодической таблицы. Изображение, показывающее периодичность логарифма содержания химических элементов в виде городского пейзажа на сетке периодической таблицы.Опасности и риски
Опасности и риски, связанные с серой:
Элементарная сера относительно безвредна, но очень токсична для многих бактерий и грибков. Серная пыль раздражает глаза и веки.
С сероуглеродом, сероводородом и диоксидом серы следует обращаться крайне осторожно. Сероводород в очень малых концентрациях может подвергаться метаболизму, но в более высоких концентрациях он может быстро вызвать смерть от паралича дыхания. Коварен тем, что быстро притупляет обоняние и более токсичен, чем цианид.Диоксид серы является опасным компонентом загрязнения атмосферного воздуха и одним из факторов, вызывающих кислотные дожди.
Сероводород в очень малых концентрациях может подвергаться метаболизму, но в более высоких концентрациях он может быстро вызвать смерть от паралича дыхания. Коварен тем, что быстро притупляет обоняние и более токсичен, чем цианид.Диоксид серы является опасным компонентом загрязнения атмосферного воздуха и одним из факторов, вызывающих кислотные дожди.
Дисульфид углерода, CS 2 , является важным промышленным растворителем. С ним нужно обращаться осторожно, так как он ядовит. Легко всасывается через кожу и при вдыхании. Это вызывает проблемы с центральной нервной системой.
Список литературы
- J.E. Huheey, E.A. Кейтер и Р.Л.Кейтер в книге Неорганическая химия: принципы структуры и реакционной способности , 4-е издание, HarperCollins, Нью-Йорк, США, 1993.
- S. Budavari (Ed.) В The Merck Index , 11-е изд., Merck, США, 1989.
- Н.Н. Гринвуд и А. Эрншоу в Chemistry of the Elements , 2nd edition, Butterworth, UK, 1997.

(PDF) Клеточная биология серы и ее функции в растениях
Мейер А.Дж., Фрикер М.Д. (2002) Контроль обусловленного потребностями биосинтеза глутатиона в зеленых клетках суспензионной культуры арабидопсиса
. Plant Physiol 130: 1927–1937
Meyer AJ, Hell R (2005) Гомеостаз глутатиона и окислительно-восстановительная регуляция сульфгидрильными группами.
Photosynth Res 86: 435–457
Meyer AJ, Rausch T (2008) Биосинтез, компартментация и клеточные функции глутатиона
в растительных клетках. В: Hell R, Dahl C, Knaff DB, Leustek T (eds) Метаболизм серы в фототрофных организмах
. Springer, Dordrecht, Нидерланды, стр. 161–184
Meyer AJ, Brach T., Marty L, Kreye S, Rouhier N, Jacquot JP, Hell R (2007) Редокс-чувствительный GFP
в Arabidopsis thaliana является количественным биосенсором для окислительно-восстановительный потенциал клеточного окислительно-восстановительного буфера глутатиона
.Plant J 52: 973–986
Meyer Y, Siala W, Bashandy T. , Riondet C, Vignols F, Reichheld JP (2008) Глутаредоксины и
, Riondet C, Vignols F, Reichheld JP (2008) Глутаредоксины и
тиоредоксины в растениях. Biochim Biophys Acta 1783: 589–600
Мейерс Д.М., Ахмад С. (1991) Связь между активностью L-3-цианоаланинсинтазы и дифференциальной чувствительностью насекомых к цианиду
. Biochim Biophys Acta 1075: 195–197
Miller AJ, Shen Q, Xu G (2009) Автострады на заводе: транспортеры для азота, фосфора и серы и их правила
.Curr Opin Plant Biol 12: 284–290
Mugford SG, Yoshimoto N, Reichelt M, Wirtz M, Hill L, Mugford ST, Nakazato Y, Noji M,
Takahashi H, Kramell R, Gigolashvili T, Flugge UI, Wasternack C, Gershenzon J, Hell R,
Saito K, Kopriva S (2009) Нарушение аденозин-50-фосфосульфаткиназы в Arabidopsis
снижает уровни сульфатированных вторичных метаболитов. Plant Cell 21: 910–927
Mu
¨ntz K, Christov V, Saalbach G, Saalbach I, Waddell D., Pickardt T., Schieder O, Wustenhagen T
(1998) Генетическая инженерия для зернобобовых культур с высоким содержанием метионина. Nahrung 42: 125–127
Nahrung 42: 125–127
Nakayama M, Akashi T, Hase T (2000) Растительная сульфидредуктаза: молекулярная структура, каталитическая функция
и взаимодействие с ферредоксином. J Inorg Biochem 82: 27–32
Ndamukong I, Abdallat A, Thurow C, Fode B, Zander M, Weigel R, Gatz C (2007) SA-индуцибельный
Глутаредоксин Arabidopsis взаимодействует с факторами TGA и подавляет JA-чувствительный PDF1 .2
транскрипция. Plant J 50: 128–139
Никифорова В., Фрейтаг Дж., Кемпа С., Адамик М., Гессе Х., Хефген Р. (2003) Анализ транскриптома
истощения серы у Arabidopsis thaliana: переплетение биосинтетических путей обеспечивает специфичность ответа
.Plant J 33: 633–650
Никифорова В.Дж., Гакьер Б., Кемпа С., Адамик М., Виллмитцер Л., Гессе Х., Хефген Р. (2004)
На пути к анализу метаболизма питательных веществ в растениях: тематическое исследование системной биологии по сере
метаболизм. J Exp Bot 55: 1861–1870
Никифорова В. Дж., Копка Дж., Толстиков В., Файн О., Хопкинс Л., Хоуксфорд М.Дж., Гессе Х., Хефген Р.
Дж., Копка Дж., Толстиков В., Файн О., Хопкинс Л., Хоуксфорд М.Дж., Гессе Х., Хефген Р.
(2005) Системная перебалансировка метаболизма в ответ на лишение серы, как показано по
анализ метаболома растений арабидопсиса.Plant Physiol 138: 304–318
Noji M, Inoue K, Kimura N, Gouda A, Saito K (1998) Изоформ-зависимые различия в регуляции обратной связи
и субклеточная локализация серинацетилтрансферазы, участвующей в биосинтезе цистеина. Arabidopsis thaliana. J Biol Chem 273: 32739–32745
Ohkama-Ohtsu N, Kasajima I., Fujiwara T, Naito S (2004) Выделение и характеристика мутанта
Arabidopsis, который сверхаккумулирует O-ацетил-L-сер. Plant Physiol 136: 3209–3222
Ohkama-Ohtsu N, Zhao P, Xiang C, Oliver D (2007a) Конъюгаты глутатиона в вакуоли
расщепляются g-глутамилтранспептидазой GGT3 у Arabidopsis.Plant J 49: 878–888
Ohkama-Ohtsu N, Oikawa A, Zhao P, Xiang C, Saito K, Oliver DJ (2008) A g-глутамил
независимый от транспептидазы путь катаболизма глутатиона в глутамат через 5-оксопролин
в арабидопсисе. Физиология растений 148: 1603–1613
Физиология растений 148: 1603–1613
Окама-Оцу Н., Радван С., Петерсон А., Чжао П., Бадр А., Сян С., Оливер Д. (2007b) Характеристика —
Зависимость внеклеточных g-глутамил транспептидаз, GGT1 и GGT2 , у Arabidopsis.
Plant J 49: 865–877
Palmieri L, Arrigoni R, Blanco E, Carrari F, Zanor MI, Studart-Guimaraes C, Fernie AR,
Palmieri F (2006) Молекулярная идентификация трансаденозилметионина арабидопсиса —
носильщик.Анализ распределения органов, бактериальная экспрессия, восстановление в липосомы и функциональная характеристика
. Физиология растений 142: 855–865
Клеточная биология серы и ее функции в растениях 275
Метаболизм серы в растениях стимулируется фотодыханием
Хоуксфорд, М. Дж. И Де Кок, Л. Дж. Управление метаболизмом серы в растениях. Plant, Cell Environ. 29 , 382–395 (2006).
CAS Статья Google ученый

Стипанук, М. Х. Метаболизм серных аминокислот: пути производства и удаления гомоцистеина и цистеина. Annu. Rev. Nutr. 24 , 539–577 (2004).
CAS Статья Google ученый
Чжао, Ф. Дж., Хоуксфорд, М. Дж. И МакГрат, С. П. Ассимиляция серы и ее влияние на урожайность и качество пшеницы. J. Cereal Sci. 30 , 1–17 (1999).
CAS Статья Google ученый
Мессик Д., Фан М. и Де Брей К. Глобальная потребность в сере и серные удобрения. FAL — Agric Res 283 , 97–104 (2005).
CAS Google ученый
Brunold, C. et al. Влияние глюкозы на восстановление ассимиляционного сульфата в корнях Arabidopsis thaliana . J. Exp. Бот. 54 , 1701–1709 (2003).
Артикул Google ученый

Kopriva, S. et al. Взаимодействие ассимиляции сульфатов с углеродным и азотным обменом у Lemna minor . Plant Physiol. 130 , 1406–1413 (2002).
CAS Статья Google ученый
Kebeish, R. et al. Хлоропластический обходной респираторный анастомоз увеличивает фотосинтез и производство биомассы у Arabidopsis thaliana . Нат. Biotechnol. 25 , 593–601 (2007).
CAS Статья Google ученый
South, P. F., Cavanagh, A. P., Liu, H. W. & Ort, D. R. Синтетические пути метаболизма гликолята стимулируют рост сельскохозяйственных культур и урожайность на поле. Наука 363 , eaat9077 (2019).
Артикул Google ученый
Jia, Y. et al. Влияние повышенного содержания CO 2 на рост, фотосинтез, элементный состав, уровень антиоксидантов и концентрацию фитохелатина в Lolium mutiforum и Lolium perenne при стрессе Cd. J. Hazard. Матер. 180 , 384–394 (2010).
J. Hazard. Матер. 180 , 384–394 (2010).
CAS Статья Google ученый
Лоладзе И. Рост атмосферного CO 2 и питание человека: к глобально несбалансированной стехиометрии растений? Trends Ecol. Эволюция 17 , 457–461 (2002).
Артикул Google ученый
Лоладзе, И. Скрытый сдвиг ионома растений, подверженных повышенному воздействию CO 2 истощает минеральные вещества в основе питания человека. eLife 3 , e02245 (2014).
Артикул Google ученый
Пеньуэлас, Дж. И Матамала, Р. Изменения содержания N и S в листьях, плотности устьиц и удельной площади листьев у 14 видов растений за последние три столетия увеличения CO 2 . J. Exp. Бот. 41 , 1119–1124 (1990).
Артикул Google ученый

Агрен, Г. И. и Вей, М. Стехиометрия растений в различных масштабах: образцы концентрации элементов больше отражают окружающую среду, чем генотип. New Phytol. 194 , 944–952 (2012).
Артикул Google ученый
Högy, P. & Fangmeier, A. Влияние повышенного содержания CO в атмосфере 2 на качество зерна пшеницы. J. Cereal Sci. 48 , 580–591 (2008).
Артикул Google ученый
Högy, P. et al. Влияние повышенного содержания CO 2 на урожай зерна и качество пшеницы: результаты 3-летнего эксперимента по обогащению CO 2 на открытом воздухе. Plant Biol. 11 (s1), 60–69 (2009).
Артикул Google ученый
Badiani, M., D’annibale, A., Paolacci, A., Miglietta, F. & Raschi, A. Антиоксидантный статус листьев сои ( Glycine max ), выращенных в условиях естественного CO 2 обогащения в полевых условиях. Funct. Plant Biol. 20 , 275–284 (1993).
CAS Статья Google ученый
Schulte, M., Von Ballmoos, P., Rennenberg, H. & Herschbach, C. Постоянный рост Quercus ilex L. при естественном CO 2 источников способствует акклиматизации серы, азота и углеводов. метаболизм потомства до повышенного pCO 2 . Plant, Cell Environ. 25 , 1715–1727 (2002).
CAS Статья Google ученый
Чан, К. X., Вирц, М., Фуа, С. Ю., Эставилло, Г. М. и Погсон, Б. Дж. Балансирование метаболитов в засухе: головоломка ассимиляции серы. Trends Plant Sci. 18 , 18–29 (2013).
CAS Статья Google ученый
Douce, R., Bourguignon, J., Neuburger, M. & Rébeillé, F.Система глициндекарбоксилазы: увлекательный комплекс. Trends Plant Sci. 6 , 167–176 (2001).
CAS Статья Google ученый
Collakova, E. et al. Arabidopsis Деформилазы 10-формилтетрагидрофолата необходимы для фотодыхания. Растительная клетка 20 , 1818–1832 (2008).
CAS Статья Google ученый
Hanson, A. D. & Roje, S. Одноуглеродный метаболизм у высших растений. Annu. Rev. Plant Biol. 52 , 119–137 (2001).
CAS Статья Google ученый
Блум, А. Дж., Бургер, М., Асенсио, Дж. С. Р. и Кузинс, А. Б. Обогащение углекислым газом подавляет ассимиляцию нитратов в пшенице и Arabidopsis . Наука 328 , 899–903 (2010).
CAS Статья Google ученый
Рахмилевич, С., Казинс, А. Б. и Блум, А. Дж. Ассимиляция нитратов в побегах растений зависит от фотодыхания. Proc. Natl. Акад. Sci. США 101 , 11506–11510 (2004).
CAS Статья Google ученый
Noctor, G. et al. Синтез глутатиона в листьях трансгенного тополя, сверхэкспрессирующего гамма-глутамилцистеинсинтетазу. Plant Physiol. 112 , 1071–1078 (1996).
CAS Статья Google ученый
Buwalda, F., Stulen, I., De Kok, L. J. и Kuiper, P. J. C. Содержание цистеина, γ-глутамил-цистеина и глутатиона в листьях шпината под воздействием темноты и внесения избытка серы. II. Накопление глутатиона в отдельных листьях, подвергшихся воздействию h3S в отсутствие света, стимулируется подачей глицина на черешок. Physiologia Plant. 80 , 196–204 (1990).
CAS Статья Google ученый
Herschbach, C. et al. Изменения серного обмена листьев тополя серого ( Populus x canescens ) при солевом стрессе: метаболическая связь с фотодыханием. Tree Physiol. 30 , 1161–1173 (2010).
CAS Статья Google ученый
Scheibe, R. Малатные клапаны для балансировки клеточной энергии. Physiologia Plant. 120 , 21–26 (2004).
CAS Статья Google ученый
Новицкая, Л., Треванион, С. Дж., Дрисколл, С., Фойер, К. Х. и Ноктор, Г. Как фотодыхание влияет на содержание аминокислот в листьях? Двойной подход через моделирование и анализ метаболитов. Plant, Cell Environ. 25 , 821–835 (2002).
CAS Статья Google ученый
Kruse, J. et al. Повышенное значение pCO 2 способствует снижению содержания нитратов в корнях табака дикого типа ( Nicotiana tabacum cv. Gat.) И значительно изменяет N-метаболизм у трансформантов, лишенных функциональной нитратредуктазы в корнях. J. Exp. Бот. 53 , 2351–2367 (2002).
CAS Статья Google ученый
Герлих, С. К., Уокер, Б. Дж., Крюгер, С. и Коприва, С.Сульфатный обмен у видов C 4 Flaveria контролируется корнем и связан с биосинтезом серина. Plant Physiol. 178 , 565–582 (2018).
CAS Статья Google ученый
Хефген, Р. и Никифорова, В. Дж. Метаболомика, интегрированная с транскриптомикой: оценка реакции систем на стресс, вызванный дефицитом серы. Physiologia Plant. 132 , 190–198 (2008).
CAS Статья Google ученый
Herath, H. M. & Ormrod, D. P. Влияние температуры и серного питания на CO 2 компенсационные значения в ячмене, горохе и рапсе. Plant Physiol. 49 , 443–444 (1972).
CAS Статья Google ученый
Коприва, С. и Ренненберг, Х. Контроль ассимиляции сульфатов и синтеза глутатиона: взаимодействие с метаболизмом азота и углерода. J. Exp. Бот. 55 , 1831–1842 (2004).
CAS Статья Google ученый
Abadie, C., Blanchet, S., Carroll, A. & Tcherkez, G. Метаболомический анализ постфотосинтетических эффектов газообразного O 2 на первичный метаболизм в освещенных листьях. Funct. Plant Biol. 44 , 929–940 (2017).
CAS Статья Google ученый
Планше, Э., Лотье, Дж. И Лимами, А. М. Гипоксический респираторный метаболизм у растений: восстановление метаболизма азота и углерода. In Дыхание растений: метаболические потоки и баланс углерода Vol. 43 (ред. Черкез Г. и Гашгай Дж.). 209−226 (Спрингер, Нью-Йорк, 2017).
Tcherkez, G. et al. Краткосрочные эффекты CO 2 и O 2 на метаболизм цитрата в освещенных листьях. Plant, Cell Environ. 35 , 2208–2220 (2012).
CAS Статья Google ученый
Abadie, C., Boex-Fontvieille, E. R., Carroll, A. J. & Tcherkez, G. Стехиометрия фотодыхательного метаболизма in vivo. Нат. заводы 2 , 15220 (2016).
CAS Статья Google ученый
Lee, B., Koprivova, A. & Kopriva, S. Ключевой фермент ассимиляции сульфатов, аденозин-5′-фосфосульфатредуктаза, регулируется HY5 в Arabidopsis . Plant J. 67 , 1042–1054 (2011).
CAS Статья Google ученый
Давидян Дж. И Коприва С. Регулирование поглощения и ассимиляции сульфатов — то же самое или не то же самое? Мол. Завод 3 , 314–325 (2010).
CAS Статья Google ученый
Wirtz, M. et al. Митохондриальный комплекс цистеинсинтазы регулирует биосинтез O-ацетилсерина в растениях. J. Biol. Chem. 287 , 27941–27947 (2012).
CAS Статья Google ученый
Jobe, T. O. et al. Ингибирование обратной связи тиолами превосходит истощение глутатиона: скрининг на основе люциферазы выявляет дефицитные по глутатиону γ-ECS и мутанты глутатионсинтетазы, нарушенные в индуцированной кадмием ассимиляции сульфата. Plant J. 70 , 783–795 (2012).
CAS Статья Google ученый
Queval, G. et al. H 2 O 2 -активированная повышающая регуляция глутатиона в Arabidopsis включает индукцию генов, кодирующих ферменты, участвующие в синтезе цистеина в хлоропласте. Мол. Завод 2 , 344–356 (2009).
CAS Статья Google ученый
Leakey, A. D. B. et al. Геномная основа стимулирования дыхания у растений, растущих в условиях повышенного содержания углекислого газа. Proc. Natl. Акад. Sci. США 106 , 3597–3602 (2009).
CAS Статья Google ученый
Habash, D. Z. et al. Системные реакции на прогрессирующий водный стресс у твердых сортов пшеницы. PLoS ONE 9 , e108431 (2014).
Артикул Google ученый
Ядав А., Кэрролл А., Эставилло Г., Ребецке Г. и Погсон Б.Аминокислотные реакции в теплице позволяют прогнозировать засухоустойчивость пшеницы на основе урожайности поля. J. Exp. Бот. https://doi.org/10.1093/jxb/erz224 (2019).
Артикул Google ученый
Gerwick, B. & Black, C. Ассимиляция серы в C 4 заводах. Plant Physiol. 64 , 590–593 (1979).
CAS Статья Google ученый
Копривова А. и др. Ассимиляционная сульфатредукция в C 3 , C 3 -C 4 и C 4 видов Flaveria . Plant Physiol. 127 , 543–553 (2001).
CAS Статья Google ученый
Weckopp, S. C. & Kopriva, S. Необходимы ли изменения в пути ассимиляции сульфатов для эволюции фотосинтеза C 4 ? Перед. Plant Sci. 5 , 773–773 (2015).
Артикул Google ученый
Abadie, C., Bathellier, C. & Tcherkez, G. Распределение углерода по основным метаболитам в освещенных листьях не только пропорционально фотосинтезу, когда изменяются газовые условия (CO 2 и O 2 ). New Phytol. 218 , 94–106 (2018).
CAS Статья Google ученый
Cui, J., Abadie, C., Carroll, A., Lamade, E. & Tcherkez, G. Ответы на дефицит K и заболачивание взаимодействуют через дыхательный и азотный метаболизм. Plant, Cell Environ. 42 , 647–658 (2019).
CAS Статья Google ученый
Перейти к основному содержанию Поиск
Поиск
- Где угодно
Поиск Поиск
Расширенный поиск- Войти | регистр
- Подписка / продление
- Учреждения
- Индивидуальные подписки
- Индивидуальные продления
- Библиотекари
- Тарифы, заказы40 Пакет для Чикаго
- Полный цикл и охват содержимого
- Файлы KBART и RSS-каналы
- Разрешения и перепечатки
- Инициатива развивающихся стран Чикаго
- Даты отправки и претензии
- Часто задаваемые вопросы библиотекарей
- Агенты
- Тарифы, заказы, и платежи
- Полный пакет Chicago
- Полный охват и содержание
- Даты отправки и претензии
- Часто задаваемые вопросы агента
- Партнеры по издательству
- О нас
- Публикуйте у нас
- Недавно приобретенные журналы
- Издательская стоимость tners
- Новости прессы
- Подпишитесь на уведомления eTOC
- Пресс-релизы
- СМИ
- Книги издательства Чикагского университета
- Распределительный центр в Чикаго
- Чикагский университет
- Условия использования
- Заявление об издательской этике
- Уведомление о конфиденциальности
- Доступность Chicago Journals
- Доступность университета
- Следуйте за нами на facebook
- Следуйте за нами в Twitter
- Свяжитесь с нами
- Медиа и рекламные запросы
- Открытый доступ в Чикаго
- Следуйте за нами на facebook
- Следуйте за нами в Twitter
Достаточно ли мы получаем серы в нашем рационе? | Питание и обмен веществ
Из-за гораздо более значительных последствий метаболизма серы и той роли, которую этот элемент играет в синтезе очень большого числа ключевых промежуточных продуктов метаболизма, таких как глутатион, мы решили расширить этот обзор, включив в него более широкий круг вопросов. перекрывающихся метаболических путей, на которые может повлиять недостаточное или маргинальное потребление серы.Есть надежда, что такой обзор побудит к дальнейшим исследованиям в этой очень важной и часто игнорируемой области метаболизма. Это включает в себя возможность повлиять на возникновение и прогрессирование большого количества аномалий, представляющих воспалительные и дегенеративные изменения, а также те, которые связаны с нормальным старением и аспектами истощения большого количества патологий.
Серусодержащие метаболиты, ключевым показателем которых является глутатион, в своем функционировании сливаются со многими другими соединениями, которые играют важную роль в механизмах, которые вызывают огромный интерес как часть традиционной и дополнительной медицинской помощи.К ним относятся полиненасыщенные жирные кислоты n-3 и n-6, минералы, такие как селен, цинк, медь и магний, витамины E и C, антиоксиданты, такие как проантоцианидины и липоевая кислота, многие из которых участвуют в синтезе простагландинов и в антиоксидантном каскаде. Накапливается все больше и больше доказательств, и они сосредотачиваются на совместной роли глутатиона и других метаболитов серы в гомеостатическом контроле этих фундаментальных механизмов.
Метаболизм серосодержащих аминокислот
Метионин и цистеин необходимы для синтеза белка у простых млекопитающих и птиц [1].Для оптимального роста диета должна обеспечивать эти две аминокислоты или только метионин. Физиологические потребности в цистеине могут быть удовлетворены за счет пищевого цистеина или за счет избытка диетического метионина. Молярная эффективность транс-сульфирования, т. Е. Метиониновой серы, превращенной в цистеиновую серу, составляет 100%. Цистеин может снизить потребность в метионине с пищей, даже если цистеин не превращается в метионин в высших организмах, за счет экономии его использования для основных процессов. С точки зрения диеты, один только метионин способен обеспечить организм всей необходимой серой, за исключением двух серосодержащих витаминов, тиамина и биотина.
В 1989 году подкомитет Национального исследовательского совета Соединенных Штатов по пищевым продуктам и питанию опубликовал последний обновленный отчет о рекомендуемых диетических нормах (RDA) для белков и аминокислот (эти рекомендации основаны на исследованиях баланса азота, проведенных много лет назад [2– 4]. Рекомендуемая суточная норма метионина (в сочетании с цистеином) для взрослых составляет 14 мг / кг массы тела. Поэтому человеку весом 70 кг, независимо от возраста и пола, требуется около 1,1 г (0,9 моль) метионина / цистеина в день.Когда Роуз предложил эти количества, он предположил, что «безопасное потребление» должно быть вдвое больше, или 2,0 г / день, вероятно, признавая, что его исследования проводились на ограниченном количестве людей, обычно 3–6 для каждой аминокислоты.
Эти потребности человека в метионине и щадящие эффекты цистеина, определенные Роузом и др. У молодых здоровых добровольцев в 1955 году, все еще принимаются сегодня, несмотря на признаки того, что они могут не отражать универсальные ценности [5]. Таттл и др. [6], давая очищенные аминокислотные диеты, содержащие различные количества метионина, пожилым людям в больнице VA в Лос-Анджелесе / Калифорнийском университете в Лос-Анджелесе, установили значения, значительно превышающие те, которые ранее были установлены Роуз для молодых студентов колледжа.Всем им требовалось более 2,1 г / день, а некоторым субъектам требовалось до 3,0 г / день, чтобы поддерживать положительный азотный баланс. Хотя Fukagawa et al [7] не смогли подтвердить такие различия, используя окисление аминокислот, а скорее этот баланс азота в качестве критерия; они согласились, что необходимы дальнейшие исследования. Ни их подходы, основанные на производстве CO2, обогащенного изотопами, ни исследования азотного баланса не учитывают уникальную роль SAA (серосодержащих аминокислот) в обеспечении S для сульфатирования.Фуллер и Гарлик [8], подробно рассмотревшие этот вопрос, пришли к выводу, что потребности в аминокислотах как для мужчин, так и для женщин занижены.
В свете этих опасений, особенно в связи с уникальной ролью SAA в обеспечении сульфатов для синтеза GAG (гликозаминогликанов), представляется важным определить, удовлетворяются ли потребности в сере, в частности, в отношении GAG. и GSH (глутатион) в хрящах. Можно предсказать, что синтез ГАГ может не протекать хорошо при предельном потреблении, и что предпочтение будет отдаваться синтезу белков и основных промежуточных продуктов метаболизма, таких как КоА, SAM (S-аденозил-L-метионин), GSH и т. Д.в головном мозге и других основных органах. К сожалению, никаких исследований, посвященных этому очень важному вопросу, не проводилось.
Исследования на людях выполнить непросто, они дороги и зависят от многих факторов. По другим видам, по-видимому, больше информации, особенно по домашней птице или крупному рогатому скоту, где стимуляция роста представляет собой значительное экономическое преимущество. Следует отметить, что в рационы птицы всегда добавляется метионин / цистеин для ускорения роста [9, 10].
Факторы, которые могут снизить доступность метионина / цистеина
Сульфатирование является основным путем детоксикации фармакологических агентов печенью. Как уже упоминалось, некоторые препараты, которые играют ключевую роль в лечении аномалий хряща, такие как ацетаминофен, требуют сульфата для их выведения. Ацетаминофен назначают в больших дозах для облегчения боли, а на этикетке рекомендуются дозы до 4 г / день, но часто употребляется больше. Тридцать пять% выводится конъюгированным с сульфатом и 3% конъюгированным с цистеином [11].Остальная часть выводится конъюгированной с глюкуроновой кислотой, которая, кстати, также является одним из основных компонентов ГАГ.
Метионин или цистеин (0,5%), добавленные в рацион, могут преодолеть тяжелый дефицит метионина, вызванный у крыс добавлением 1% ацетаминофена (эквивалент дозы 4 г / день для человека) [12]. Интересно отметить, что D-, а также L-метионин могут восстанавливать рост, подразумевая, что истощение серы было первичным дефектом, а не одним, связанным с синтезом белка.
Наиболее важным является то, что концентрации активного сульфата в печени в форме PAPS (аденозин-3′-фосфат 5′-фосфосульфат), ключевого метаболического предшественника ГАГ, также были снижены и могут быть восстановлены до нормального уровня путем добавления метионина [13]. . Экскреция сульфата с мочой была снижена до 95% при кормлении крыс диетами с низким содержанием метионина, и наблюдалось 60% -ное снижение содержания метионина в печени [14]. В зависимости от степени истощения во время приема добавок может быть достигнуто восстановление нормальной экскреции сульфатов и уровней глутатиона в печени.Неорганический сульфат был не так эффективен в восстановлении уровней PAPS, как метионин (рис. 1).
Рисунок 1Упрощенная диаграмма, которая изображает взаимосвязь между SAA, синтезом GAG, хранением цистеина в виде глутатиона, синтезом белка и метаболизмом азота.
У крыс, подвергшихся недостаточному потреблению серы для изучения сульфатирования ацетаминофена с целью биодеградации, наблюдались изменения гомеостаза PAPS [15]. Одновременно эти животные выводили ацетаминофен из крови более медленными темпами и превращали его в токсичный промежуточный тиоэфир.Снижение сульфатирования, по-видимому, вызвано снижением доступности неорганического сульфата для синтеза PAPS.
Глутатион (GSH) ключевой метаболит и форма хранения серы
Аминокислоты серы вносят существенный вклад в поддержание и целостность клеточных систем, влияя на окислительно-восстановительное состояние клеток и способность выводить токсичные соединения, свободные радикалы и активные формы кислорода [ 16]. Цистеин и метионин не накапливаются в организме. Любой избыток пищи легко окисляется до сульфата, выводится с мочой (или реабсорбируется в зависимости от диетических уровней) или сохраняется в форме глутатиона (GSH).Даже в экстремальных ситуациях, например, когда дефицит триптофана приводит к общему катаболическому эффекту, организм пытается сэкономить потерю серы, продолжая хранить любую доступную серу в виде GSH в печени [17]. Доступность цистеина, по-видимому, является фактором, ограничивающим скорость синтеза GSH. Значения GSH ниже нормы при большом количестве истощающих заболеваний и после приема определенных лекарств, что часто приводит к плохой выживаемости [18, 19]. Предоставляя SAA, многие из этих изменений можно отменить.В головном мозге, который обычно является наиболее щадящим органом при дефиците питательных веществ, концентрация GSH снижается, чтобы поддерживать адекватный уровень цистеина. Эта потеря GSH нарушает антиоксидантную защиту. Активной формой глутатиона является восстановленная форма GSH, в то время как неактивная форма GSSG должна быть преобразована в GSH. Обычное соотношение GSH: GSSG в тканях составляет около 100: 1. Хрящ, менее важный для выживания, может плохо себя чувствовать в условиях дефицита серы, что объясняет, почему диетические добавки, содержащие серу (хондроитинсульфат, глюкозамина сульфат, МСМ (метилсульфонилметан) и т. Д.) может быть полезным при лечении заболеваний суставов [20]. Ни GSH, ни синтез GAG в этом контексте не исследовались.
Было показано, что даже гидротерапия сероводородной водой, часто сопровождаемая приемом такой воды и рассматриваемая как эмпирический метод лечения различных заболеваний, включает каскад антиоксидантов, связанный с GSH [21, 22]. Взаимосвязь диеты, возраста и других физиологических параметров с концентрацией GSH в крови и тканях хорошо задокументирована [23–26].Поскольку все исследованные диетические добавки, содержащие сульфат, включая МСМ [27], легко метаболизируются до или вскоре после абсорбции до сульфата или низкомолекулярных промежуточных продуктов, они должны быть в состоянии уменьшить потери GSH, связанные с диетическим дефицитом, повышенным использованием из-за болезни или измененная иммунная функция.
Активные формы кислорода (АФК) образуются во время нормальной клеточной активности и могут присутствовать в избытке при некоторых патофизиологических состояниях, таких как воспаление или предперфузионное повреждение.Эти молекулы окисляют различные клеточные компоненты, но особенно чувствительны серосодержащие аминокислотные остатки [28]. Таким образом, изучение фундаментальных аспектов метаболизма серы, таких как регуляция функции клеток путем окисления и восстановления метионина, а также антиоксидантные эффекты серосодержащих аминокислот [29], может помочь выяснить механизм, с помощью которого работают рассматриваемые пищевые добавки.
Глутатион: его защитная роль против окислительного повреждения и повреждения свободными радикалами и его потенциал для усиления иммунной функции
Способ, которым клетки и ткани реагируют на изменения в потреблении SAA, ограничивается характеристиками ключевых ферментов, участвующих в метаболических путях [30].При низких внутриклеточных концентрациях метионина реметилирование продукта метаболизма предпочтительнее транссульфурации, и метионин сохраняется. С увеличением потребления метионина увеличивается путь транссульфурации, который обеспечивает субстрат для синтеза GSH.
Таким образом, в условиях низкого потребления SAA синтез белка будет поддерживаться, а синтез сульфата и GSH будет сокращен. Изменения в доступности GSH могут отрицательно влиять на функцию иммунной системы и механизмов антиоксидантной защиты.
С другой стороны, было показано, что высокое потребление метионина с пищей (5–6 г / день) повышает уровень гомоцистеина в плазме, несмотря на адекватное потребление витаминов группы В [31–33]. Это вызывает некоторую озабоченность, так как никто не хочет активировать иммунную систему за счет усиления прикрепления моноцитов к эндотелиальным клеткам.
Как обсуждалось ранее, на GSH влияет потребление SAA с пищей. В исследовании изотопов на крысах, когда рационы с различным содержанием SAA давались на адекватных уровнях, 7 молекул S были включены в GSH на каждые 10 молекул, включенных в белок [34].При недостаточном уровне потребления соотношение упало до <3:10. Эта реакция на низкое потребление SAA приводит к нарушению антиоксидантной защиты.
Снижение уровней GSH и, как следствие, антиоксидантной защиты может увеличить риск повреждения хозяина посредством активации фактора транскрипции, что приводит к усилению регуляции провоспалительных цитокинов, таких как факторы ядерной транскрипции и белки-активаторы, индуцируемые в свою очередь. такими агентами, как перекись водорода, митогены, бактерии, вирусы, а также ультрафиолетовое и ионизирующее излучение.
Повреждение клеток окислителем вызовет каскад провоспалительных эффектов за счет производства перекисей липидов. Несмотря на то, что некоторые из этих эффектов являются двухфазными по своей природе, поскольку они связаны с уровнями SAA, общепринято считать, что GSH и связанная с ним антиоксидантная активность оказывают иммуностимулирующий эффект путем активации факторов транскрипции, которые тесно связаны с пролиферацией клеток, а также параллельной противовоспалительный эффект, как описано ранее.
Дальнейшие знания об этих метаболических процессах на других уровнях, помимо доступности субстрата, будут необходимы для того, чтобы мы могли с большей точностью модулировать эти процессы на благо всего организма.
Регуляция биосинтеза простагландинов с помощью глутатиона
Простагландины (PG), как очень хорошо известно, играют важную роль во множестве нормальных функций организма, а также в ключевых метаболических этапах, связанных со многими событиями, связанными с воспалением.
PG синтезируются из свободной арахидоновой кислоты с помощью двух изоформ циклооксигеназы (COX, также называемой PGh3-синтетазой). Хотя доступность арахидоновой кислоты как основного метаболического фактора, контролирующего продукцию PG, активно исследуется, очевидно, что другие клеточные кофакторы также могут регулировать биосинтез PG.
PGH-синтетаза имеет две активности: циклооксигеназную активность, которая вводит 5-членное кольцо в PUFA (полиненасыщенную жирную кислоту), и другую, которая вводит эндопероксид и гидропероксид в PUFA. Активность пероксидазы восстанавливает гидропероксид до гидроксильной группы с использованием GSH в качестве источника восстанавливающих эквивалентов.
Наблюдение, что как конститутивные, так и индуцируемые митогеном изоформы простагландин h3 синтетазы заметно зависят от GSH и GSH пероксидазы [35], вызвало значительный интерес в связи с этим процессом.Сайты действия GSH и пероксидазы GSH на рассматриваемый метаболический путь показаны на рисунке 2.
Рисунок 2Ферментативное превращение арахидоновой кислоты (AA) в PG и сайты ингибирования GSH и GSH пероксидазой (GSSPx) . (По материалам Marglit et al. [36]).
Исследования Margalit et al [36] предоставили четкие доказательства на мышах, что повышенные уровни GSH ингибируют продукцию PG и, скорее всего, проявляют свои противовоспалительные эффекты в модели, индуцированной кристаллами уратов, посредством этого механизма.Это ослабление синтеза PG in vivo проливает свет на другое потенциальное преимущество, связанное с повышенным потреблением SAA и адекватными уровнями GSH в тканях. С практической точки зрения это повышает вероятность того, что удовлетворительное потребление SAA в сочетании с PUFA может оказаться значительным преимуществом для людей, страдающих различными аномалиями суставов, связанными с воспалением.
Вопрос о том, как в присутствии адекватных предшественников ПНЖК конститутивные и индуцибельные формы простагландин-Н-синтетазы могут быть индуцированы для выработки соответствующих форм простагландина, необходимых для поддержания тканевого гомеостаза, будет зависеть от дальнейшего понимания кофакторов и механизмов обратной связи. вовлеченный.
Пока не будут даны ответы на эти фундаментальные вопросы, лучшее, что мы можем сделать, это продолжать снижать соотношение омега-6 / омега-3 в нашем рационе ПНЖК (которое в настоящее время составляет около 10,0 по сравнению с 12,0 всего несколько лет назад) за счет увеличения потребление рыбы и некоторых растительных масел, что считается идеальным соотношением 2,3 / 1,0 [37].
Метаболические исследования, изучающие взаимосвязь потребления серы с пищей и экскреции неорганического сульфата с мочой
Приветствуется отсутствие доступных данных о взаимосвязи пищевых добавок, таких как хондроитинсульфат и его аналоги, с потреблением серы с пищей и любой возможной взаимосвязи Нам предстоит рассмотреть серию исследований метаболизма / баланса человека, которые будут связывать потребление белков, пищевых добавок, содержащих серу и SAA, с экскрецией сульфатов.
Наши предварительные исследования были представлены в Американском колледже клинического питания, Американском колледже ревматологии (2001) и впоследствии опубликованы [20]. Эти исследования, хотя и ограниченные по объему, предоставляют дополнительные доказательства быстрого превращения серы в пищевых добавках в неорганический сульфат. Удержание серы из SAA или из диетических добавок, вводимых во время приема пищи с низким или предельным уровнем белка, по сравнению с усиленным выведением во время более высокого уровня потребления, дало ценные ключи к разгадке (рис.3). Из наших результатов следует, что минимальные адекватные значения потребления, определенные в условиях VA у пожилых людей Tuttle et al [6], могут быть ближе к точности, чем те, которые в настоящее время принимаются в качестве RDA.
Рисунок 3Прием SAA как часть основной диеты (темная полоса) дополняется добавкой 10 ммоль метионина, вводимой в виде однократной дозы утром в день эксперимента. Таким образом, общая высота столбца представляет поступление S в ммоль. В соседнем столбце указано количество свободного сульфата, выделяемого с мочой за 24-часовой период.
Наши исследования проводились на нормальных добровольцах (возраст 35–70). Сульфат, свободный и этерифицированный, определяли модификацией нефелометрического метода Берглунда и Сорбо [38] и креатинина мочи с использованием набора (555-A) от Sigma. Потребление SAA оценивали с помощью программного обеспечения для анализа питания (ESHA Research, версия 7.6). L-метионин (Solgar) покупали в виде пищевых добавок. Состав L-метионина с замедленным высвобождением был специально приготовлен Xcel Medical Pharmacy (Woodland Hills, CA.).
Взаимосвязь между диетическим потреблением белка с метионином или S-содержащими соединениями или без них и экскрецией свободного сульфата с мочой
Субъекты были адаптированы к определенному уровню диетического белка, начав их диету за 24 часа до фактического теста. Уровни протеина были увеличены за счет добавления к основному рациону обезжиренного тунца, который в основном состоит из протеина. На рис. 3 приведены результаты исследований баланса серы, включающих добавки L-метионина.
Наши результаты (рис. 3) ясно демонстрируют, что задержка S происходит во время потребления низких уровней белка.Когда потребляется менее 10 ммоль серы, полученной из пищевых белков, добавление в рацион 10 ммоль L-метионина сопровождалось сохранением этой аминокислоты. При более высоком уровне потребления белка с пищей, когда предположительно удовлетворяются потребности в сере, практически весь метионин, добавленный в рацион, выводится с мочой.
Значительное удержание метионина при низком уровне потребления белка дало первые подсказки о том, что наш рацион серы может быть пограничным или даже неудовлетворительным для многих людей.
Потребление SAA в нормальной популяции: связь с RDA и потенциальной потерей сульфатов, связанной с метаболизмом лекарства
Обобщенную оценку потребления и качества диеты очень сложно сделать по очевидным причинам. Неоднородность населения (культурная, социально-экономическая, этническая, географическая, род занятий, потребление фаст-фуда, реклама и т. Д.) — все это влияет на потребление пищи. Тем не менее, для целей этого исследования казалось важным попытаться создать профиль, который охватывал бы различные сегменты населения и соотносил полученные значения с принятой RDA для SAA и альтернативными более высокими требованиями, предложенными другими.Чтобы получить более подробное представление, мы сгруппировали различных людей, прошедших оценку, в подгруппы (таблица 1).
Таблица 1 Среднее потребление серы-аминокислот, связанное с разнообразием типичных диет.Несмотря на то, что диеты периодически меняются, мы заметили, что люди склонны придерживаться определенных повторяющихся схем, которые в некотором роде облегчили оценку. Потребление SAA, измеренное у 32 человек, колебалось от 1,8 до 6,0 г / день (от 14 до 45 ммоль / день). Для расчетов цистеин и метионин были объединены как SAA.В целом соотношение цистеин / метионин близко к белку из птицы и красного мяса и 0,7 для рыбы. Молочные продукты, как правило, содержат немного больше метионина, а продукты, богатые крахмалом, немного больше цистеина. Яйца содержат значительно больше цистеина. Для оценки молярных концентраций использовали соотношение 1: 1. Некоторые из более низких значений SAA, зафиксированные в нашем опросе, включали людей, которые, как правило, были более заботливыми о своем здоровье и не потребляли красного мяса и небольшого количества животного белка, а также тех, кто потреблял «модные диеты».Многие пожилые люди могут оказаться полностью дефицитными (группа X) независимо от используемых критериев (рис. 4). Очевидно, что эти диетические оценки следует считать очень предварительными, но в настоящее время они предназначены для того, чтобы попытаться пролить свет на редко исследуемую территорию.
Рисунок 4Диетическое потребление SAA (метионин плюс цистеин), измеренное в различных подгруппах населения. Их сравнивали с предложенными требованиями: RDA (1989), 2x RDA (запас прочности Роуза) [4] и Tuttle et al [6], определенными для пожилых людей.Справа от каждой группы находится сплошная полоса, которая представляет потребление SAA, уменьшенное на 0,9 г / день, чтобы учесть предполагаемую потерю серы, связанную с потреблением стандартной дозы ацетаминофена, выводимого в виде сульфатированного конъюгата.
На приведенном выше рисунке сравнивается потребление SAA в г / день с принятой RDA (1989), удвоенными значениями RDA, принятыми для обеспечения большей безопасности большой популяции, и значениями, полученными для пожилых людей в результате исследования VA Tuttle et al. al.[6].
Также включен столбец, в котором доступные SAA уменьшаются на 0,9 г / день, что эквивалентно потере SAA, связанной с приемом стандартной более высокой рекомендованной дозы парацетамола. Как уже отмечалось, этот препарат, как и некоторые другие, выводится в основном конъюгированным с сульфатом. В зависимости от того, какое допущение для минимальных требований используется, только те группы, которые появляются выше границы отсечения, будут получать адекватное количество SAA. Используя оценки Tuttle et al [6] (которые хорошо согласуются с нашими текущими оценками) в сочетании с предполагаемой потерей сульфата из-за конъюгации с ацетаминофеном, большая часть населения, в которую входят наиболее уязвимые к OA, может оказаться с дефицитом серы. или получающих предельное потребление.
В настоящее время мы не можем сделать какие-либо однозначные выводы из этих оценок. Мы знаем, что реабсорбция сульфатов почками увеличивается в периоды дефицита [39], но неизвестно, как долго может сохраняться такой щадящий эффект. Значения, полученные Tuttle et al., Получены из ограниченной выборочной популяции VA. То же самое и у нас, и у Роуза и др. Пока эти исследования не будут расширены за счет одновременного определения S и N-баланса и исследований биосинтеза на животных, а также до проведения хорошо контролируемых исследований S-баланса на людях, мы не сможем четко ответить на этот важный вопрос.
Следует отметить, что мы не смогли найти в зарегистрированной литературе никаких исследований, которые эффективно измеряли бы баланс серы у человека или других животных. В этой связи все метаболические исследования, даже те, которые сосредоточены на потребностях в серных аминокислотах, изучают баланс азота, но не баланс серы. По сути, это означает, что роль серосодержащих аминокислот оценивалась только в синтезе белка, но никогда не с точки зрения их способности вносить серу во многие важные метаболиты.В рамках наших предварительных исследований мы оценили потребление SAA с пищей, экскрецию неорганического сульфата и креатинина с мочой у 35-летнего мужчины, потребляющего произвольно сбалансированную диету в течение 3-дневного периода. Результаты представлены на рис. 5.
Рисунок 5Выведение сульфатов и креатинина с мочой во время стандартной диеты в течение 48 часов.
На приведенном выше рисунке подчеркивается еще один аспект предлагаемых исследований — взаимосвязь между выделением S и N.Мы не включали эфирный сульфат (менее 5% от общего количества), поскольку лекарства не принимались. Экскреция креатинина в течение 24-часового периода долгое время была связана с мышечной массой и использовалась для метаболических расчетов. Они бесполезны для исследований N-баланса, так как не отслеживают потребление белка [40]. С другой стороны, очевидно, что потребление и выведение сульфатов довольно хорошо коррелируют. Свободные аминокислоты, как правило, не могут храниться, и, в частности, SH-фрагмент цистеина легко окисляется.Цистеин может быть цитотоксичным, поскольку реакционноспособная тиоламиновая структура может сочетаться с альдегидами, такими как пиридоксаль, а также может хелатировать основные двухвалентные катионы. SAA используются для пополнения запасов GSH, который можно рассматривать как форму хранения серы, и только когда эта цель достигнута, избыток окисляется до сульфата.
Выведение сульфата, связанное с приемом метилпреднизолона, включено, чтобы проиллюстрировать, как катаболическое событие может повлиять на потерю серы (рис. 6). Поскольку стероиды часто используются пациентами с заболеваниями суставов, большая экскреция сульфата может, среди прочего, мешать синтезу PG и других важных метаболитов, таких как GSH.Этот аспект катаболического эффекта стероидов, похоже, не исследован.
Рис. 6Выведение с мочой свободного сульфата после однократного перорального приема метилпреднизолона (24 мг) с последующей второй дозой (20 мг) на следующий день при соблюдении диеты, которая обеспечивала 19 ммоль SAA / день.
Употребление газированной минеральной воды, содержащей 0,5 г сульфата / литр (в данном случае Сан-Пеллегрино, одна из очень немногих минеральных вод, содержащих сульфат-ионы) в течение дня (2 литра, содержащие примерно 10 ммоль), сопровождалось количественным выделением сульфат, когда уровни пищевого белка обеспечивали 25 ммоль SAA или более в день (рис. 7).
Рисунок 7Выведение сульфата с мочой за сутки у лиц, потребляющих различное количество белка в сочетании с 10 ммолями сульфата из источника минеральной воды, равномерно распределенных в дневные часы и по сравнению с контролем (случай 1, базальная диета : 17 мМ диетическая SAA, случай 2, базовая диета: 26 мМ SAA).
Эти данные подтверждают наблюдение, иногда оспариваемое, что неорганические сульфаты легко абсорбируются и выводятся с мочой, несмотря на осмотические эффекты, которые они могут вызывать и которые приводят к их использованию в качестве слабительных [11, 41].В нашем случае постоянное введение разбавленного раствора могло способствовать абсорбции из желудочно-кишечного тракта и усилению экскреции с мочой. По оценкам, абсорбция в тонком кишечнике достигает 5 ммоль / день, а оставшаяся часть абсорбируется в толстой кишке [41].
Уровни сульфатов в питьевой воде значительно различаются в зависимости от их источника и местонахождения. Исследование, проведенное в Огайо, по оценке концентраций сульфатов в колодезных водах, потребляемых сельскохозяйственными животными, показало, что значения находятся в диапазоне от 6 до 1600 г / литр.На этикетке указано, что вода San Pellegrino из итальянского источника содержит 0,535 г сульфат-ионов на литр. Мы экспериментально обнаружили, что использованные партии не отличались более чем на 5% от заявленного значения. Неорганические сульфаты — это лишь второстепенные компоненты нашего рациона. Некоторые обработанные или обогащенные продукты содержат незначительное количество сульфитов в качестве консервантов, а некоторые добавки, входящие в состав муки, например (сульфат железа), могут содержать сульфат. Чеснок, лук и брюссельская капуста содержат значительное количество серы.Корма, скармливаемые животным, были исследованы на предмет содержания серы гораздо более подробно, чем продукты для людей, и наблюдались колебания от 0,2% в жоме свеклы до 1,2% в жмыхе канолы (в пересчете на сухой вес). Как отмечалось ранее, уровень серы в рационе может сильно повлиять на рост и здоровье скота.
Потребности пожилых людей в белках и аминокислотах с особым упором на серосодержащие аминокислоты
Расчетные потребности в белках для всех возрастов, как обсуждалось ранее, основывались на исследованиях азотного равновесия и иногда подкреплялись функциональными показателями, такими как иммунитет. функция или мышечная сила.Данные из различных источников свидетельствуют о том, что потребность в белке для азотного равновесия у пожилых людей превышает 0,8 г / кг веса тела в день. Предлагались значения около 1,0 г / кг [42]. Однако из-за методологических трудностей данные не позволяют сделать очень надежный прогноз.
Как указывает Янг [43], наши знания о диетических потребностях пожилых людей часто ограничены и противоречивы, хотя по-прежнему прилагаются значительные усилия для решения этой проблемы.Существует общее мнение, что потребности этой популяции в белках недооцениваются, и было высказано предположение, что в общей сложности 15% потребностей в энергии этой популяции обеспечивается за счет белков. Это соответствует примерно 75–85 г белка в день. Это количество белка обеспечит от 3,5 до 4,0 г SAA в день, что более чем соответствует всем оценкам потребностей в этих аминокислотах. К сожалению, этот уровень потребления белка нечасто достигается пожилым слоем населения.Хорошо известная саркопения, связанная с пожилым возрастом, по-видимому, частично связана со снижением потребления белка и энергии, вызванным изменениями вкусовых ощущений, зубными рядами, социальной изоляцией, депрессией и экономическими факторами. В дополнение к неоптимальному потреблению пищи пожилые люди, по-видимому, заменяют белок пищей, богатой жирами и углеводами, что также может отражать изменения вкуса [44]. Рекомендации ВОЗ по потреблению SAA в дозе 13 мг / кг массы тела находятся в том же диапазоне, что и рекомендации RDA.Существует мнение, что при заболеваниях и после травм эти значения могут быть в 2–3 раза выше [45].
Растет объем данных, указывающих на потенциальную важность окислительного стресса и, как следствие, изменений окислительно-восстановительного состояния при многих заболеваниях, включая сепсис, хроническое воспаление, рак, СПИД / ВИЧ и, конечно же, старение. Эти наблюдения требуют постоянного внимания к потенциальной добавочной роли добавок SAA в форме дополнительного белка или, как было обнаружено, полезного, N-ацетилцистеина в некоторых конкретных обстоятельствах.Из-за токсичности цистеина и, возможно, даже добавок метионина, вводимых в избытке, и внутренних проблем, связанных с индуцированным дисбалансом аминокислот, белки, богатые SAA, рассматривались как добавки. Immunocal ® , очищенная молочная фракция, обогащенная сывороточным белком, в настоящее время используется из-за ее способности усиливать антиоксидантную защиту и улучшать иммунную функцию [46]. Двадцать граммов / день Immunocal значительно улучшили мышечную активность и уровень GSH лимфоцитов в группе из 20 молодых людей.Хотя сывороточные белки содержат значительно больше цистеина, чем казеина (2,5% против 0,35), общее количество общих SAA отличается менее значимо (5,2% против 3,2%).
Стоимость и доступность стали еще одним ключевым фактором в снижении потребления белка с пищей у пожилых людей, так же как и предполагаемая непереносимость определенных групп продуктов, трудности при разрыве и пережевывании волокнистой пищи, а также страх употребления слишком большого количества жира или холестерина. К сожалению, яйца, аминокислотный профиль которых считается стандартом, с которым сравниваются другие белки, и которые относятся к белкам с более высоким содержанием SAA и являются одними из наименее дорогих с точки зрения стоимости, часто не включаются в качестве основных ингредиентов в диеты пожилых людей.
Нельзя недооценивать важность диетического белка для этой группы населения, поскольку недостаточное потребление белка способствует, среди прочего, снижению резервной емкости легких, повышенной хрупкости кожи, остеопорозу, снижению иммунной функции и мышечной массы (саркопения), плохому заживлению и более длительное восстановление после болезни [2, 47].
6.5: Биохимия серосодержащих аминокислот
S. cerevisiae требует для жизни трех серосодержащих аминокислот.Помимо Met
и Cys, которые включены в клеточные белки, клеткам также требуется S-аденозилметионин (AdoMet), который поставляет активированные метильные группы для многих реакций метилирования. Консенсусное мнение о синтезе этих трех аминокислот на предыдущей странице теперь хорошо подтверждается биохимическими и генетическими данными из многих лабораторий (обзор в Thomas
& Surdin-Kerjan, 1992). Связь ген-фермент не могла быть окончательно установлена до тех пор, пока не были разработаны методы молекулярного клонирования и секвенирования ДНК, которые позволили исследователям использовать плазмидную комплементацию для непосредственного тестирования функции генов.В этих экспериментах исследователи сконструировали плазмиды с генами MET , CYS или SAM дикого типа, которые были трансформированы в мутантные штаммы. Трансформированные штаммы были способны выжить только в том случае, если плазмида содержала аллель дикого типа инактивированного гена в мутанте. (Вы будете использовать плазмидную комплементацию в этом классе, чтобы подтвердить идентификацию ваших штаммов и плазмид.)
Большинство генов, с которыми мы будем работать в этом семестре, кодируют ферменты, которые катализируют взаимное превращение одной серосодержащей молекулы во вторую серосодержащую молекулу.Другие гены MET кодируют ферменты, которые не участвуют напрямую в синтезе серосодержащих аминокислот, но катализируют синтез кофактора или донора метила, необходимого для синтеза серосодержащих аминокислот. В кратком описании ниже мы проследим превращение атома серы из неорганического сульфата в его превращение в Met, Cys или AdoMet.
Ассимиляция сульфатов включает активацию серы и восстановление до сульфида
Ранние этапы пути, который включает реакции, участвующие в превращении сульфата в сульфид, включают путь ассимиляции сульфата.Сульфат-ионы являются источником большинства серы в биологических молекулах, но требуется значительная метаболическая энергия, чтобы активировать сульфат из его степени окисления +6 и преобразовать его в сульфид, который имеет степень окисления -2. Ферменты, ответственные за ассимиляцию сульфатов, широко распространены в микроорганизмах и растениях. В S. cerevisiae сульфат сначала активируется АТФ-сульфурилазой, или Met3p, с образованием 5’-аденилилсульфата (APS). Затем APS фосфорилируется Met14p или киназой APS, образуя 3’-фосфо-5’-аденилилсульфат (PAPS).PAPS представляет собой интересную молекулу, поскольку она содержит активированный атом серы, который можно использовать для различных реакций переноса серы. У млекопитающих PAPS используется для различных реакций сульфатирования в Golgi, где акцепторы включают липиды, белки и множество небольших молекул. (Интересно, что киназа APS — единственный дрожжевой фермент, участвующий в ассимиляции сульфатов с гомологами у млекопитающих.)
Последние две стадии ассимиляции сульфатов — это НАДФН-зависимые реакции восстановления.PAPS-редуктаза, или Met16p, катализирует первую реакцию, которая добавляет два электрона к атому серы. Окончательное 6-электронное восстановление катализируется сульфитредуктазой. Сульфитредуктаза представляет собой сложный металлофермент, содержащий две субъединицы Met5p и две субъединицы Met10p, а также несколько простетических групп, включая сирогем, которые участвуют в переносе электронов. (Простетическая группа — это ион металла или органическая молекула, ковалентно связанная с ферментом и необходимая для его активности.) В дрожжах сирогем синтезируется в серии реакций, катализируемых Met1p и Met8p.Синтез сирогема формально не считается частью пути ассимиляции сульфата, но его функция является критической для сборки функциональной сульфитредуктазы.
Синтез и трансульфурация гомоцистеина
На следующем этапе биосинтеза Met и Cys сульфид включается в аминокислотный гомоцистеин (Hcy). Hcy находится в точке разветвления между несколькими путями в дрожжах. Аминокислотный каркас Hcy в конечном итоге происходит из аспарагиновой кислоты, которая была преобразована в
за серию стадий в гомосерин.(Примечание: «гомо» аминокислоты имеют дополнительный атом углерода в своих боковых цепях по сравнению с однофамильцами без префикса.) Met2p активирует гомосерин
в реакции ацетилирования, в которой используется ацетил-КоА. Met17p, также известный как гомоцистеинсинтаза или O-ацетил гомосеринсульфгидриаза, затем катализирует реакцию O-ацетилгомосерина с сульфидом с образованием Hcy.
В дрожжах Hcy служит предшественником Cys или Met. Путь, соединяющий Hcy и Cys, называется путем транссульфурации.Транссульфурация обеспечивает S. cerevisiae необычайной гибкостью в отношении источников серы. Четыре различных генных продукта участвуют в превращении Hcy в Cys и наоборот, используя цистатионин (см. Ниже) в качестве общего промежуточного продукта. Str2p катализирует синтез цистатионина из Cys и O-ацетилгомосерина, продукта реакции, катализируемой Met2p. В противоположном пути Cys4p (также известный как Str4p) катализирует синтез цистантина из Hcy и Ser. Четыре гена, участвующие в пути переноса серы, демонстрируют разные закономерности эволюционной консервации.Например, E. coli не может синтезировать Cys из Met, в то время как млекопитающие не могут синтезировать Met из Cys.
Цистатионин является промежуточным продуктом для реакций трансульфурации. Ферменты в пути транссульфурации S. cerevisiae кодируются генами STR1 — STR4 . Str2p и Str1p (Cys3p) катализируют синтез и гидролиз, соответственно, связи цистатионина S-C g . Str3p и Str4p (Cys4p) катализируют соответственно синтез и гидролиз цистатиониновой связи S-C b .
Метионин и AdoMet образуются во время метильного цикла
Hcy также является отправной точкой цикла, который производит Met и AdoMet. Цикл начинается, когда Met6p катализирует превращение Hcy в Met, используя необычный донор метила, полиглутамил-5-метилтетрагидрофолат (THF). Гены MET13, и MET7 кодируют ферменты, которые катализируют последние две стадии синтеза полиглутамил 5-метил-ТГФ, что объясняет их неспособность клеток met7 и met13 синтезировать метионин.
Как и следовало ожидать, большая часть метионина используется для синтеза белка в клетках, но заметное количество преобразуется в высокоэнергетический донор метила, AdoMet, двумя почти идентичными синтазами AdoMet, Sam1p и Sam2p. S. cerevisiae способен синтезировать большие количества AdoMet, который либо используется для реакций трансметилирования, либо хранится в вакуоли. (Фактически, дрожжи являются источником большинства коммерчески производимых AdoMet.) Множественные дрожжевые метилтранферазы катализируют перенос метильных групп от AdoMet к сотням различных субстратов, которые включают нуклеотидные основания и сахара в ДНК и РНК, различные боковые цепи аминокислот в белки, липиды, небольшие молекулы и многое другое.Каждая реакция трансметилирования генерирует одну молекулу S-аденозилгомоцистеина (AdoHcy), которая гидролизуется Sah2p до аденозина и Hcy, завершая метильный цикл.
Мы не будем изучать ферменты, участвующие в метильном цикле этого класса, но
важно понимать их важность для выживания клеток. Аминокислотные последовательности Sam1p и Sam2p идентичны на 93%, что намного выше, чем у других белков, возникших в результате дупликации генов в S. cerevisiae .Эта избыточность обеспечивает буфер против потери любой функции. Клетки с мутацией в гене SAM1 или SAM2 способны выжить, но клетки с мутациями в обоих генах не могут выжить. Сходным образом ген SAh2 является одним из немногих важных генов в S. cerevisiae , вероятно, потому, что накопление AdoHcy будет ингибировать многие реакции метилтрансферазы.
Мутации нарушают биохимические пути
Мутанты met , которые вы анализируете, не способны катализировать одну из реакций, необходимых для синтеза серной аминокислоты.В этой лаборатории вы будете использовать селективные и дифференциальные среды, чтобы определить, какие гены были инактивированы в ваших штаммах. Думайте о каждой мутации как о стирании одной из стрелок, показанных на пути серно-аминокислотного пути. Наши селективные среды содержат множество источников серы. В зависимости от положения мутации встретился с мутацией относительно источника серы, штамм может или не может быть способен синтезировать серные аминокислоты.
Вы также будете использовать дифференциальную среду, агар BiGGY, чтобы различать штаммы дрожжей
по количеству производимого ими сероводорода.Это связано с тем, что BiGGY содержит висмут, который реагирует с сульфидом с образованием осадка от коричневато-черного до черного. Ожидается, что все штаммы будут расти на BiGGY, поскольку он содержит дрожжевой экстракт, который является источником метионина. BiGGY также содержит сульфит, а не сульфат, в качестве основного источника серы. Найдите положение мутировавших генов в пути относительно сульфида и сульфита. Мутации в генах перед сульфидом должны давать более светлые колонии, так как будет производиться меньше сульфида. Из них мутации, предотвращающие восстановление сульфита, должны давать самые легкие колонии.Мутации в генах ниже сульфида должны приводить к образованию более темных колоний, потому что штаммы не могут метаболизировать сульфид.
Делая свои прогнозы для этого эксперимента, вы можете найти эту аналогию полезной: метаболический путь мало чем отличается от одностороннего ( из-за энергетических соображений, большинство метаболических путей являются однонаправленными ) шоссе с серией мостов, соединяющих острова. ( Острова имеют разные уровни энергии. ) Машины, проезжающие по шоссе, представляют собой молекулы, которые превращаются из одной формы в другую.Когда автомобиль подъезжает к следующему острову на пути, его цвет меняется, потому что он превратился в другую молекулу. Мосты — это ферменты
в пути. Они облегчают проезд автомобилей, поскольку катализируют реакции, в результате которых одна молекула превращается в другую. Если мутация происходит в гене, кодирующем определенный фермент, этот конкретный мостик рушится. Перед разрушенным мостом начинают скапливаться машины, и очень мало машин можно будет найти на островах за разрушенным мостом.В некоторых случаях может быть альтернативный маршрут или путь спасения, но обычно это менее эффективный путь.
Sulfur Biology
Молекулы, содержащие восстанавливающий тиол, такой как глутатион, цистеин и белок, реагирующий на окислительно-восстановительный потенциал, в живом организме действуют как антиоксидантные или реагирующие на окисление молекулы. Эти молекулы считаются наиболее важной группой молекул, которые способствуют поддержанию окислительно-восстановительного гомеостаза в живом организме.Персульфиды и полисуфиды (Рис.1), содержащие сульфаны серы, привлекают большое внимание в поддержании клеточного окислительно-восстановительного гомеостаза.
|
Рис.1 Химические вещества, содержащие сульфановую серу |
Сероводород (H 2 S), известный как высокотоксичный газ, является третьей наиболее газообразной сигнальной молекулой после оксида азота (NO) и оксида углерода (CO). Сообщается, что H 2 S оказывает физиологическое воздействие на вазолидацию, цитопротекцию, секрецию инсулина и нейротрансмиссию.В физиологических условиях примерно 20% H 2 S недиссоциировано, а 80% диссоциировано на ионы гидросульфида (пик 7,0). Сероводород присутствует в живом организме в небольших количествах. Сульфид-ион оказывается чувствительным к изменениям окислительно-восстановительного состояния (рис. 2). Молекулярные механизмы, определяющие, как H 2 S влияет на передачу сигналов в клетках и другие физиологические события, остаются недостаточно изученными 1) .
|
Фиг.2 Функция сероводорода in vivo |
Согласно недавнему исследованию, полисульфиды образуются из H 2 S в головном мозге, стимулируя передачу сигнала в головном мозге (рис. 3) 2) . Недавние исследования показывают, что тетрасульфид натрия (Na 2 S 4 ) оказывает эффект защиты клеток от окислительного стресса посредством передачи сигналов Keap1 / Nrf2 (Рис. 4) 3) .
|
Фиг.3 Нейронная передача полисульфидом |
Рис.4 Цитопротекция полисульфидом |
Цистеин-персульфид синтезируется из цистеина с помощью двух ферментов, цистатионин-β-лиазы (CSE) и цистатионин-β-синтазы (CBS). Сообщается, что в живом организме присутствует высокая концентрация цистеин-персульфида и глутатион-персульфида (рис. 5) 4) .
|
Фиг.5 Биосинтез персульфида цистеина |
Персульфид, который содержит атомы двухвалентной серы, связанные с другим атомом серы, называемым сульфановой серой, играет иную роль, чем сероводород. Белковые тиолы — это молекулы, которые действуют на сероводород или пер (поли) сульфид. Чтобы понять биологическую роль соединений с сульфановой серой или сероводородом, необходимо подробное объяснение протеина тиола.
|
Фиг.6 Профили модификации тиоловых остатков в белке |
Список литературы
1) Х. Кимура, редактор, «Сероводород и его терапевтическое применение»
2) Ю. Кимура, Ю. Миками, К. Осуми, М. Цугане, J-I. Ока и Х. Кимура, «Полисульфиды — возможные сигнальные молекулы, производные от h3S, в головном мозге крысы», FASEB. J. , 2013 , 27 , 2451
3) С. Койке, Ю. Огасавара, Н. Сибуя, Х. Кимура и К.Исии, «Полисульфид оказывает защитное действие против цитотоксичности, вызываемой трет-бутилгидропероксидом, посредством передачи сигналов Nrf2 в клетках нейробластомы», FEBS Lett. , 2013 , 3548
4) Т. Ида, Т. Сава, Х. Ихара. Ю. Цучия, Ю. Ватанабэ, Ю. Кумагаи, М. Суэмацу, Х. Мотохаши, С. Фуджи, Т. Мацунага, М. Ямамото, К. Оно, Н. О. Девари-Баез, М. Сиань, Дж. М. Фукуто, и Т. Акаике, «Реактивные персульфиды цистеина и S-политиоляция регулируют окислительный стресс и окислительно-восстановительную передачу сигналов», Proc Natl Acad Sci US A.


 д.). В виде сульфат–аниона сера присутствует в жидких средах организма. Атомы серы являются составной частью молекул незаменимых аминокислот (цистин, цистеин, метионин), гормонов (инсулин, кальцитонин), витаминов (биотин, тиамин), глутатиона, таурина и других важных для организма соединений. В их составе сера участвует в окислительно–восстановительных реакциях, процессах тканевого дыхания, выработки энергии, передачи генетической информации, и выполняет много других важных функций.
д.). В виде сульфат–аниона сера присутствует в жидких средах организма. Атомы серы являются составной частью молекул незаменимых аминокислот (цистин, цистеин, метионин), гормонов (инсулин, кальцитонин), витаминов (биотин, тиамин), глутатиона, таурина и других важных для организма соединений. В их составе сера участвует в окислительно–восстановительных реакциях, процессах тканевого дыхания, выработки энергии, передачи генетической информации, и выполняет много других важных функций. ), которые производятся микрофлорой кишечника, а также связывает чужеродные для организма вещества, в том числе лекарственные препараты и их метаболиты. При этом образуются безвредные соединения – конъюгаты, которые затем выводятся из организма.
), которые производятся микрофлорой кишечника, а также связывает чужеродные для организма вещества, в том числе лекарственные препараты и их метаболиты. При этом образуются безвредные соединения – конъюгаты, которые затем выводятся из организма.

 е. сенсибилизированы к ним). Для снижения негативного воздействия сульфитов на организм рекомендуется увеличивать содержание в рационе сыров, яиц, жирного мяса, мяса птицы.
е. сенсибилизированы к ним). Для снижения негативного воздействия сульфитов на организм рекомендуется увеличивать содержание в рационе сыров, яиц, жирного мяса, мяса птицы.