Хроническая воспалительная демиелинизирующая полинейропатия (ХВДП) (информация для пациента)
Хроническая воспалительная демиелинизирующая полинейропатия (ХВДП)
Что означают эти термины?
«Хроническая» — означает, что заболевание имеет длительный курс течения, а симптоматика может неуклонно прогрессировать и рецидивировать. Для установления диагноза хронической полинейропатии должно пройти более 8 недель от момента появления первых симптомов.
«Воспалительная» — подразумевает «воспаление» как основной механизм повреждения периферических нервов вследствие нарушения комплексной работы иммунной системы, поэтому данное заболевание также можно назвать “аутоиммунным”.
«Демиелинизирующая» — характеризует тип повреждения периферических нервов, при котором преимущественно страдает миелиновая оболочка нерва.
«Полирадикулонейропатия» — означает, что патологический процесс вовлечено более одного нерва, а также корешки спинного мозга и стволы сплетений.
Как часто встречается это заболевание?
ХВДП является довольно редким заболеванием. Средняя распространенность пациентов с ХВДП в мире в среднем составляет до 0,81-1,90 случаев на 100 000 человек. Мужчины заболевают несколько чаще женщин. Дебютировать ХВДП может в любом возрасте, даже в детском, однако пик заболеваемости приходится на средний возраст — 40-50 лет.
Каковы причины развития заболевания?
Причины развития ХВДП до сих пор полностью не изучены. Однако результаты многочисленных исследований и эффективность иммуномодулирующей терапии указывают на нарушение работы иммунной системы, как ключевой причины развития заболевания. Иммунная система представляет собой очень сложный и гармоничный механизм. Ключевыми звеньями иммунной системы являются антитела, ряд белков сыворотки крови и белые клетки крови, лейкоциты. В норме иммунная система борется с чужеродными агентами (белки, вирусы, бактерии). Однако при ряде заболеваний (аутоиммунные заболевания) компоненты иммунной системы по ошибке начинают работать против собственного организма. К одним из таких заболеваний и относится ХВДП. В данном случае развивается реакция против компонентов оболочки периферических нервов, что проявляется в виде специфических симптомов, характерных для ХВДП.
К одним из таких заболеваний и относится ХВДП. В данном случае развивается реакция против компонентов оболочки периферических нервов, что проявляется в виде специфических симптомов, характерных для ХВДП.
Есть ли факторы риска заболевания?
В качестве триггерных факторов описаны респираторно-вирусные заболевания, оперативные вмешательства, беременность, вакцинация и другие причины, тем не менее прямая связь вышеуказанных факторов с развитием заболевания пока не доказана.
Возможна ли передача заболевания по наследству?
Нет. Существует ряд исследований, в которых выявлены гены, предполагаемые в развитии заболевания. Тем не менее, пока не доказано их участие в риске развития заболевания у потомков.
Как проявляется ХВДП и в чем особенности этого заболевания?
ХВДП — это заболевание периферических нервов. В подавляющем большинстве в патологический процесс вовлекаются так называемые “толстые” нервные волокна, имеющие толстый слой миелиновой оболочки, которая и является мишенью при данном заболевании. Эти волокна несут от головного и спинного мозга к нашей скелетно-мышечной системе информацию о двигательной команде и в обратном направлении о положении тела в пространстве для обеспечения равновесия. Поэтому самым распространенными симптомами являются:
Эти волокна несут от головного и спинного мозга к нашей скелетно-мышечной системе информацию о двигательной команде и в обратном направлении о положении тела в пространстве для обеспечения равновесия. Поэтому самым распространенными симптомами являются:
- слабость в руках и ногах
- неустойчивость при ходьбе
- ощущение онемения в кистях и стопах
- похудание мышц и снижение их тонуса
Точный механизм ХВДП до конца не раскрыт ввиду комплексности иммунных реакций, а потому симптоматика и характер течения заболевания могут варьировать. Отсюда выделены так называемые атипичные формы ХВДП, которые несколько отличаются от классического течения заболевания и могут иметь особенности прогноза и лечения. Диагностика таких форм может быть затруднена. К атипичным формам ХВДП относят:
- мультифокальную форму ХВДП (синдром Льюиса-Самнера)
- дистальную форму ХВДП
- чисто сенсорную или чисто моторную формы ХВДП
- ХВДП с острым началом
- хроническую иммунную сенсорную полирадикулонейропатию
Течение заболевания также может быть вариабельным — у части пациентов может развиваться грубая симптоматика, приводящая к инвалидизации, у других — минимальные неврологические нарушения; ряд пациентов может испытывать частые обострения, в то время как встречаются случаи с единственным обострением в жизни.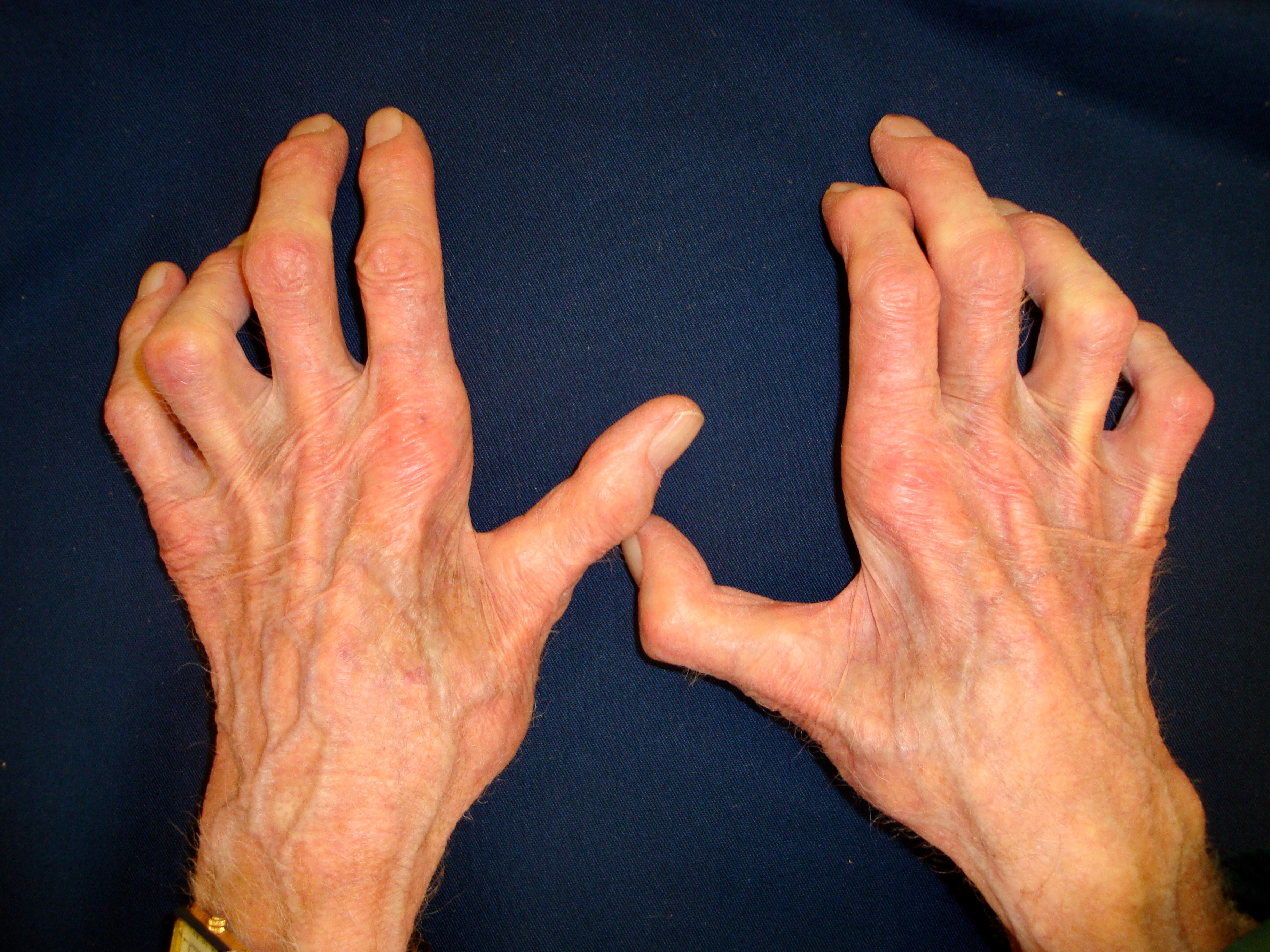
На основании чего мне установили диагноз ХВДП?
Ключевым в постановке диагноза является клинический осмотр неврологом. Существуют критерии заболевания, предложенные Европейской федерацией неврологических сообществ в 2010 г. Для подтверждения диагноза и исключения альтернативных причин полинейропатии обычно проводится ряд лабораторных анализов, а также инструментальные методы исследования. К сожалению, до сих пор нет “золотого” стандарта диагностики, который с высокой точностью мог бы указывать на «ХВДП». Поэтому диагноз зачастую ставится на основании клинической картины и результатов исследования.
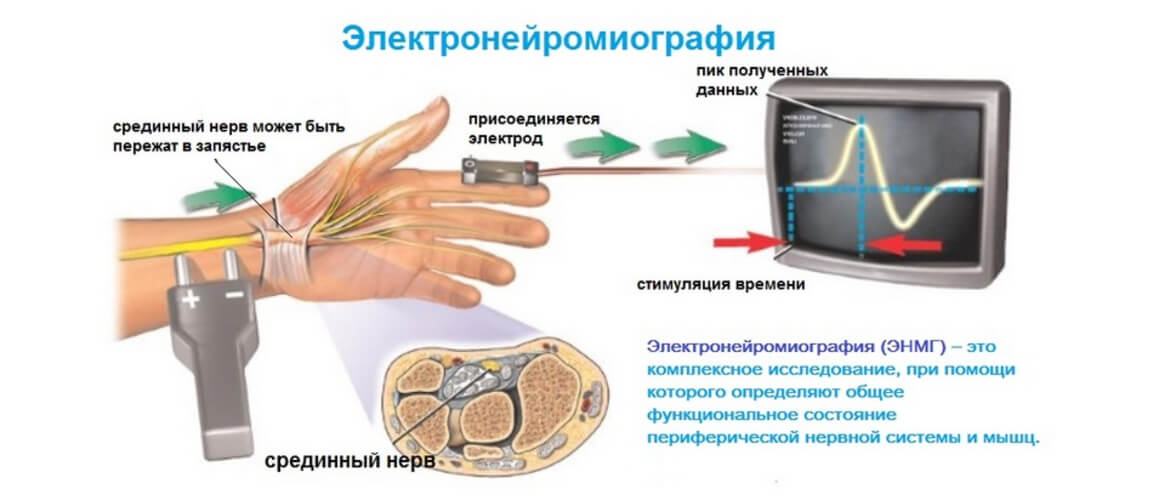
Ключевым инструментальным методом диагностики ХВДП, как и любой полинейропатии, является электронейромиография. Это исследование проводимости периферических нервов при помощи коротких электрических импульсов, передающихся по ходу нерва. Стимуляция приводит к сокращению мышцы, иннервируемой исследуемым нервом, которое регистрируется электродом.
Если данных для установки диагноза окажется недостаточно, могут дополнительно проводиться МРТ сплетений, анализ спинномозговой жидкости, УЗИ периферических нервов и в редких случаях биопсия нерва. К одним из критериев правильности установленного диагноза относится улучшение состояния, либо приостановление прогрессирования заболевания на фоне патогенетической терапии.
Какие варианты лечения ХВДП существуют?
До 80% пациентов с ХВДП имеют эффект от терапии, модулирующей работу иммунной системы. На основании крупных исследований в лечении ХВДП доказанную эффективность имеют следующие варианты лечения:
- глюкокортикостероидные препараты
- препараты внутривенного человеческого иммуноглобулина
- плазмаферез
Ни один из известных на сегодняшний день препаратов не излечивает ХВДП, только позволяет снизить активность заболевания, предупредить от дальнейшего ухудшения или обострения, а также уменьшить выраженность симптомов. Кроме того, ответ на лечение у разных людей может различаться.
Кроме того, ответ на лечение у разных людей может различаться.
Каждый способ лечения имеет свои плюсы и минусы, которые обговариваются врачом, учитывая все индивидуальные особенности?
Глюкокортикостероидные препараты (преднизолон, метилпреднизолон) назначаются в форме таблеток и инфузий. Вначале подбирается высокая доза из расчета массы тела, которая со временем постепенно снижается. Длительность приема и величина поддерживающей дозы зависят от тяжести симптоматики, скорости ее прогрессирования, а также ответа на лечение. Тем не менее, для оценки эффективности лечения, длительность терапии должна быть не менее 12 недель. Несмотря на доказанную эффективность и относительно низкую стоимость, лечение ГКС может быть сопряжено с рядом побочных явлений — набор веса, тошнота, бессонница, раздражительность, обострение язвенной болезни, повышение цифр артериального давления и уровня сахара крови, снижение плотности костной ткани. Поэтому наряду с основным препаратом назначается комплексная терапия для предупреждения развития вышеуказанных последствий лечения.
Аналогичными по эффективности глюкокортикостероидам являются препараты человеческого иммуноглобулина, однако последние гораздо реже сопряжены с развитием побочных эффектов, а потому более безопасны. Пожалуй, главным недостатком такого лечения является его высокая стоимость. Препараты человеческого иммуноглобулина получают путем очистки большого количества (>10,000 л) человеческой плазмы (>1000 доноров), что обуславливает их дороговизну. Лечение заключается в ежемесячном курсовом внутривенном введении препарата. Курс обычно занимает 4-5 дней. В дальнейшем частота введения препарата может варьироваться в зависимости от его эффективности. Важным моментом является выбор препарата. Необходимо обратить внимание на его основные характеристики: препарат должен подходить для проведения высокодозной внутривенной иммунотерапии, содержание IgG должно быть не менее 95%, количества IgA и IgM должны быть следовыми. При этом количество IgA должно быть четко обозначено в инструкции, так как именно с этим классом иммуноглобулинов ассоциировано развитие аллергических реакций.
Третьим вариантом лечения является высокообъемный плазмаферез. Данный способ терапии представляет собой забор плазмы с патогенными антителами через катетер и восполнение ее стерильными растворами, белковыми растворами и/или донорской плазмой. Процедура повторяется около 5 раз, обычно с интервалом через день. Эффект от такого лечения сохраняется на протяжении 3-4 недель. Учитывая его сложность, такой способ терапии не используется для длительного лечения и часто бывает полезен в случае стремительного и\или тяжелого обострения.
У некоторых больных, несмотря на грамотное лечение, заболевание всё равно может прогрессировать или не поддаваться контролю. В этих случаях назначаются иммунодепрессанты (микофенолата мофетил, азатиоприн, циклоспорин, циклофосфамид) или моноклональные антитела (ритуксимаб). Назначение данных препаратов должно исходить от врача, имеющего опыт их применения, учитывая все показания и противопоказания, с последующим тщательным контролем эффективности и безопасности терапии.
Нужно ли вносить какие-либо изменения в привычный образ жизни?
Да. Существуют ряд рекомендаций для больных с диагнозом ХВДП:
- избегать любых вирусных и бактериальных инфекций (респираторно-вирусных, энтеровирусных заболеваний и др.)
- больше двигаться — в случае выраженных двигательных нарушений может быть назначена физическая реабилитация, эрготерапия или поддерживающие средства для ходьбы – ортезы и пр.
- ограничить курение, употребление алкоголя, что оказывает негативное влияние на кровообращение, отягощая течение полинейропатии
- исключить прием нейротоксических препаратов, усугубляющий течение полинейропатии
- тщательный уход за стопами очень важен, особенно при наличии сопутствующего сахарного диабета. Необходимо ежедневно осматривать стопы на предмет порезов, мозолей, язв.
- придерживаться диеты с низким содержанием жиров, богатой злаками, фруктами и овощами.
- избегать длительного сдавления конечностей
Каковы прогнозы при данном заболевании?
В целом, продолжительность жизни не отличается от таковой у людей, не имеющих данное заболевание. Течение болезни может быть различным — протекать с частыми обострениями, иметь медленно прогрессирующее течение, либо достигнуть стойкой ремиссии с минимальными клиническими проявлениями. Крайне важным для прогноза является своевременное назначение лечения, тщательное наблюдение за пациентом и эффектами проводимой терапии.
Течение болезни может быть различным — протекать с частыми обострениями, иметь медленно прогрессирующее течение, либо достигнуть стойкой ремиссии с минимальными клиническими проявлениями. Крайне важным для прогноза является своевременное назначение лечения, тщательное наблюдение за пациентом и эффектами проводимой терапии.
Если у вас есть симптомы полинейропатии или вам поставлен диагноз «Полинейропатия» или «ХВДП», вы можете пройти комплексное обследование в Центре заболеваний периферической нервной системы ФГБНУ НЦН, где вам помогут уточнить диагноз, выявить причины поражения периферических нервов и назначат терапию с позиций доказательной медицины.
Сотрудники центра заболеваний периферической нервной системы консультируют пациентов амбулаторно в рамках ОМС и на коммерческой основе.
ЗАПИСЬ НА ПРИЕМ И ЭНМГ/иЭМГ ПО МНОГОКАНАЛЬНОМУ ТЕЛЕФОНУ
+7 (495) 374-77-76
+7 (985) 931-60-24
Невропатия
Невропатия — это заболевание или нарушение функции нервов или отдельного нерва. Любые нервные волокна во всех участках тела могут быть повреждены в связи с травмой или болезнью. Невропатия классифицируется согласно типу и локализации возникшего повреждения нерва. Кроме того данное заболевание может быть разделено на подгруппы исходя из вида болезни, ставшей причиной нарушения функции нерва (например, невропатия, ставшая следствием изменений в организме из-за сахарного диабета, называется диабетической невропатией).
Любые нервные волокна во всех участках тела могут быть повреждены в связи с травмой или болезнью. Невропатия классифицируется согласно типу и локализации возникшего повреждения нерва. Кроме того данное заболевание может быть разделено на подгруппы исходя из вида болезни, ставшей причиной нарушения функции нерва (например, невропатия, ставшая следствием изменений в организме из-за сахарного диабета, называется диабетической невропатией).
Типы невропатий
- Периферическая невропатия: нарушение работы нервов вне головного и спинного мозга (периферической нервной системе). Соответственно данный тип невропатии поражает нервные окончания конечностей – пальцев ног, ступни, ноги, пальцы рук, ладони, руки. Термин проксимальной невропатии используется для описания повреждения нервных волокон, которое проявляется болью в бедрах и ягодицах.
- Краниальная невропатия: данный тип заболевания возникает при нарушении работы любой из двенадцати пар черепно-мозговых нервов (берут начало непосредственно из головного мозга).
 Выделяют два специфических подтипа краниальной невропатии: зрительную (оптическую) и слуховую (аудиторную). Оптическая невропатия возникает при повреждении или заболевании зрительного нерва, переносящего сигналы от сетчатки глаза к головному мозгу и ответственного за зрение. Аудиторная невропатия возникает при повреждении или заболевании слухового нерва, переносящего сигналы от внутреннего уха к головному мозгу и ответственного за слух.
Выделяют два специфических подтипа краниальной невропатии: зрительную (оптическую) и слуховую (аудиторную). Оптическая невропатия возникает при повреждении или заболевании зрительного нерва, переносящего сигналы от сетчатки глаза к головному мозгу и ответственного за зрение. Аудиторная невропатия возникает при повреждении или заболевании слухового нерва, переносящего сигналы от внутреннего уха к головному мозгу и ответственного за слух. - Автономная невропатия характеризуется повреждением нервов вегетативной нервной системы, отвечающих за работу сердца, кровоток (включая кровяное давление), пищеварение, функцию мочевого пузыря и перистальтику кишечника, сексуальную функцию, потоотделение. Возможно повреждение нервов других внутренних органов.
- Местная невропатия возникает при заболевании или повреждении одного нерва или группы нервов, одного участка тела. Симптомы данного подвида невропатии возникают внезапно.

- Причины. Повреждение нервных волокон может быть вызвано множеством заболеваний, травм, инфекционных поражений и даже недостаточностью витаминов.
- Сахарный диабет очень часто способствует развитию невропатии. Характерные проявления периферического повреждения нервов у больных с повышенным уровнем глюкозы крови часто называют диабетической невропатией. Риск возникновения данного подвида поражения нервов увеличивается с возрастом и длительностью симптомов сахарного диабета. Периферическая невропатия возникает у больных, десятилетиями страдающих от повышения уровня сахара крови. Особенно часто данная проблема затрагивает тех лиц, которые сталкиваются с трудностями контролирования течения болезни, имеют лишний вес, страдают от повышенного уровня липидов крови, повышенного кровяного давления.
- Недостаточность витамина B12 и фолиевой кислоты, других витаминов группы В может способствовать развитию повреждения нервных волокон.
- Аутоиммунная невропатия: автоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка, синдром Гийена-Барре могут вызвать невропатию. Инфекции: некоторые инфекции, включая ВИЧ/СПИД, болезнь Лайма, лепра и сифилис могут вызывать нарушение целостности нервов.
- Постгерпетическая невралгия является осложнением опоясывающего лишая (вирус семейства ветряной оспы).
- Алкогольная невропатия: алкоголизм часто сопровождается периферической невропатией. Точные причины повреждения нервов при злоупотреблении алкоголем не ясны. Допускают, что заболевание развивается в связи с токсическим влиянием самого спиртного и из-за плохого питания, недостаточности витаминов, характерной для алкоголиков.
- Генетические или врожденные заболевания могут влиять на нервы и в отдельных случаях способствуют развитию невропатии. Примерами считают атаксию Фридрейха и болезнь Шарко-Мари-Тута.

- Амилоидоз является заболеванием, при котором аномальные белковые волокна откладываются в тканях и органах. Данные изменения приводят к различным повреждениям внутренних органов, могут приводить к невропатии.
- Уремия (высокая концентрация продуктов жизнедеятельности организма в связи с почечной недостаточностью) вызывает повреждение нервов.
- Токсины и яды могут повреждать нервные волокна. К примеру, соединения золота, свинец, мышьяк, ртуть, некоторые промышленные растворители, окись азота, фосфатные удобрения не безопасны для нервной системы человека.
- Лекарства: определенные лекарственные препараты могут вызвать повреждение нервных волокон. Например, противоопухолевые препараты (винкристин) и антибиотики (метронидазол и изониазид) пагубно влияют на нейроны.
- Травма/повреждение нервов, включая продолжительное сдавливание нерва или группы нервных волокон, часто является основной причиной невропатии.
 Ухудшение кровоснабжения (ишемия) нервных волокон может вызвать длительное повреждение.
Ухудшение кровоснабжения (ишемия) нервных волокон может вызвать длительное повреждение. - Опухоли: доброкачественные или злокачественные новообразования нервов и близлежащих структур могут вызывать непосредственные повреждения нейронов или создавать давления на нервные волокна. Оба вышеописанные проблемы приводят к невропатии.
- Идиопатическая невропатия – повреждение нервных волокон без определенной причины. Термин идиопатическое происхождение используется в медицине для описания любых процессов, причину которых установить не удается.
Симптомы. Вне зависимости от причины заболевания невропатия характеризуется рядом характерных симптомов. У некоторых больных данная патология ничем не проявляется, но общие признаки невропатии все же существуют.
Степень проявления болезни у каждого пациента может сильно различаться.
Повреждения чувствительных нервов характерно для периферической невропатии.
 Автономная невропатия, в основе которой лежит повреждение нервных волокон, отвечающих за функционирование внутренних органов и желез, может проявить себя разнообразными симптомами:
Автономная невропатия, в основе которой лежит повреждение нервных волокон, отвечающих за функционирование внутренних органов и желез, может проявить себя разнообразными симптомами:
- Тошнота, рвота, вздутие живота после приема пищи
- Нарушение работы мочеполовой системы: недержание мочи, трудности с мочеиспусканием, ощущение неполного опустошения мочевого пузыря
- Импотенция (эректильная дисфункция) у мужчин
- Головокружение и обмороки
- Запор и диарея
- Размытое зрение
- Непереносимость тепла или сниженное потоотделение
Бессимптомная гипогликемия: снижение уровня глюкозы крови сопровождается дрожанием рук, повышенным потоотделением, учащенным сердцебиением. Люди, страдающие автономной невропатией, могут переносить гипогликемию бессимптомно, что угрожает здоровью и даже жизни человека.
Диагностика. Диагностические мероприятия назначаются исходя из первоначальных проявлений и симптомов невропатии. Диагноз ставится на основании данных тщательного медицинского обследования, изучения истории заболевания, уточнения причины болезни и степени тяжести невропатии. Неврологическое обследование, тестирование рефлексов и функции чувствительных и двигательных нервов являются важной частью диагностического процесса. Не существует специфических анализов крови, указывающих на наличие невропатии. В то же время данный тип диагностики проводится с целью уточнения причины заболевания и сопутствующих болезней (например, сахарного диабета и недостаточности витаминов группы В), играющих активную роль в повреждении нервов. Визуализирующие методы исследований, например, рентгенография, компьютерная томография, магнитно-резонансное сканирование, проводятся с целью определить, возникло ли патологическое давление на нервные волокна тела. Для определения нарушений функции нервной системы проводят следующие методики:Электромиография является исследованием функции нервов и мышц.
Диагностические мероприятия назначаются исходя из первоначальных проявлений и симптомов невропатии. Диагноз ставится на основании данных тщательного медицинского обследования, изучения истории заболевания, уточнения причины болезни и степени тяжести невропатии. Неврологическое обследование, тестирование рефлексов и функции чувствительных и двигательных нервов являются важной частью диагностического процесса. Не существует специфических анализов крови, указывающих на наличие невропатии. В то же время данный тип диагностики проводится с целью уточнения причины заболевания и сопутствующих болезней (например, сахарного диабета и недостаточности витаминов группы В), играющих активную роль в повреждении нервов. Визуализирующие методы исследований, например, рентгенография, компьютерная томография, магнитно-резонансное сканирование, проводятся с целью определить, возникло ли патологическое давление на нервные волокна тела. Для определения нарушений функции нервной системы проводят следующие методики:Электромиография является исследованием функции нервов и мышц.
Лечение. Курс лечения невропатии состоит из мер для контролирования симптомов заболевания и борьбы с причиной болезни. Специализированное лечение диабета, аутоиммунных заболеваний, инфекции, болезней почек, недостаточности витаминов, другие виды терапии направлены на устранение определенной причины невропатии. Во многих случаях борьба с первопричиной помогает снизить или вовсе избавиться от симптомов вышеупомянутого заболевания. Некоторые пациенты, страдающие от механического сдавливания нервного волокна опухолью или другими структурами, требуют хирургического вмешательства. Контролирование уровня глюкозы крови является основной частью лечения диабетической невропатии и помогает предотвратить дальнейшее повреждение нервов. При лечении невропатий используют препараты следующих групп:
Во многих случаях борьба с первопричиной помогает снизить или вовсе избавиться от симптомов вышеупомянутого заболевания. Некоторые пациенты, страдающие от механического сдавливания нервного волокна опухолью или другими структурами, требуют хирургического вмешательства. Контролирование уровня глюкозы крови является основной частью лечения диабетической невропатии и помогает предотвратить дальнейшее повреждение нервов. При лечении невропатий используют препараты следующих групп:
- Антидепрессанты,
- Противосудорожные средства,
- Антиоксиданты.
- Из не медикаментозны средств в лечении невропатий большую роль играют физиотерапевтические методы лечения, иглорефлексотерапия.
Профилактика. В случае, если можно исключить возникновение причины данного заболевания, только тогда говорят о возможности предотвращения самой невропатии. Чтоб уберечься от сахарного диабета, как показывают исследования, следует строго контролировать уровень глюкозы крови. Данная мера позволит избежать развития диабетической невропатии и других осложнений. Не допустить невропатию, развивающуюся в связи с неадекватным или недостаточным приемом пищи, алкогольной зависимостью возможно, сделав все возможное для организации правильного здорового питания. Генетические и унаследованные невропатии предотвратить невозможно.
Данная мера позволит избежать развития диабетической невропатии и других осложнений. Не допустить невропатию, развивающуюся в связи с неадекватным или недостаточным приемом пищи, алкогольной зависимостью возможно, сделав все возможное для организации правильного здорового питания. Генетические и унаследованные невропатии предотвратить невозможно.
Прогноз заболевания зависит от первопричины невропатии. В случае, если к вышеупомянутой проблеме привело сопутствующее заболевание или другая причина, от которой можно избавиться лекарственными средствами, хирургическим путем, то прогноз выздоровления от невропатии отличный или очень хороший. Нерв, поврежденный патологическими процессами, требует времени для восстановления даже после избавления от первопричины. При генетических причинах невропатии лечение неэффективно. Тяжелые повреждения нервного волокна не поддаются восстановлению.
Невропатии периферических нервов. / Статьи / «Авиценна» в Волгограде
06/12/20
Невропатии периферической нервной системы.
Признаками невропатии являются:
онемение,
чувство покалывания и « парастезии»,
боли в конечности,
стреляющая боль, подобная удару электрическим током,
неприятные ощущения мурашек,
слабость мышц,
уменьшение объема мышц,
непроизвольное сокращение мышц,
двигательные нарушения,
трудности при движении,
потеря или повышение тактильной чувствительности,
Нейропатия (периферическая) – это поражение одного или нескольких периферических нервов вызванное разными причинами. Она включает в себя многочисленные синдромы.
Если поражен один нерв, то врачи называют это состояние мононевропатией, если несколько нервов, локализованных в одной зоне – множественной невропатией, если поражаются нервы в различных зонах, то говорят о полиневропатии.
Поражении нервов нарушается питание мышечной ткани и ограничиваются ее функции – мышца теряет способность нормально сокращаться, возникает гипотрофия и в последующем атрофия.
Наиболее распространённые виды невропатии:
— диабетическая (проявляется у лиц с сахарным диабетом),
— токсическая (поражаются преимущественно нервы конечностей в основном при алкоголизме, приеме препаратов и т.д.),
— посттравматическая (является следствием сдавливания нервов после переломов, при неправильном формировании рубца, а также в результате травматизации нерва новообразованием),
— невропатии, вызваны остеохондрозом позвоночника или артритом.
Симптомы невропатий варьируют в зависимости от поврежденного участка нерва и степени выраженности процесса.
Клинически невозможно определить, что происходит с нервом и какова степень выраженности процесса.
Для этого существуют два основных обследования.
Первое — нейрофизиологические исследования (исследование скорости распространения возбуждения по нервам и электромиография), которые позволяют установить примерную локализацию поражения и определить, является ли оно преимущественно аксональным или демиелинизирующим.
Второе – УЗИ исследование, которое определяет нарушения структуры в нерве.
Ультразвуковое исследование (УЗИ) оценивает: точное место изменения ствола нерва, вид нарушения нерва и причины, по которым это произошло (воспаление, частичное повреждение нерва, полный разрыв, опухоль нерва и другие). Данное исследование позволяет понять, какие следует применять меры для лечения — консервативное или операция.
Достоинства УЗИ:
Безопасность и безвредность исследования.
Возможность многократного динамического проведения исследования.
Отсутствие предварительной подготовки больного.
Возможность визуализировать ствол нерва с дифференциацией на пучки.
Возможность визуализировать причину , которая изменяет структуру ствола нерва.
Возможность исследования при наличии металлоконструкций в теле человека.
С помощью УЗИ мы можем оценить:
— Плечевое сплетение
— Срединный нерв
— Локтевой нерв
— Лучевой нерв
— Пальцевые нервы кисты
— Бедренный нерв
— Седалищный нерв
— Большеберцовый нерв
— Общий малоберцовый нерв
На конечностях можно оценить нервы в тех местах, где они сужаются, что может свидетельствовать о туннельной невропатии:
— компрессия срединного нерва (синдром карпального канала на уровне лучезапястного сустава и на уровне локтевой ямки — компрессия мышцей),
— компрессия локтевого нерва (с-м кубитального канала — локтевой сустав и канал Гийона- лучезапястный сустав),
— компрессия лучевого нерва (с-м спирального канала — это средняя треть плеча, канал супинатора-это верхняя треть предплечья ),
— компрессия седалищного нерва (на уровне ягодичной области),
— компрессия малоберцового нерва (на уровне верхней трети голени),
— компрессия пальцевого нерва стопы(невринома Мортона),
— компрессия плечевого сплетения на уровне надключичной и подключичной области.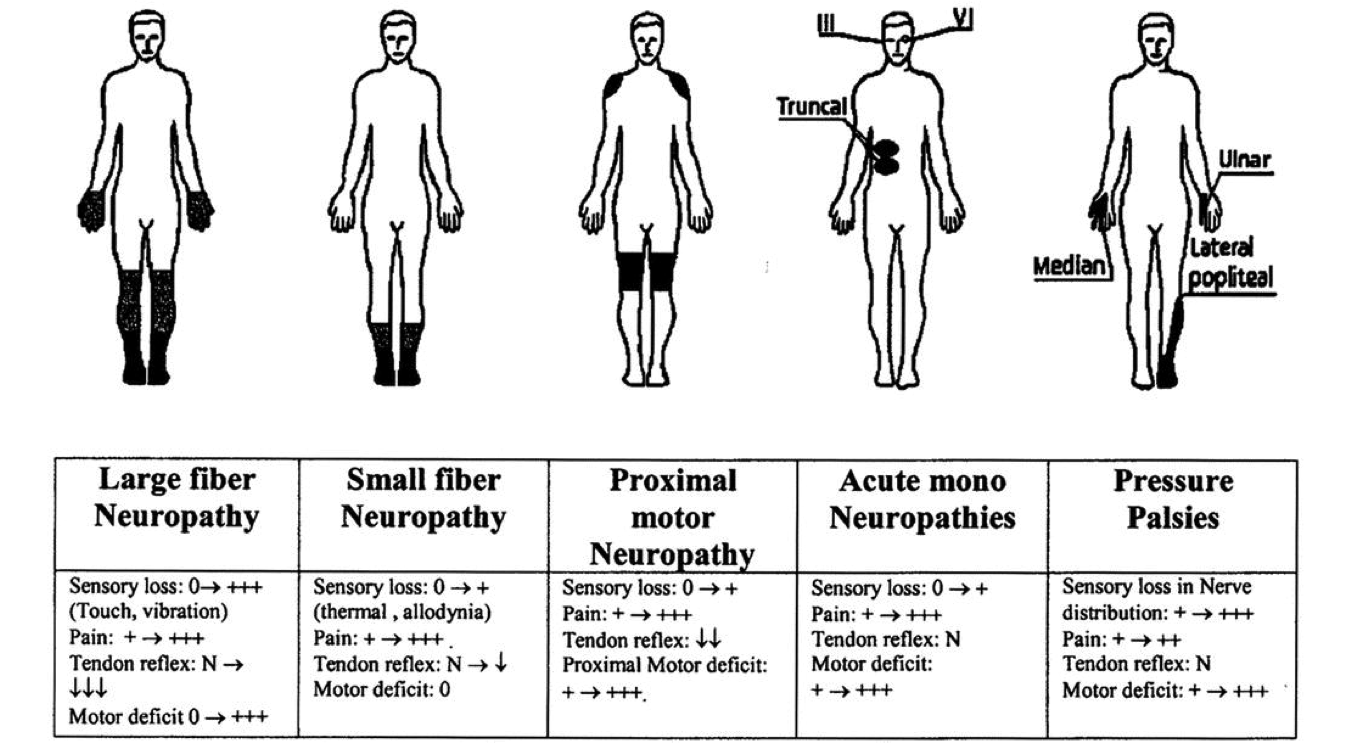
Лечение нейропатии производится врачом неврологом или нейрохирургом. Однако при отсутствии полной информации о состоянии нерва, грамотное лечение провести практически невозможно.
В нашей клинике врач УЗИ занимается диагностикой периферических нервов уже на протяжении 7 лет. Довольно часто патология нервов сочетается с изменениями суставов, мышц, мягких тканей. Подобными проблемами с опорно-двигательным аппаратом врач занимается уже более 20 лет.
Это исследование одно из самых сложных в ультразвуковой диагностике и требует высокого класса оборудования, которое имеется в нашей клинике.
Зачастую нейропатии развиваются в течение длительного времени, иногда годами оставаясь бессимптомными. Проявление симптомов могут спровоцировать такие факторы, как стресс, употребление алкоголя, обострение хронического заболевания.
Берегите себя и свое здоровье!
Болевые синдромы при полиневропатии: дифференцированный подход к диагностике и лечению | #11/16
В современной русскоязычной научно-медицинской литературе невропатиями принято называть заболевания нервной системы с преимущественным поражением периферических нервов. Традиционно выделяют мононевропатии, обусловленные вовлечением одного из периферических нервов и проявляющиеся клиническими симптомами и признаками, строго соответствующими известным зонам иннервации. Формы, обусловленные множественным (системным) поражением периферических нервов, называют полиневропатиями (ПНП) [1].
Традиционно выделяют мононевропатии, обусловленные вовлечением одного из периферических нервов и проявляющиеся клиническими симптомами и признаками, строго соответствующими известным зонам иннервации. Формы, обусловленные множественным (системным) поражением периферических нервов, называют полиневропатиями (ПНП) [1].
Термин «нейропатия» обычно используют как синоним «невропатии», однако некоторые зарубежные авторы подразумевают под нейропатией не только вовлечение аксонов и миелиновой оболочки периферических нервов, но и нейронов, что, на наш взгляд, не корректно (поражение нейронов в классической невропатологии принято называть нейронопатией).
Согласно данным европейских регистров, общая распространенность периферических невропатий в популяциях составляет в среднем 2400 × 10-5, а среди лиц пожилого возраста достигает 8000 × 10-5. Первичная заболеваемость невропатиями обычно не превышает 40 × 10-5 в год [3]. В России диагноз полиневропатии регистрируют не менее чем у 60% пациентов с признаками поражения периферической нервной системы [4].
В МКБ-10 мононевропатии относят к рубрикам G50-G53, G56-G59, полиневропатии — к рубрикам G60 (наследственные и идиопатические), G63 (воспалительные) и G63 (другие) [5], что очевидно не отражает многообразия форм и причин развития этой патологии.
В настоящее время отсутствует единая и удобная клиническая классификация ПНП.
По характеру клинической картины выделяют моторные, сенсорные, вегетативные и смешанные формы ПНП.
В зависимости от течения заболевания ПНП классифицируют на острые, подострые и хронические.
Согласно электронейромиографии (ЭНМГ) различают: 1) аксональные, характеризующиеся снижением амплитуды М-ответа при нормальной или незначительно сниженной скорости проведения импульса (СПИ) по нервам; 2) демиелинизирующие, характеризующиеся снижением СПИ по моторным и/или сенсорным волокнам; 3) смешанные (аксонально-демиелинизирующие) ПНП.
В соответствии с этиологией выделяют идиопатические ПНП, значительная часть которых генетически детерминирована, этиология других форм остается неизвестной./58/1.png)
Для обозначения ПНП, являющихся проявлением или осложнением других известных медицине заболеваний (инфекционные, эндокринные, онкологические заболевания, диффузные болезни соединительной ткани (ДБСТ), экзогенные интоксикации, заболевания внутренних органов и др.), не существует единого термина, однако по сути они являются вторичными (симптоматическими). Именно эта патология периферической нервной системы является одним из наиболее частых поводов обращения пациентов к врачам различных специальностей.
В зарубежной литературе используют понятие «болевые невропатии» и активно рассматривают проблемы купирования нейропатической боли [2]. Однако надо иметь в виду, что, с одной стороны, любое поражение периферических нервов так или иначе проявляется или сопровождается болью (для одних форм боль — обязательное проявление и критерий диагностики, для других — осложнение, вызванное прогрессированием заболевания с развитием мышечно-тонических нарушений, контрактур, деформаций скелета и др. ), с другой стороны, не всегда боль (в силу указанных выше причин) при невропатии является нейропатической.
), с другой стороны, не всегда боль (в силу указанных выше причин) при невропатии является нейропатической.
Согласно классическим канонам невропатологии, ПНП характеризуются наличием нарушений чувствительности по полинейропатическому типу и болевым синдромом, преимущественно выраженными в дистальных отделах конечностей; слабости мышц, ограничения амплитуды движений в конечностях и двигательной активности в целом (в т. ч. нарушением ходьбы), сопровождающихся атрофией и гипотонией мышц, угасанием сухожильных и периостальных рефлексов, а также вегетативных нарушений. Одними из ключевых критериев, позволяющих диагностировать ПНП, является преимущественное поражение дистальных отделов конечностей и относительная симметричность патологического процесса.
Диагностика ПНП как синдрома (топическая) обычно не вызывает значительных клинических сложностей, однако нередко возникают затруднения при определении этиологии и нозологической принадлежности ПНП. Так, даже при тщательном (в т. ч. нейрофизиологическом) обследовании в специализированных европейских клиниках причина ПНП остается не установленной примерно в 25% случаев, а в медицинских учреждениях общего профиля затруднения в определении нозологического диагноза возникают при обследовании 50% больных [6, 7].
ч. нейрофизиологическом) обследовании в специализированных европейских клиниках причина ПНП остается не установленной примерно в 25% случаев, а в медицинских учреждениях общего профиля затруднения в определении нозологического диагноза возникают при обследовании 50% больных [6, 7].
В силу вариабельности клинических проявлений ПНП, в перечень для дифференциальной диагностики приходится включать значительное число других нервно-мышечных заболеваний, таких как радикулопатия, миастения, нейронопатия и другие. Особые трудности возникают при обследовании лиц пожилого возраста, поскольку более 90% из них страдают коморбидной патологией, такой как сахарный диабет, заболевания щитовидной железы и онкологические заболевания. Не меньшие сложности испытывают доктора в процессе лечения ВИЧ-инфицированных лиц, страдающих оппортунистическими заболеваниями.
В настоящее время известно не менее 200 причин развития ПНП, среди которых интоксикации (воздействие промышленных токсинов и солей тяжелых металлов, употребление наркотических препаратов и злоупотребление алкоголем), инфекции (вирусные, такие как ВИЧ, и бактериальные, такие как бруцеллез), системные заболевания соединительной ткани, дефицит витаминов, особенно группы В (В6, В12), злокачественные новообразования (лейкозы, лимфогранулематоз и др. ), эндокринные заболевания (заболевания щитовидной железы, сахарный диабет и др.), ятрогенное воздействие лекарственных препаратов (антибактериальных, в т. ч. противотуберкулезных, и антиретровирусных препаратов, антиаритмических и гиполипидемических средств и др.), сывороток и вакцин [8].
), эндокринные заболевания (заболевания щитовидной железы, сахарный диабет и др.), ятрогенное воздействие лекарственных препаратов (антибактериальных, в т. ч. противотуберкулезных, и антиретровирусных препаратов, антиаритмических и гиполипидемических средств и др.), сывороток и вакцин [8].
Боль является одной из наиболее частых причин обращения пациентов с ПНП к доктору. По результатам исследования EPIC, проведенного в 2008 г., выявлено, что из всех пациентов, амбулаторно обратившихся к неврологам, 39% обращались по поводу болевого синдрома, а 18% предъявляли жалобы, характерные для проявлений нейропатии [9].
Боль при ПНП наиболее часто носит нейропатический характер, однако она может быть и ноцицептивной, и смешанной.
Наиболее часто в клинической практике встречаются дисметаболические ПНП, среди которых значительно преобладает диабетическая. Среди пациентов с сахарным диабетом ПНП диагностируют более чем в 50% случаев [10, 11]. Хроническая нейропатическая боль выявляется у 16–26% пациентов при сахарном диабете.
Патогенез боли при различных дисметаболических ПНП аналогичен, но наиболее изучен на модели поражения периферических нервов при сахарном диабете.
Одним из основных механизмов нейропатической боли является повышение возбудимости мембран нервных волокон, связанное с повышением экспрессии потенциал-зависимых натриевых каналов [12]. В ходе ряда экспериментов установлено, что в поддерживании нейропатической боли важную роль играют патологические взаимодействия периферических сенсорных волокон: при дегенерации эфферентных волокон нерва отмечается спонтанная эктопическая нейрональная активность в интактных С-волокнах, сенситизация нейронов на фоне экспрессии цитокинов и нейротрофических факторов. Сенситизация нервных волокон, возникновение термической гипералгезии обусловлены действием серотонина. Возникновение боли при этом связывают с работой основных натриевых каналов: Nav1.3, Nav1.7, Nav1.8 и Nav1.9 [13]. Увеличение численности Na-каналов способствует развитию воспаления и вторичной центральной сенситизации.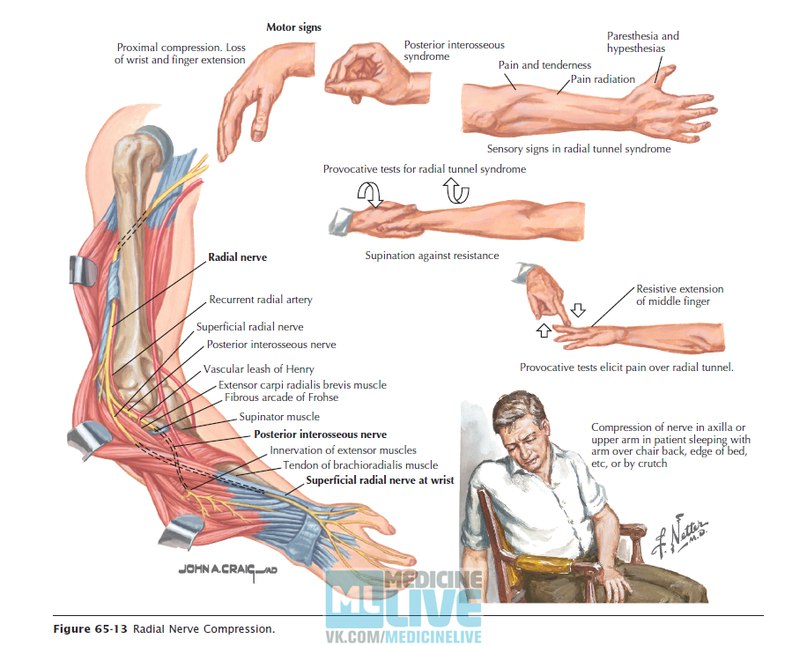 Показано, что каналы Nav1.7, Nav1.8, Nav1.9 экспрессированы на тонких ноцицептивных волокнах и участвуют в проведении болевой афферентации [14–17]. Повышенная экспрессия каналов Nav1.3, которые в норме у взрослых лишь в небольшой степени представлены в периферической нервной системе, и Nav 1.6 может играть важную роль в повышении возбудимости нейронов и развитии нейропатической боли при повреждении периферических нервов и спинного мозга [18, 19].
Показано, что каналы Nav1.7, Nav1.8, Nav1.9 экспрессированы на тонких ноцицептивных волокнах и участвуют в проведении болевой афферентации [14–17]. Повышенная экспрессия каналов Nav1.3, которые в норме у взрослых лишь в небольшой степени представлены в периферической нервной системе, и Nav 1.6 может играть важную роль в повышении возбудимости нейронов и развитии нейропатической боли при повреждении периферических нервов и спинного мозга [18, 19].
Другой механизм развития боли при ПНП обусловлен повреждением Aδ- и C-волокон [20, 21]. При нейропатической боли определяется более низкий порог активации Аβ- и Аδ-волокон на механическую стимуляцию, а также отмечается увеличение спонтанной активности в С-волокнах. Установлено, что аллодиния, возникающая при диабетической ПНП, является следствием гибели С-волокон с дальнейшей центральной сенситизацией, а повреждение Аδ-волокон, воспринимающих холодовые стимулы, ведет к холодовой гипералгезии.
Имеются данные об увеличении высвобождения нейротрансмиттеров при активации вольтажзависимых кальциевых каналов. Установлено, что у пациентов с сахарным диабетом отмечается увеличение плотности кальциевых каналов с α2Δ-1 субъединицей, что обуславливает развитие аллодинии.
Установлено, что у пациентов с сахарным диабетом отмечается увеличение плотности кальциевых каналов с α2Δ-1 субъединицей, что обуславливает развитие аллодинии.
В ряде экспериментальных работ показано, что при сахарном диабете интенсивность боли обусловлена быстрой активацией как MARK-киназы (the mitogen-activated protein kinase), так и внеклеточной сигнал-зависимой киназы — компонента ERK-каскада (extracellular signal-regulated protein kinase) не только в поврежденных, но и в интактных нейронах [22].
Среди токсических преобладает алкогольная ПНП, выявляющаяся у 12–30% пациентов, наблюдающихся по поводу хронического алкоголизма [23]. При проведении ЭНМГ ПНП выявляется у 97–100% больных, хронически злоупотребляющих алкоголем [24]. Механизм развития ПНП обусловлен токсическим действием ацетальдегида и пировиноградной кислоты, приводящим к аксональной дегенерации, а в патогенезе демиелинизации основное значение имеет дефицит витаминов группы В и никотиновой кислоты [25]. Поражение тонких волокон при алкогольной ПНП приводит к избирательной потере болевой или температурной чувствительности, парестезиям, дизестезиям, спонтанной боли.
Поражение тонких волокон при алкогольной ПНП приводит к избирательной потере болевой или температурной чувствительности, парестезиям, дизестезиям, спонтанной боли.
Другой разновидностью токсических являются ПНП, обусловленные применением химиотерапии. Наиболее часто поражение периферических нервов развивается при применении винкристина, цисплатина, оксалиплатина и карбоплатина [26].
Патофизиология нейропатических нарушений наиболее изучена на экспериментальных моделях винкристиновой ПНП, при назначении которого в патогенезе болевого синдрома важную роль играет активация протеинкиназ А и С, оксида азота, способствующих возникновению механической гипералгезии [27].
Кроме того, экзогенные токсические полинейропатии могут быть следствием интоксикации солями тяжелых металлов, органическими, в том числе и фосфорорганическими, соединениями и лекарственными препаратами. В основе патологического процесса лежит аксональная дегенерация, а вторичная демиелинизация чаще всего имеет сегментарный характер и менее выражена.
Среди больных соматической патологией наиболее часто клинические признаки ПНП выявляют при тяжелых хронических заболеваниях печени, почек, желудочно-кишечного тракта, легких. Так, при билиарном циррозе ПНП диагностируется у 60–70% больных. Уремическую ПНП выявляют почти у 50% больных с хронической почечной недостаточностью [28, 29]. При заболеваниях желудочно-кишечного тракта, сопровождающихся нарушением питания и мальабсорбцией, развитие ПНП часто связано с дефицитом витаминов группы В [30, 31].
Среди пациентов, страдающих инфекционными заболеваниями, ПНП наиболее часто возникает у ВИЧ-инфицированных. Различные варианты периферической нейропатии клинически проявляются у 20–35% больных ВИЧ, а при аутопсии признаки поражения периферических нервов обнаруживают в 95% случаев [32]. Механизм боли преимущественно связан с поражением C-волокон, опосредующих восприятие тепловых стимулов [33], а также непосредственным токсическим действием антиретровирусных препаратов.
При воспалительных полинейропатиях боль является следствием поражения аксонов на фоне нарушения распределения натриевых каналов и выброса воспалительных медиаторов, что приводит к раздражению ноцицептивных рецепторов. В данном случае боль обусловлена повышением уровня циклооксигеназы-2, ПГ2 как в нейронах дорсального ганглия, так и задних рогах спинного мозга [34, 35].
В данном случае боль обусловлена повышением уровня циклооксигеназы-2, ПГ2 как в нейронах дорсального ганглия, так и задних рогах спинного мозга [34, 35].
Среди идиопатических воспалительных наиболее часто встречается острая воспалительная демиелинизирующая полирадикулонейропатия (ОВДП, синдром Guillain–Barré). Заболеваемость ОВДП составляет 1,1–1,8 × 10-5 и возрастает с увеличением возраста: у лиц до 16 лет она составляет 0,4–1,4-5, а у лиц старше 60 лет — 3,3 × 10-5 в год [36, 37].
Нейропатическая боль при васкулитах и ДБСТ также обусловлена увеличением экспрессии провоспалительных цитокинов в периферических нервах [38]. Частота возникновения ПНП при различных формах ДБСТ различна. Так, у пациентов с системной красной волчанкой ПНП развивается в 8–56% случаев; при ревматоидном артрите ПНП диагностируют практически у всех пациентов; при системной склеродермии и синдроме Шегрена — у 5–10% больных, при саркоидозе — у 5–15% пациентов [39–43].
Паранеопластические ПНП составляют около 1% всех ПНП и встречаются приблизительно у 5% больных с онкологическими заболеваниями [44]. Наиболее часто ПНП возникают у больных раком легких или дыхательных путей — 2,5–5,5% случаев, при миеломной болезни — в 5%. По данным ЭНМГ, изменения периферических нервов обнаруживают почти у 30% пациентов с впервые установленным диагнозом онкологического заболевания [45–47]. В таких случаях ПНП не связана со сдавлением нервов опухолью, метастатическим поражением нервной ткани или побочными эффектами химиотерапии и лучевой терапии, метаболическими, сосудистыми, гормональными изменениями. В ходе исследований выявлена связь паранеопластических синдромов с определенным типом онконевральных антител к антигенам Hu, CV2 [48, 49].
Около 25% случаев нейропатических нарушений неясной этиологии обусловлены наследственными ПНП. Среди которых выделяют наследственные моторно-сенсорные нейропатии (НМСН) и ряд ПНП, встречающихся при других наследственных заболеваниях.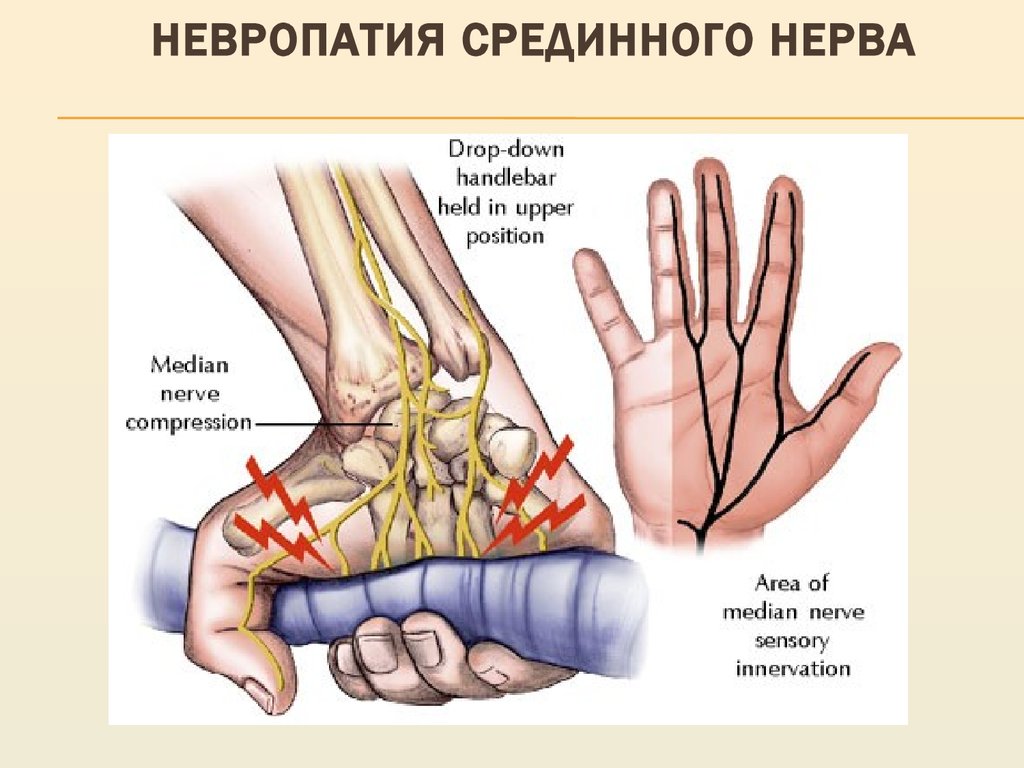 Наличие метаболического дефекта выявлено при некоторых наследственных ПНП: метахроматической лейкодистрофии, болезни Фабри, болезни Рефсума, болезни Бассейна–Корнцвейга и некоторых других.
Наличие метаболического дефекта выявлено при некоторых наследственных ПНП: метахроматической лейкодистрофии, болезни Фабри, болезни Рефсума, болезни Бассейна–Корнцвейга и некоторых других.
При болезни Фабри — врожденном заболевании, характеризующемся наследственным дефицитом фермента альфа-G4-галактозидазы, ПНП обусловлена отложением сфингогликолипидов и гликопротеидов в тканях и нервных ганглиях. Нейропатическая боль является одним из ведущих клинических синдромов. Боль носит характер «кризов», в виде приступов интенсивных мучительных жгучих болей в руках и ногах, с иррадиацией в другие части тела, продолжительностью от нескольких минут до нескольких дней, лихорадки, каузалгии.
Прогрессирующая болевая ПНП встречается у пациентов при семейном варианте амилоидоза, парапротеинемиях и в 10% случаев первичного амилоидоза [50]. В настоящее время описано более 40 мутаций белка транстиретина (Amiloid-Transtiretin — A-TTR), ассоциированных с отложением амилоидных включений, которые выявляются при биопсии нервов.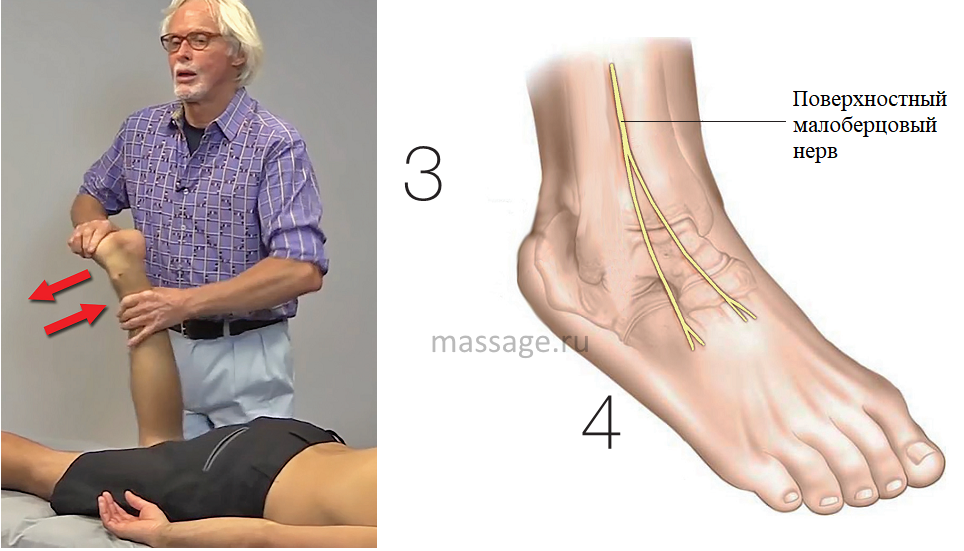
ПНП, как правило, имеют хроническое течение, медленно прогрессируя на протяжении нескольких лет. Во многих случаях своевременно установить правильный нозологический диагноз и назначить адекватное лечение ПНП можно, применяя пошаговые алгоритмы с анализом анамнестических сведений, результатов осмотра и доступных лабораторных исследований (рис.).
Прежде всего больного следует расспросить о злоупотреблении алкоголем, воздействии токсических веществ и приеме лекарственных препаратов. В случае выявления показаний пациента необходимо направлять на консультацию к психиатру-наркологу. При подозрении на наличие нежелательных явлений лекарственных препаратов важно своевременно провести коррекцию терапии (шаг 1).
Устранение этиологических факторов при токсической ПНП позволяет надеяться на значительное улучшение состояния пациента. Патогенетическое лечение может включать дезинтоксикационную терапию, препараты тиоктовой кислоты (при алкогольной ПНП), витамины группы В (при ПНП, вызванной употреблением алкоголя, противотуберкулезных препаратов и др.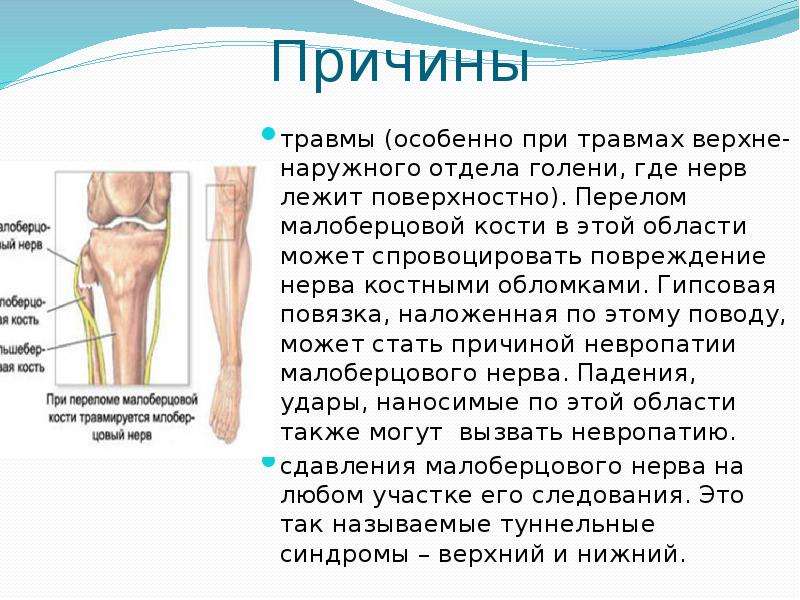 ). Симптоматическое лечение направлено на купирование боли.
). Симптоматическое лечение направлено на купирование боли.
Следующим шагом необходимо оценить соматическое состояние пациента и, с учетом анамнеза и жалоб, назначить обследование с целью исключения инфекционной патологии (в первую очередь — ВИЧ-инфекции, сифилиса, бруцеллеза, боррелиоза). При выявлении инфекционного заболевания пациента необходимо направить к профильным специалистам (шаг 2).
Своевременное и адекватное этиотропное лечение (специфическая антиретровирусная или антибактериальная терапия) позволяет в ряде случаев добиться улучшения или стабилизации состояния больного. Патогенетическая терапия является вспомогательной и недифференцированной. Симптоматическое лечение (купирование боли) может потребоваться в начале этиотропной терапии или на терминальных стадиях заболеваний. При ВИЧ-ассоциированных ПНП в случаях незначительной боли предлагают использовать ацетаминофен, нестероидные противовоспалительные препараты (НПВП) в сочетании с гастропротекторами (ингибиторами протонной помпы), при умеренной боли — НПВП в сочетании с легкими опиоидными анальгетиками, при сильной боли — опиоидные анальгетики. В качестве адъювантной терапии рекомендуют антидепрессанты и (или) антиконвульсанты [51].
В качестве адъювантной терапии рекомендуют антидепрессанты и (или) антиконвульсанты [51].
С целью скрининга эндокринных заболеваний и патологии внутренних органов при выявлении симптомов и признаков ПНП в рутинной практике рекомендуют: общий клинический анализ крови, общий анализ мочи, биохимический анализ, позволяющий оценить функцию печени и почек, определение уровня гликемии, Т3 и тиреотропного гормона, витамина В12 и фолиевой кислоты. В случае отклонения результатов лабораторных анализов от референсных значений пациент должен быть проконсультирован терапевтом или эндокринологом с целью уточнения этиологического диагноза для последующего назначения или коррекции уже имеющейся терапии (шаг 3). При необходимости обследование дополняют определением уровня HbA1с, тестом на толерантность к глюкозе.
Если причина ясна и клиническая картина типична для определенной формы ПНП (например, при диабетической ПНП), соответствующее патогенетическое лечение в дополнение к этиотропному (например, заместительной терапии инсулином при сахарном диабете) может быть начато без дальнейшего обследования и включать препараты тиоктовой кислоты (при диабетической ПНП), витамины группы В (при ПНП, возникшей на фоне дефицита витамина В12). Симптоматическое лечение направлено на купирование боли. Наиболее эффективным считается назначение антиконвульсантов, достаточно эффективны — антидепрессанты, капсаицин, чрескожная стимуляция нервов.
Симптоматическое лечение направлено на купирование боли. Наиболее эффективным считается назначение антиконвульсантов, достаточно эффективны — антидепрессанты, капсаицин, чрескожная стимуляция нервов.
Если причина ПНП по-прежнему не ясна, в дальнейшем необходимо предпринять попытку провести поиск онкологических заболеваний, ДБСТ и иной соматической патологии.
Зарубежные авторы рекомендуют включать в план обследования электрофорез белков сыворотки крови и мочи с иммунофиксацией, исследование активности ангиотензин-превращающего фермента, определение уровня антинуклеарных антител (АТ), Р-ANCA, С-ANCA, исследование на наличие паранеопластических АТ (anti-Hu, anti-Yo, anti-Ri, anti-Tr, anti-Ma, anti-CV2), антисульфатидных АТ, криоглобулинов, компьютерную томографию органов грудной клетки и брюшной полости, при необходимости выполнить позитронно-эмиссионную томографию [3, 8].
Однако, прежде чем проводить указанное выше углубленное обследование, необходимо исключить наследственный характер ПНП. При указании на повторные случаи в семье заболеваний со сходной клинической картиной необходимо проведение медико-генетического консультирования, включающего консультацию генетиком и молекулярно-генетические исследования, доступные в настоящее время (шаг 4). В спорадических случаях углубленное медико-генетическое консультирование может быть проведено параллельно с обследованием внутренних органов.
При указании на повторные случаи в семье заболеваний со сходной клинической картиной необходимо проведение медико-генетического консультирования, включающего консультацию генетиком и молекулярно-генетические исследования, доступные в настоящее время (шаг 4). В спорадических случаях углубленное медико-генетическое консультирование может быть проведено параллельно с обследованием внутренних органов.
К сожалению, в большинстве случаев генетически детерминированных заболеваний патогенетическое лечение не разработано, а симптоматическая терапия недостаточно эффективна. Исключение составляют единичные заболевания, например, болезни Фабри. При своевременной диагностике заболевания и раннем назначении заместительной ферментной терапии (агалсидаза бета) можно рассчитывать на стабилизацию состояния больного и уменьшение боли.
Если причина ПНП остается не ясной или клиническая картина заболевания атипична, обязательным является выполнение электронейромиографии [6, 8]. Основные задачи нейрофизиолога: определить уровень (распространенность), характер (аксональный, демиелинизирующий или смешанный) и выраженность поражения периферических нервов (шаг 5).
Аксональная ПНП, согласно результатам ЭНМГ, может быть сенсорной или моторно-сенсорной. Среди причин, большинство из которых можно уточнить при сборе анамнестических сведений, наиболее частыми являются заболевания щитовидной железы и сахарный диабет, алкогольная и другие интоксикации, дефицит витаминов группы В. Значительно реже аксональные ПНП развиваются вследствие интоксикации солями тяжелых металлов, порфирии, паранеопластическом синдроме. Хроническая аксональная ПНП может быть идиопатической (наследственная моторно-сенсорная нейропатия II типа) или вторичной (ПНП при мультисистемных заболеваниях).
В случае выявления по данным ЭНМГ изменений демиелинизирующего характера, крайне важно оценить симметричность патологического процесса. Если снижение скорости проведения импульсов обнаружено при анализе ЭНМГ всех исследованных нервов, следует заподозрить наследственную моторно-сенсорную нейропатию I типа и направить пациента для проведения медико-генетического консультирования.
Иная ЭНМГ-картина наблюдается при демиелинизирующих воспалительных ПНП. Для хронической воспалительной демиелинизирующей полиневропатии характерны мультифокальные нарушения с частичным блоком проведения по моторным нервам.
В случае выявления воспалительной ПНП должно быть начато адекватное патогенетическое лечение — согласно отечественным и Европейской федерации неврологических сообществ (European Federation of Neurological Societies, EFNS) рекомендациям, курсовое внутривенное введение IgG (ВВИГ) и (или) плазмаферез. При хронической ВДП в дополнение возможно назначение кортикостероидов. Важное значение для верификации диагноза ВДП имеет динамическое наблюдение, включающее оценку изменения клинических и ЭНМГ-признаков в ответ на лечение, исследование цереброспинальной жидкости, определение anti-МАG IgM, АТ к ганглиозидам [8]. Симптоматическая терапия направлена на купирование боли и включает антиконвульсанты, НПВП и (или) легкие опиоидные анальгетики.
В 10% случаев демиелинизирующая ПНП обусловлена парапротеинемией.
Если в ходе диагностики так и не удается установить причину ПНП, рекомендуют провести гистологическое исследование биоптата нерва. Чаще всего в таких случаях обнаруживают признаки васкулита.
Однако, даже после выполнения всего спектра доступных современной медицине обследований, в 25% случаев причина ПНП по-прежнему остается неизвестной. Идиопатические хронические формы заболевания чаще всего наблюдают у лиц пожилого возраста, они представляют собой сенсорные медленно прогрессирующие ПНП.
Во всех случаях ПНП одним из важнейших направлений лечения является немедикаментозная реабилитация, которая направлена на сохранение или восстановление функции ходьбы и включает активную и пассивную лечебную физкультуру (ЛФК) под контролем методиста и врача ЛФК, массаж с целью профилактики контрактур; профилактику пролежней, гипостатической пневмонии, тромбозов глубоких вен; контроль и коррекцию нарушений глотания, дыхания, состояния функций мочевого пузыря и желудочно-кишечного тракта.
Анализ отечественной и зарубежной литературы показывает, что в настоящее время отсутствует единый подход к классификации и тактике ведения пациентов с ПНП. Учитывая высокую распространенность ПНП и значительный фенотипический полиморфизм, для практического здравоохранения крайне важно наличие простого доступного алгоритма диагностики и лечения, который бы позволял в условиях многопрофильных медицинских учреждений рационально планировать мероприятия по обследованию и реабилитации больных ПНП.
Литература
- Неврология. Национальное руководство / Под ред. Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой, А. Б. Гехт. М.: ГЭОТАР-Медиа. 2010: 1040. ISBN: 978–5-9704–0665–6.
- Marchettini P., Lacerenza M., Mauri E., Marangoni C. Painful Peripheral Neuropathies // Current Neuropharmacology. 2006; 4: 175–181.
- Hughes R. A. Clinical review: peripheral neuropathy // BMJ. 2002; 324: 466–469.
-
Жулев Н.
 М. Невропатии. Руководство для врачей / Под ред. Н. М. Жулева. СПб: СПбМАПО, 2005. 416 c.
М. Невропатии. Руководство для врачей / Под ред. Н. М. Жулева. СПб: СПбМАПО, 2005. 416 c. - http://apps.who.int/classifications/icd10/browse/2015/en#/G60-G64 (дата обращения: 25.09.2016).
- Imreova H., Pura M. Differential diagnosis of peripheral neuropathy // Cas Lek Cesk. 2005; 144 (9): 628–635.
- Smith A. G., Singleton J. R. The Diagnostic yield of a standardized approachto idiopathic sensory-predominant neuropathy // Arch Intern Med. 2004; 164: 1021–1025.
- Azhary H., Farooq M. U., Bhanushali M. et al. Peripheral neuropathy: differential diagnosis and management // Am Fam Physician. 2010; 81 (7): 887–892.
- Яхно Н. Н., Кукушкин М. Л., Давыдов О. С. и др. Результаты Российского эпидемиологического исследования распространенности невропатической боли (EPIC Study). Лечение невропатической боли // Consilium medicum. Неврология 2008; 2: 64–70.
-
Bhadada S. K., Sahay R.
 K., Jyotsna V. P. et al. Diabetic Neuropathy: Current Concepts // Journal of Indian Academy of Clinical Medicine. 2001; 2: 304–318.
K., Jyotsna V. P. et al. Diabetic Neuropathy: Current Concepts // Journal of Indian Academy of Clinical Medicine. 2001; 2: 304–318. - Kaur S., Pandhi P., Dutta P. Painful diabetic neuropathy: an update // Annals of Neurosciences. 2011; 18 (4): 168–175.
- Dworkin R. H. Advances in neuropathic pain // Arch. Neurol. 2003; 60: 1524–1534.
- Craner M. J., Klein J. P., Renganathan M. et al. Changes of sodium channel expression in experimental painful diabetic neuropathy // Annals of Neurosciences. 2002; 52: 786–792.
- Minett M. S., Falk S., Santana-Varela S. et al. Pain without Nociceptors? Nav1.7-Independent Pain Mechanisms // Cell Reports. 2014; 6 (2): 301–312.
- Thakor D. K., Lin A., Matsuka Y. et al. Increased peripheral nerve excitability and local NaV1.8 mRNA up-regulation in painful neuropathy // Molecular Pain. 2009; 5: 14.
- Ahn H. S., Black J. A., Zhao P. et al. Nav1.7 is the predominant sodium channel in rodent olfactory sensory neurons // Molecular Pain. 2011; 7: 32.
- Huang J., Han C., Estacion M. et al. Gain-of-function mutations in sodium channel Na (v)1.9 in painful neuropathy // Brain. 2014; 137 (6): 1627–1642.
- Sittl R., Lampert A., Huth T. et al. Anticancer drug oxaliplatin induces acute cooling-aggravated neuropathy via sodium channel subtype NaV1.6-resurgent and persistent current // Proceedings of the National Academy of Sciences of the United States of America. 2012; 109 (17): 6704–6709.
- Alessandri-Haber N., Alcaraz G., Deleuze C. et al. Molecular determinants of emerging excitability in rat embryonic motoneurons // The Journal of Physiology. 2002; 541 (1): 25–39.
- Строков И. А., Баринов А. Н. Клиника, патогенез и лечение болевого синдрома при диабетической полиневропатии // Неврологический журнал. 2001; 6: 47–54.
- Vinik A. I., Mehrabyan A. Diabetic neuropathies // Med Clin North Am. 2004; 88: 947–999.
- Schafers M., Lee D. H., Brors D. et al. Increased sensitivity of injured and adjacent uninjured rat primary sensory neurons to exogenous tumor necrosis factor-alpha after spinal nerve ligation // J. Neuroscience. 2003; 23: 3028–3038.
- Beghi E., Monticelli M. L. Chronic symmetric symptomatic polyneuropathy in the elderly: a field screening investigation of risk factors for polyneuropathy in two Italian communities // J. Clin. Epidemiol. 1998; 51: 697–702.
- Dyck P. J., Thomas P. K. Peripheral neuropathy. W. B. Saunders Company. 1984; 2: 1912–1931.
- Koike H., Iijima M., Sugiura M. et al. Alcoholic neuropathy is clinicopathologically distinct from thiamine-deficiency neuropathy // Ann Neurol. 2003; 54 (1): 19–29.
- Quasthoff S., Hartung H. P. Chemotherapy-induced peripheral neuropathy // J. Neurol. 2002; 249: 9–17.
- Aley K. O., Levine J. D. Different peripheral mechanisms mediate enhanced nociception in metabolic/toxic and traumatic painful peripheral neuropathies in the rat // Neuroscience. 2002; 111: 389–397.
- Bolton C. F. Peripheral Neurophathies Associated With Chronic Renal Failure // Canadian Journal of Neurological Sciences. 1980; 7: 89–96.
- Janda K., Stompor T., Gryz E. et al. Evaluation of polyneuropathy severity in chronic renal failure patients on continuous ambulatory peritoneal dialysis or on maintenance hemodialysis // Przegl Lek. 2007; 64 (6): 423–430.
- McCombe P. A., McLeod J. G. The peripheral neuropathy of vitamin B 12 deficiency // Journal of the neurological sciences. 1984; 66: 117–126.
- Koike H., Misu K., Hattori N. et al. Postgastrectomy polyneuropathy with thiamine deficiency. J. Neurol Neurosurg Psychiatry. 2001; 71: 357–362.
- Estanislao L., Hart P., Simpson D. HIV neuropathy and selected infectious neuropathies // Continuum. 2003; 9 (6): 118–145.
- Martin C., Solders G., Sonnerborg A. et al. Painful and non-painful neuropathy in HIV-infected patients: an analysis of somatosensory nerve function // Eur. J. Pain. 2003; 7: 23–31.
- Ma W., Eisenach J. C. Morphological and pharmacological evidence for the role of peripheral prostaglandins in the pathogenesis of neuropathic pain // Eur. J. Neuroscience. 2002; 15: 1037–1047.
- Ma W., Du W., Eisenach J. C. Role for both spinal cord COX-1 and COX-2 in maintenance of mechanical hypersensitivity following peripheral nerve injury // Brain Res. 2002; 937: 94–99.
- Hughes R. A., Rees J. H. Clinical and epidemiologic features of Guillain-Barre syndrome // J. Infect Dis. 1997; 176: 92–98.
- McGrogan A., Madle G. C., Seaman H. E. et al. The epidemiology of Guillain-Barré syndrome worldwide. A systematic literature review // Neuroepidemiology 2009; 32 (2): 150–163.
- Heuss D., Schlotter-Weigel B., Sommer C. Diagnosis and therapy of vasculitic neuropathy // Fortschr Neurol Psychiatr. 2003; 71: 172–186.
- Bougea A., Anagnostou Konstantinos G. et al. A systematic review of peripheral and central nervous system involvement of rheumatoid arthritis, systemic lupus erythematosuS., primary Sjogren’s syndrome, and associated immunological profiles // International Journal of Chronic Diseases. 2015; 2015: 910352.
- Agarwal V., Singh R., Wiclaf et al. A clinical, electrophysiological, and pathological study of neuropathy in rheumatoid arthritis // Clin Rheumatol 2008; 27: 841–844.
- Sim M. K., Kim D. Y., Yoon J. et al. Assessment of peripheral neuropathy in patients with rheumatoid arthritis who complain of neurologic symptoms // Annals of Rehabilitation Medicine. 2014; 38 (2): 249–255.
- Cojocaru I. M., Cojocaru M., Silosi I. et al. Peripheral Nervous System Manifestations in Systemic Autoimmune Diseases // Mædica. 2014; 9 (3): 289–294.
- Said G., Lacroix C., Planté-Bordeneuve V. et al. Nerve granulomas and vasculitis in sarcoid peripheral neuropathy: a clinicopathological study of 11 patients // Brain 2002; 125: 264–75.
- Шнайдер Н. А., Кантимирова Е. А. Паранеопластическая полинейропатия: дефиниция, этиопатогенез, диагностика // Сибирское медицинское обозрение. 2010; 1: 12–16.
- Grisold W., Drlicek M. Paraneoplastic neuropathy // Curr. Opin. Neurol. 1999; 12 (5): 617–625.
- Шнайдер Н. А., Кантимирова Е. А. Паранеопластическая полинейропатия: дефиниция, этиопатогенез, диагностика // Сибирское медицинское обозрение. 2010; 1: 12–16.
- Forman A. D. Peripheral neuropathy and cancer // Current oncology reports. 2004; 6 (1): 20–25.
- Antoine J. C., Honnorat J., Camdessanche J. P. et al. Paraneoplastic anti-CV2 antibodies react with peripheral nerve and are associated with a mixed axonal and demyelinating peripheral neuropathy // Ann. Neurol. 2001; 49: 214–221.
- Antoine J. C., Mosnier J. F., Honnorat J. et al. Paraneoplastic demyelinating neuropathy, subacute sensory neuropathy, and anti-Hu antibodies: clinicopathological study of an autopsy case // Muscle Nerve. 1998; 21 (7): 850–857.
- Plante-Bordeneuve V., Ferreira A., Lalu T. et al. Diagnostic pitfalls in sporadic transthyretin familial amyloid polyneuropathy (TTR-FAP) // Neurology. 2007; 69: 693–698.
- https://aidsetc.org/guide/pain-syndrome-and-peripheral-neuropathy (дата обращения: 25.09.2016).
- Javed S., Petropoulos I. N., Alam U., Malik R. A. Treatment of painful diabetic neuropathy // Ther Adv Chronic Dis. 2015; 6 (1): 15–28.
И. В. Ситкали
О. В. Колоколов1, доктор медицинских наук
А. В. Фисун
ФГБОУ ВО СГМУ им. В. И. Разумовского МЗ РФ, Саратов
1 Контактная информация: [email protected]
Лечение невропатии большеберцового и малоберцового нервов — врачи, лечащие заболевание
Неврологи Москвы — последние отзывы
Врач провела полный осмотр и молоточком, и с иголочкой. Я думала, что проведу там минут двадцать — тридцать, но пробыла у неё два часа. Анна Эдуардовна сделала некоторые анализы по поставленному ею диагнозу. Очень внимательно выслушала, изучила снимки мои, всё рассказала и показала. Тихая, спокойная девушка. Ничего плохого сказать не могу!
На модерации, 21 августа 2021
Мы с большой благодарности относимся к вашему центру, лечимся всей семьёй, очень довольны качеством, и уровнем обслуживания, врачами. Ирина Викторовна назначила лечение, порекомендовала сдать анализы и мы пойдём на повторный приём. Она внимательная, доброжелательная!
Светлана, 19 августа 2021
Хороший врач, очень пунктуальный, вежливый, компетентный. Доктор сделала очень много всего, чтобы мне помочь. Она ответила на все вопросы, даже на те, которые нельзя было предусмотреть, ей все рассказала, мы поговорили. Также Кристина Сергеевна порекомендовала, что нужно предпринять, какие сделать анализы и обследования. В целом у меня осталось очень хорошее, положительное впечатление. Я думаю, что буду обращаться к этому специалисту еще, обязательно порекомендовала бы ее знакомым.
Диана, 18 августа 2021
Доктор у нас был на дому. Я вызывала пожилой маме. Елена Леонидовна ей понравилась. Внимательный, любезный, знающий специалист. Врач все у нас расспросила и дала нам рекомендации, расписала схему лечения. Специалиста нашла по отзывам. Рекомендую.
Марина, 16 августа 2021
Врач классный, внимательный, понятно и доступно все объясняет. Доктор меня проконсультировал, выписал нужные рекомендации, сделал назначения. Все прошло хорошо, я остался очень доволен, так как получил от приема все, что хотел.
Михаил, 14 августа 2021
На приеме доктор опросил меня по поводу моей проблемы, объяснил какие причины, назначил анализы и предварительно выписал лечение и препараты. Пойду повторно после получения анализов. Доктор все доходчиво объясняет, впечатления приятные остались после приема.
Пëтр, 11 августа 2021
Вызывали Елену Александровну на дом. Отличный доктор! Очень внимательная и квалицированная. Остались довольны врачом! Ознакомилась подробно с предыдущими выписками, всё досконально расспросила, осмотрела и сделала назначение. Понятно объясняла. Видимо и дальше будем обращаться к этому специалисту!
Ольга, 04 августа 2021
Доктор профессионал своего дела. Елена Михайловна рассказала мне то, что нужно.
Марина, 01 апреля 2021
Доктор внимательный. Ирина Васильевна меня выслушала, сделала выводы и ответила на вопросы.
Константин, 29 марта 2021
Наталья Александровна очень приятный и грамотный врач. Она дала мне рекомендации и назначила лечение.
Анастасия, 06 февраля 2021
Показать 10 отзывов из 15231причины, симптомы, диагностика и лечение
Полиневропатии — гетерогенная группа заболеваний, характеризующаяся системным поражением периферических нервов. Полиневропатии подразделяются на первично аксональные и первично демиелинизирующие. Независимо от типа полинейропатии ее клиническая картина характеризуется развитием мышечной слабости и атрофии, снижением сухожильных рефлексов, различными нарушениями чувствительности (парестезиями, гипо- и гиперестезией), возникающими в дистальных отделах конечностей, вегетативными расстройствами. Важным диагностическим моментом при установлении диагноза полиневропатии является определение причины ее возникновения. Лечение полинейропатии носит симптоматический характер, основной задачей является устранение причинного фактора.
Общие сведения
Полиневропатии — гетерогенная группа заболеваний, характеризующаяся системным поражением периферических нервов. Полиневропатии подразделяются на первично аксональные и первично демиелинизирующие. Независимо от типа полинейропатии ее клиническая картина характеризуется развитием мышечной слабости и атрофии, снижением сухожильных рефлексов, различными нарушениями чувствительности (парестезиями, гипо- и гиперестезией), возникающими в дистальных отделах конечностей, вегетативными расстройствами. Важным диагностическим моментом при установлении диагноза полиневропатии является определение причины ее возникновения. Лечение полинейропатии носит симптоматический характер, основной задачей является устранение причинного фактора или компенсация основного заболевания.
Полиневропатии
Этиология и патогенез полиневропатий
Независимо от этиологического фактора при полиневропатиях выявляют два типа патологических процессов — поражение аксона и демиелинизацию нервного волокна. При аксональном типе поражения возникает вторичная демиелинизация, при демиелинизирующем поражении вторично присоединяется аксональный компонент. Первично аксональными являются большинство токсических полиневропатий, аксональный тип СГБ, НМСН II типа. К первично демиелинизирующим полиневропатиям относятся классический вариант СГБ, ХВДП, парапротеинемические полиневропатии, НМСН I типа.
При аксональных полиневропатиях страдает главным образом транспортная функция осевого цилиндра, осуществляемая аксоплазматическим током, который несет в направлении от мотонейрона к мышце и обратно ряд биологических субстанций, необходимых для нормального функционирования нервных и мышечных клеток. В процесс вовлекаются в первую очередь нервы, содержащие наиболее длинные аксоны. Изменение трофической функции аксона и аксонального транспорта приводит к появлению денервационных изменений в мышце. Денервация мышечных волокон стимулирует развитие сначала терминального, а затем и коллатерального спраутинга, роста новых терминалей и реиннервацию мышечных волокон, что ведет к изменению структуры ДЕ.
При демиелинизации происходит нарушение сальтаторного проведения нервного импульса, в результате чего снижается скорость проведения по нерву. Демиелинизирующее поражение нерва клинически проявляется развитием мышечной слабости, ранним выпадением сухожильных рефлексов без развития мышечных атрофий. Наличие атрофий указывает на дополнительный аксональный компонент. Демиелинизация нервов может быть вызвана аутоиммунной агрессией с образованием антител к различным компонентам белка периферического миелина, генетическими нарушениями, воздействием экзотоксинов. Повреждение аксона нерва может быть обусловлено воздействием на нервы экзогенных или эндогенных токсинов, генетическими факторами.
Классификация полиневропатий
На сегодняшний день общепринятой классификации полиневропатий не существует. По патогенетическому признаку полиневропатии разделяют на аксональные (первично поражение осевого цилиндра) и демиелинизирующие (патология миелина). По характеру клинической картины выделяют моторные, сенсорные и вегетативные полиневропатии. Однако в чистом виде эти формы наблюдаются весьма редко, чаще выявляют сочетанное поражение двух или трех видов нервных волокон (моторно-сенсорные, сенсорно-вегетативные др.).
По этиологическому фактору полиневропатии разделяют на наследственные (невральная амиотрофия Шарко-Мари-Тута, синдром Русси-Леви, синдром Дежерина-Сотта, болезнь Рефсума и пр.), аутоиммунные (синдром Миллера-Флешера, аксональный тип СГБ, парапротеинемические полиневропатии, паранеопластические невропатии и др.), метаболические (диабетическая полинейропатия, уремическая полиневропатия, печеночная полинейропатия и др.), алиментарные, токсические и инфекционно-токсические.
Клиническая картина полиневропатии
В клинической картине полиневропатии, как правило, сочетаются признаки поражения моторных, сенсорных и вегетативных волокон. В зависимости от степени вовлеченности волокон различного типа в неврологическом статусе могут преобладать моторные, сенсорные либо вегетативные симптомы. Поражение моторных волокон приводит к развитию вялых парезов, для большинства полиневропатий типично поражение верхних и нижних конечностей с дистальным распределением мышечной слабости, при продолжительных поражениях аксона развиваются мышечные атрофии. Для аксональных и наследственных полиневропатий характерно дистальное распределение мышечной слабости (чаще в нижних конечностях), которая более выражена в мышцах-разгибателях, чем в мышцах-сгибателях. При выраженной слабости перонеальной группы мышц развивается степпаж (т. н. «петушиная походка»).
Приобретенные демиелинизирующие полиневропатии могут проявляться проксимальной мышечной слабостью. При тяжелом течении может отмечаться поражение ЧН и дыхательных мышц, что чаще всего наблюдается при синдроме Гийена-Барре (СГБ). Для полиневропатий характерна относительная симметричность мышечной слабости и атрофии. Асимметричные симптомы характерны для множественных мононевропатий: мультифокальной моторной невропатии, мультифокальной сенсомоторной невропатии Самнера-Льюиса. Сухожильные и периостальные рефлексы при полиневропатии обычно снижаются или выпадают, в первую очередь снижаются рефлексы ахиллова сухожилия, при дальнейшем развитии процесса — коленные и карпорадиальные, сухожильные рефлексы с двуглавых и трехглавых мышц плеча могут оставаться сохранными длительное время.
Сенсорные нарушения при полиневропатии также чаще всего относительно симметричны, сначала возникают в дистальных отделах (по типу «перчаток» и «носков») и распространяются проксимально. В дебюте полиневропатии часто выявляют позитивные сенсорные симптомы (парестезия, дизестезия, гиперестезия), но при дальнейшем развитии процесса симптомы раздражения сменяются симптомами выпадения (гипестезия). Поражение толстых миелинизированных волокон приводит к нарушениям глубокомышечной и вибрационной чувствительности, поражение тонких миелинизированных волокон — к нарушению болевой и температурной чувствительности кожи.
Нарушение вегетативных функций наиболее ярко проявляется при аксональных полиневропатиях, так как вегетативные волокна являются немиелизированными. Чаще наблюдают симптомы выпадения: поражение симпатических волокон, идущих в составе периферических нервов, проявляется сухостью кожных покровов, нарушением регуляции сосудистого тонуса; поражение висцеральных вегетативных волокон приводит к дизавтономии (тахикардия, ортостатическая гипотензия, снижение эректильной функции, нарушение работы ЖКХ).
Диагностика полиневропатий
При выявлении медленно прогрессирующей сенсомоторной полиневропатии, дебютировавшей с перонеальной группы мышц, необходимо уточнить наследственный анамнез, особенно наличие у родственников утомляемости и слабости мышц ног, изменений походки, деформации стоп (высокий подъем). При развитии симметричной слабости разгибателей кисти необходимо исключить интоксикацию свинцом. Как правило, токсические полиневропатии характеризуются, помимо неврологических симптомов, общей слабостью, повышенной утомляемостью и редко абдоминальными жалобами. Кроме того, необходимо выяснить, какие препараты принимал/принимает пациент для того, чтобы исключить лекарственную полиневропатию.
Медленно прогрессирующее развитие асимметричной слабости мышц — клинический признак мультифокальной моторной полиневропатии. Для диабетической полиневропатии характерна медленно прогрессирующая гипестезия нижних конечностей в сочетании с чувством жжения и другими проявлениями в стопах. Уремическая полиневропатия возникает, как правило, на фоне хронического заболевания почек (ХПН). При развитии сенсорно-вегетативной полиневропатии, характеризующейся жжением, дизестезиями, на фоне резкого уменьшения массы тела необходимо исключить амилоидную полиневропатию.
Для наследственных полиневропатий характерны преобладание слабости разгибателей мышц стоп, степпаж, отсутствие ахилловых сухожильных рефлексов, высокий свод стопы. В более поздней стадии заболевания отсутствуют коленные и карпорадиальные сухожильные рефлексы, развиваются атрофии мышц стоп, голеней. Поражение мышц, соответствующее иннервации отдельных нервов, без сенсорных нарушений характерно для множественной моторной полиневропатии. В большинстве случаев преобладает поражение верхних конечностей.
Сенсорные полиневропатии характеризуются дистальным распределением гипестезий. В начальных стадиях заболевания возможна гиперестезия. Сенсомоторные аксональные невропатии характеризуются дистальными гипестезиями и дистальной мышечной слабостью. При вегетативных полиневропатиях возможны как явления выпадения, так и раздражение вегетативных нервных волокон. Для вибрационной полиневропатии типичны гипергидроз, нарушения сосудистого тонуса кистей, для диабетической полиневропатии, напротив, сухость кожных покровов, трофические нарушения, вегетативная дисфункция внутренних органов.
Исследование антител к GM1-гангликозидам рекомендуют проводить у пациентов с моторными невропатиями. Высокие титры (более 1:6400) специфичны для моторной мультифокальной невропатии. Низкие титры (1:400-1:800) возможны при хронической воспалительной демиелинизирующей полирадикулоневропатии (ХВДП), синдроме Гийена-Барре и иных аутоиммунных невропатиях. Следует помнить, что повышенный титр антител к GM1-гангкликозидам выявляют у 5% здоровых людей (особенно пожилого возраста). Антитела к ассоциированному с миелином гликопротеину выявляют у 50% пациентов с диагнозом «парапротеинемическая полиневропатия» и в некоторых случаях других аутоиммунных невропатий.
При подозрении на полиневропатии, связанные с интоксикацией свинцом, алюминием, ртутью проводят анализы крови и мочи на содержание тяжелых металлов. Возможно проведение молекулярно-генетического анализа на все основные формы НМСН I, IVA, IVB типов. Проведение игольчатой электромиографии при полиневропатиях позволяет выявить признаки текущего денервационно-реиннервационного процесса. Прежде всего, необходимо исследовать дистальные мышцы верхних и нижних конечностей, а при необходимости и проксимальные мышцы. Проведение биопсии нервов оправдано только при подозрении на амилоидную полиневропатию (выявление отложений амилоида).
Лечение полиневропатий
При наследственных полиневропатиях лечение носит симптоматический характер. При аутоиммунных полиневропатиях цель лечения заключается в достижении ремиссии. При диабетической, алкогольной, уремической и других хронических прогрессирующих полиневропатиях лечение сводится к уменьшению выраженности симптоматики и замедлению течения процесса. Один из важных аспектов немедикаментозного лечения — лечебная физкультура, направленная на поддержание мышечного тонуса и предупреждение контрактур. В случае развития дыхательных нарушений при дифтерийной полиневропатии может потребоваться проведение ИВЛ. Эффективного медикаментозного лечения наследственных полиневропатий не существует. В качестве поддерживающей терапии используют витаминные препараты и нейротрофические средства. Впрочем, эффективность их до конца не доказана.
Для лечения порфирийной полиневропатии назначают глюкозу, которая обычно вызывает улучшение состояния пациента, а также обезболивающие и другие симптоматические препараты. Медикаментозное лечение хронической воспалительной демиелинизирующей полиневропатии включает в себя проведение мембранного плазмафереза, применение иммуноглобулина человеческого или преднизолона. В ряде случаев эффективность плазмафереза и иммуноглобулина оказывается недостаточной, поэтому, если нет противопоказаний, лечение следует сразу начинать с глюкокортикостероидов. Улучшение наступает, как правило, через 25-30 дней; через два месяца можно начинать постепенное снижение дозы до поддерживающей. При снижении дозы глюкокортикостероидов необходимо проведение ЭМГ-контроля. Как правило, полностью отменить преднизолон удается в течение 10-12 месяцев, при необходимости можно «подстраховаться» азатиоприном (либо циклоспорин, либо микофенолата мофетил).
Лечение диабетической полиневропатии проводится совместно с эндокринологом, основной его целью является поддержание нормального уровня сахара крови. Для купирования болевого синдрома применяют трициклические антидепрессанты, а также прегабалин, габапентин, ламотриджин, карбамазепин. В большинстве случаев применяют препараты тиоктовой кислоты и витамины группы В. Регресс симптомов на ранней стадии уремической полиневропатии достигается нефрологами при коррекции уровня уремических токсинов в крови (программный гемодиализ, трансплантация почки). Из лекарственных средств применяются витамины группы В, при выраженном болевом синдроме — трициклические антидепрессанты, прегабалин.
Основной терапевтический подход в лечении токсической полиневропатии — прекращение контакта с токсическим веществом. При дозозависимых лекарственных полиневропатиях необходимо скорректировать дозу соответствующего лекарственного препарата. При подтвердившемся диагнозе «дифтерия» введение антитоксической сыворотки уменьшает вероятность развития дифтерийной полиневропатии. В редких случаях в связи с развитием контрактур и деформации стоп может понадобиться хирургическое лечение. Однако следует помнить, что длительная обездвиженность после оперативного вмешательства может негативно повлиять на двигательные функции.
Прогноз при полиневропатии
При хронической воспалительной демиелинизирующей полирадикулоневропатии прогноз на жизнь достаточно благоприятный. Летальность очень низкая, однако, полное выздоровление наступает очень редко. До 90% пациентов на фоне иммуносупрессивной терапии достигают полной либо неполной ремиссии. В то же время заболевание склонно к обострениям, применение иммуносупрессивной терапии может быть в виду ее побочных действий, приводящих к многочисленным осложнениям.
При наследственных полиневропатиях редко удается добиться улучшения состояния, так как заболевание медленно прогрессирует. Однако пациенты, как правило, адаптируются к своему состоянию и в большинстве случаев до самых поздних стадий заболевания сохраняют способность к самообслуживанию. При диабетической полиневропатии прогноз на жизнь благоприятный при условии своевременного лечения и тщательного контроля гликемии. Лишь в поздних стадиях заболевания выраженный болевой синдром способен значительно ухудшить качество жизни пациента.
Прогноз на жизнь при уремической полиневропатии полностью зависит от выраженности хронической почечной недостаточности. Своевременное проведение программного гемодиализа либо трансплантация почки способны привести к полному либо почти полному регрессу уремической полиневропатии.
Ходулев Василий Иосифович
Ходулев Василий Иосифович – врач высшей квалификационной категории, доктор медицинских наук, доцент.
Профессор учебного отдела РНПЦ неврологии и нейрохирургии.
Окончил Смоленский государственный медицинский институт в 1986 году по специальности «педиатрия».
В 1989 г. – специализация по нервным болезням в областной детской больнице г. Вологды.
В 1990 г. – специализация по общей иглорефлексотерапии в Ленинградском ордена Трудового Красного Знамени педиатрическом медицинском институте.
В 1995 г. – специализация по электромиографии в НИИ неврологии Российской АМН.
В 2001 г. защитил кандидатскую диссертацию на тему «Электронейромиографическая характеристика алкогольной и хронической воспалительной демиелинизирующей полиневропатий» по специальности 14.00.13 – нервные болезни.
В 2005 г. присвоена первая квалификационная категория.
В 2006 г. – курсы GCP.
В 2014 г. защитил докторскую диссертацию на тему «Функциональное состояние периферических нервов при аксональных и демиелинизирующих невропатиях (клинико-электронейромиографическое исследование)» по специальности 14.01.11 – нервные болезни.
В 2014 г. присвоено ученое звание доцента по специальности «Клиническая медицина».
В 2015 году приказом Министерства здравоохранения присвоена высшая квалификационная категория по квалификации врач
Автор более 150 научных работ, 18 изобретений, 22 рационализаторских предложений, 2 методических рекомендаций, 7 инструкций по применению, утвержденных Министерством здравоохранения Республики Беларусь.
Контакты: e-mail: [email protected]
Сфера научных интересов: электронейромиография, диагностика и механизмы развития аксональных и демиелинизирующих невропатий при заболеваниях периферической нервной системы: компрессионно-ишемические (туннельные) невропатии, полиневропатии различного генеза (алкогольная, диабетическая, наследственная моторно-сенсорная невропатия, хроническая воспалительная демиелинизирующая полирадикулоневропатия), радикулопатии.
Основные публикации
Статьи в журналах и научных сборниках, включенных в перечень ВАК Республики Беларусь:- Ходулев, В.И. Электронейромиографическая характеристика алкогольной полиневропатии / В.И. Ходулев, Н.И. Нечипуренко, С.В. Марченко // Журн. неврологии и психиатрии имени Корсакова. – 1999. – Т. 99, № 12. – С. 47–49.
- Ходулев, В.И. Изменения формы М-ответа при полиневропатиях различного генеза / В.И. Ходулев, Н.И. Нечипуренко, С.В. Марченко // Журн. неврологии и психиатрии им. Корсакова. – 2001. – Т. 101, № 8. – С. 29–31.
- Ходулев, В.И. Индекс средней амплитуды потенциала действия чувствительного нерва / В.И. Ходулев // Сб. науч. тр. / НИИ неврологии, нейрохирургии и физиотерапии. – Минск, 2001. – Вып. 3 : Актуальные проблемы неврологии и нейрохирургии им. Корсакова. – С. 167–172.
- Поражение центральной нервной системы при воспалительных демиелинизирующих полиневропатиях / В.В. Пономарев, И.П. Антонов, А.И. Антоненко, Г.И. Овсянкина, В.И. Ходулев // Журн. неврологии и психиатрии им. Корсакова. – 2002. – Т. 102, № 11. – С. 17–19.
- Ходулев, В.И. Характеристика кортикальной мозжечковой атаксии алкогольного генеза с использованием соматосенсорных вызванных потенциалов / В.И. Ходулев // Сб. науч. тр. / НИИ неврологии, нейрохирургии и физиотерапии. – Минск, 2002. – Вып. 4 : Актуальные проблемы неврологии и нейрохирургии. – С. 192–198.
- Ходулев, В.И. Электронейромиографические критерии частичного моторного блока проведения и временной дисперсии у больных алкогольной полиневропатии / В.И. Ходулев, Н.И. Нечипуренко, Г.И. Овсянкина // Журн. неврологии и психиатрии им. Корсакова. – 2002. – Т. 102, № 1. – С. 49–52.
- Ходулев, В.И. Состояние проводящей функции периферических нервов на ранней стадии аксональной (алкогольной) полиневропатии (электронейромиографическое исследование) / В.И. Ходулев // Сб. науч. тр. / НИИ неврологии, нейрохирургии и физиотерапии. – Минск, 2003. – Вып. 5 : Актуальные проблемы неврологии и нейрохирургии. – С. 162–169.
- Электронейромиографическое исследование функционального состояния лучевого нерва: многофакторный статистический анализ / В.И. Ходулев, А.С. Мастыкин, И.П. Антонов, Г.Д. Аркинд // Новости мед.-биол. наук. – 2004. – № 4. – С. 5–12.
- Пономарев, В.В. Неврологические проявления узелкового полиартериита: клинико-электронейромиографические особенности / В.В. Пономарев, В.И. Ходулев // Актуальные проблемы неврологии и нейрохирургии : сб. науч. тр. – Минск, 2005. – Вып. 7. – С. 119–128.
- Матусевич, Л.И. Интратекальный синтез иммуноглобулинов класса G в центральной нервной системе и состояние гематоэнцефалического барьера у больных с полиневропатиями / Л.И. Матусевич, Н.Ю. Щербина, В.И. Ходулев // Актуальные проблемы неврологии и нейрохирургии : сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2006. – Вып. 8. – С. 91–96.
- Ходулев, В.И. Электронейромиографическое исследование лучевого нерва на уровне плеча: нормативные данные и блок проведения / В.И. Ходулев // Журн. неврологии и психиатрии им. Корсакова. – 2006. – Т. 106, № 7. – С. 35–40.
- Ходулев, В.И. Электронейромиографическое исследование срединного нерва: особенности формирования М-ответа с передней группы мышц предплечья при стимуляции плечевого сплетения / В.И. Ходулев, Н.И. Нечипуренко, И.П. Антонов // Журн. неврологии и психиатрии им. Корсакова. – 2006. – Т. 106, № 9. – С. 47–51.
- Ходулев, В.И. Электронейромиографическая характеристика диабетической дистальной симметричной полиневропатии / В.И. Ходулев // Сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2007. – Вып. 9 : Актуальные проблемы неврологии и нейрохирургии. – С. 194–204.
- Нечипуренко, Н.И. Состояние периферических нервов при свинцовой интоксикации по данным электронейромиографии / Н.И. Нечипуренко, В.И. Ходулев // Весцi НАН Беларусi. Сер. мед. навук. – 2008. – № 2. – С. 14–19.
- Пономарев, В.В. Нейроэндокринные нарушения при воспалительных демиелинизирующих полиневропатиях / В.В. Пономарев, Е.И. Дашкевич, В.И. Ходулев // Журн. неврологии и психиатрии им. Корсакова. – 2008. – Т. 108, № 7. – С. 72–73.
- Ходулев, В.И. Компрессионно-ишемическая невропатия малоберцового нерва: блок проведения и суммарная электромиограмма / В.И. Ходулев // Сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2008. – Вып. 11 : Актуальные проблемы неврологии и нейрохирургии. – С. 261–271.
- Ходулев, В.И. Электронейромиографическая оценка дисфункции проведения по периферическим нервам при алкогольной полиневропатии с использованием нормированного отклонения / В.И. Ходулев // Сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2008. – Вып. 10 : Актуальные проблемы неврологии и нейрохирургии. – С. 255–262.
- Ходулев, В.И. Электронейромиографическая характеристика функционального состояния периферических нервов при хронической воспалительной демиелинизирующей полиневропатии / В.И. Ходулев // Сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2008. – Вып. 11 : Актуальные проблемы неврологии и нейрохирургии. – С. 271–282.
- Электронейромиографическое исследование лучевого нерва при компрессионно-ишемической невропатии / В.И. Ходулев, Н.И. Нечипуренко, И.П. Антонов, Г.Д. Аркинд // Журн. неврологии и психиатрии им. Корсакова. – 2008. – Т. 108, № 7. – С. 48–55.
- Ходулев, В.И. Зависимость проводящей функции малоберцового нерва от его аксональной целостности при диабетической дистальной симметричной полиневропатии / В.И. Ходулев, Н.И. Нечипуренко, Н.Ю. Щербина // Мед. панорама. – 2009. – № 5. – С. 27–30.
- Ходулев, В.И. Клинико-электронейро-миографическая оценка болевой чувствительности у больных с алкогольной полиневропатией / В.И. Ходулев, Н.И. Нечипуренко, Н.Ю. Щербина // Мед. панорама. – 2009. – № 5. – С. 30–33.
- Ходулев, В.И. Клинико-электронейромиографическая оценка болевой чувствительности у больных с хронической воспалительной демиелинизирующей полиневропатией / В.И. Ходулев // Сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2009. – Вып. 12 : Актуальные проблемы неврологии и нейрохирургии. – С. 372–380.
- Ходулев, В.И. Особенности формирования М-ответа с мышц возвышения большого пальца кисти при стимуляции плечевого сплетения / В.И. Ходулев // Сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2009. – Вып. 12 : Актуальные проблемы неврологии и нейрохирургии. – С. 362–371.
- Ходулев, В.И. Состояние проводящей функции малоберцового нерва при алкогольной полиневропатии / В.И. Ходулев, А.В. Сидоренко // Весцi НАН Беларусi. Сер. мед. навук. – 2009. – № 3. – С. 53–58.
- Ходулев, В.И. Электронейромиографическая характеристика функционального состояния периферических нервов при хронической свинцовой интоксикация легкой степени / В.И. Ходулев, Н.И. Нечипуренко, А.А. Агарышев // Весцi НАН Беларусi. Сер. мед. навук. – 2009. – № 1. – С.51–56.
- Клинико-электронейромиографическая характеристика состояния нервов нижних конечностей при сахарном диабете 1 типа / В.И. Ходулев, Г.В. Забродец, О.Б. Князькина, Н.Ю. Щербина // Мед. панорама. – 2010. – № 5. – С. 24–28.
- Клинико-электрофизиологическая и спекл-оптическая характеристика острых компрессионно-ишемических невропатий малоберцового и лучевого нервов / Н.И. Нечипуренко, В.И. Ходулев, Е.А. Короткевич, Л.А. Василевская, Г.В. Забродец // Неврология и нейрохирургия в Беларуси. – 2010. – № 2. – С. 18–30.
- Невропатия, обусловленная моноклональной IgM гаммапатией неопределенного значения / С.А. Лихачев, А.В. Астапенко, В.И. Ходулев, Г.В. Забродец, С.Л. Куликова, Л.И. Матусевич, Н.Ю. Щербина, А.Н. Качинский // Неврология и нейрохирургия в Беларуси. – 2010. – № 1. – С. 42–51.
- Ходулев, В.И. Клинико-электронейромиографическая оценка болевой чувствительности у больных с диабетической дистальной симметричной полиневропатией / В.И. Ходулев // Весцi НАН Беларусi. Сер. мед. навук. – 2010. – № 1. – С. 62–67.
- Ходулев, В.И. Клинико-электронейромиографическая характеристика наследственной моторно-сенсорной невропатии 1 типа / В.И. Ходулев // Актуальные проблемы неврологии и нейрохирургии : сб. науч. тр. / РНПЦ неврологии и нейрохирургии ; под ред. С.А. Лихачева. – Минск, 2010. – Вып. 13. – С. 188–197.
- Ходулев, В.И. Современное представление о структуре и функции миелинизированных нервных волокон / В.И. Ходулев, Л.А. Фурсова, М.И. Тукало // Неврология и нейрохирургия в Беларуси. – 2010. – № 4. – С. 151–159.
- Власова С.В., Ходулев В.И., Пономарев Г.Н. Количественная электромиографическая оценка межмышечного взаимодействия у спортсменов // Теория и практика физической культуры. – 2016. – № 8. – С. 97-99.
- Подгайский В. Н., Рустамов Х. М., Ладутько Д. Ю., Мечковский С. Ю., Подгайский А. В., Пекарь А. В., Ходулев В. И., Черненко Н. И. Аутотрансплантация сегмента нежной мышцы бедра с тригеминальной невротизацией как способ лечения стойкого лицевого паралича после удаления невриномы преддверно-улиткового нерва (клинический случай) // Хирургия. Восточная Европа. 2017. Т. 6. № 4. С. 538–546.
- Ходулев, В.И. Компрессионно-ишемические невропатии: анатомо-морфологические особенности, патофизиологические паттерны, клиника / В.И. Ходулев, Н.И. Нечипуренко // Медицинские новости. – 2018. – Т.280, №1. – C.27–32.
Материалы конференций, тезисы докладов
- Khodulev, V. The positive peak of the compound muscle action potential in diagnosis of alcohol polyneuropathy / V. Khodulev, N. Nechipurenko, S. Marchenko // Eur. J. Neurol. – 1999. – Vol. 6, Suppl. 3. – P. 68.
- Khodulev, V. Nerve conduction study and the new diagnostic criterion / V. Khodulev, N. Nechipurenko, S. Marchenko // Clin. Neurophysiol. – 1999. – V. 110, Suppl. 1. – P. 209-210.
- Marchenko, S. Nerve conduction study in alcohol polyneuropathy / S. Marchenko, V. Khodulev, N. Nechipurenko // Clin. Neurophysiol. – 1999. – V. 110, Suppl. 1. – P. S231.
- Khodulev, V. Сlassification of compound muscle action potentials / V. Khodulev // Clin. Neurophysiol. – 2001. – Vol. 112, suppl. 1. – P. S19.
- Khodulev, V. Criteria of partial motor conduction block: a study based on patients with alcohol polyneuropathy / V. Khodulev, N.I. Nechipurenko, G.I. Ovsyankina // J. Neurol. Sci. – 2001. – Vol. 187, suppl. – P. S501.
- Ходулев, В.И. Критерии частичного моторного блока проведения и временной дисперсии, разработанные на основе анализа М-ответов у здоровых и больных с алкогольной полиневропатией / В.И. Ходулев // Достижения медицинской науки Беларуси : науч.-практ. ежегод. – Минск, 2002. – Вып. 7. – С. 15–16.
- Ходулев, В.И. Технология электронейромиографической диагностики блока проведения импульса по моторным нервам / В.И. Ходулев, В.В. Пономарев, Н.И. Нечипуренко // Медэлектроника–2002. Средства медицинской электроники и новые медицинские технологии : сб. науч. ст. Междунар. науч.-тех. конф., Минск, 20–21 нояб. 2002 г. / Белорус. гос. ун-т информат. и радиоэлектроники ; редкол.: С.К. Дик [и др.]. – Минск, 2002. – С. 158–161.
- Ходулев, В.И. Электронейромиографическая характеристика поражения периферических нервов у больных с хронической воспалительной демиелинизирующей полиневропатией / В.И. Ходулев, Н.И. Нечипуренко, В.В. Пономарев // Достижения медицинской науки Беларуси : науч.-практ. ежегод. – Минск, 2002. – Вып. 7. – С. 16–17.
- Khodulev, V. Hereditary motor and sensory neuropathy I and II type: analysis of the amplitude and the area of compound muscle action potential / V. Khodulev, V. Ponomarev, S. Vlasova // Clin. Neurophysiol. – 2002. – Vol. 113, suppl. 1. – P. S.42–S.43.
- Ходулев, В.И. Морфология М-ответов при патологии периферической нервной системы / В.И. Ходулев // Достижения медицинской науки Беларуси / М-во здравоохранения Респ. Беларусь, Респ. науч. мед. б-ка. – Минск, 2003. – Вып. 8. – C. 21–22.
- Khodulev, V. Conducting function status of peripheral nerves in alcoholic polyneuropathy / V. Khodulev, S. Vlasova, V. Veres // Eur. J. Neurol. – 2003. – Vol. 10, suppl. 1. – P. 113.
- Vlasova, S. Relation between movement disorders and electrophysiological features in stroke patients with hemiparesis / S. Vlasova, V. Khodulev, A. Veres // Eur. J. Neurol. – 2003. – Vol. 10, Suppl. 1. – P. 115–116.
- Veres, A. Risk factors in occurrence of low back pain / A. Veres, S. Vlasova, V. Khodulev // Eur. J. Neurol. – 2003. – Vol. 10, Suppl. 1. – P. 172.
- Ishukova, O.A. Parsonage-Turner syndrome: Data of a complex examination of 30 patients and a search for a rational differential therapy / O.A. Ishukova, V.V. Ponomarev, V.I. Khodulev // Eur. J. Neurol. – 2004. – Vol. 11, suppl. 2. – P. 138.
- Ходулев, В.И. Блок проведения, аксональная дегенерация и вторичная демиелинизация при компрессионно-ишемической невропатии лучевого нерва / В.И. Ходулев // Медэлектроника–2004. Средства медицинской электроники и новые медицинские технологии : сб. науч. ст. 3 Междунар. науч.-тех. конф., Минск, 9–10 дек. 2004 г. / Белорус. гос. ун-т информат. и радиоэлектроники ; редкол.: В.С. Улащик [и др.]. – Минск, 2004. – С. 200–203.
- Ходулев, В.И. Вклад передней группы мышц предплечья в формирование М-ответа с разгибателя пальцев при стимуляции точки Эрба / В.И. Ходулев, В.В. Пономарев // Достижения медицинской науки Беларуси / М-во здравоохранения Респ. Беларусь, Респ. науч. мед. б-ка. – Минск, 2004. – Вып. 9. – C. 29–30.
- Ходулев, В.И. Электронейромиографическая методика исследования лучевого нерва / В.И. Ходулев, В.В. Пономарев, Г.И. Овсянкина // Достижения медицинской науки Беларуси / М-во здравоохранения Респ. Беларусь, Респ. науч. мед. б-ка. – Минск, 2004. – Вып. 9. – C. 30–31.
- Аркинд, Г.Д. Структура заболеваний периферических нервов конечностей по материалам работы городского отделения медицинской реабилитации неврологических больных 21-й поликлиники г. Минска / Г.Д. Аркинд, В.И. Ходулев, Е.Н. Пономарева // Современные подходы и внедрение новых методик в диагностике : сб. материалов, посвящ. 10-летнему юбилею Витеб. диаг. центра, Витебск, 18–19 марта 2005 г. / Витеб. обл. диаг. центр ; сост. В.И. Орехова, Г.И. Наумова, А.П. Пилант. – Витебск, 2005. – С. 8–12.
- Содержание иммуноглобулина G, его интратекальный синтез в нервной системе и состояние гематоэнцефалического барьера у больных с полиневропатией / Н.И. Нечипуренко, Л.И. Матусевич, Н.Ю. Щербина, В.И. Ходулев // Нейроиммунология : сб. материалов 14 Всерос. конф., Санкт-Петербург, 19-22 мая 2005 г. – СПб., 2005. – С. 122.
- Ходулев, В.И. Формирование М-ответов с мышц предплечья в норме при стимуляции плечевого сплетения / В.И. Ходулев // Современные подходы и внедрение новых методик в диагностике : сб. материалов, посвящ. 10-летнему юбилею Витеб. диаг. центра, Витебск, 18–19 марта 2005 г. / Витеб. обл. диаг. центр ; сост. В.И. Орехова, Г.И. Наумова, А.П. Пилант. – Витебск, 2005. – С. 215–217.
- Ходулев, В.И. Особенности формирования М-ответа с передней поверхности предплечья при стимуляции точки Эрба / В.И. Ходулев // Достижения медицинской науки Беларуси / М-во здравоохранения Респ. Беларусь, Респ. науч. мед. б-ка. – Минск, 2006. – Вып. 11. – C. 143–144.
- Ходулев, В.И. Оценка проводящей функции периферических нервов на ранней стадии аксональной полиневропатии / В.И. Ходулев // XI съезд Белорусского общества физиологов : тез. докл., Минск, 21-22 сент. 2006 г. – Минск, 2006. – С. 158–159.
- Ходулев, В.И. Характер поражения периферических нервов при диабетической полиневропатии / В.И. Ходулев // Достижения медицинской науки Беларуси / М-во здравоохранения Респ. Беларусь, Респ. науч. мед. б-ка. – Минск, 2006. – Вып. 11. – C. 144–145.
- Khodulev, V.I. Estimation of motor conduction velocity with radial nerve neuropathy in spiral groove using nerve conduction studies / V.I. Khodulev, J.I. Musienko, S.V. Vlasava // Clin. Neurophysiol. – 2006. – Vol. 117, suppl. 1. – P. 198.
- Musienko, J.I. The formation features of compound muscle action potential from anterior forearm muscles at brachial plexus stimulation / J.I. Musienko, V.I. Khodulev, S.V. Vlasava // Clin. Neurophysiol. – 2006. – Vol. 117, suppl. 1. – P. 196.
- Технология электронейромиографической диагностики повреждений лучевого нерва / В.И. Ходулев, Н.И. Нечипуренко, Г.В. Зобнина, М.А. Щуревич // Медэлектроника–2008. Средства медицинской электроники и новые медицинские технологии : сб. науч. ст. 5 Междунар. науч.-тех. конф., Минск, 11–12 дек. 2008 г. / Белорус. гос. ун-т информат. и радиоэлектроники ; редкол.: В.С. Улащик [и др.]. – Минск, 2008. – С. 333–338.
- Возможности использования количественного сенсорного тестирования в диагностике поражений периферических нервов / Г.И. Овсянкина, Г.Д Ситник, В.И. Ходулев, Г.В. Зобнина // Научное обоснование физического воспитания, спортивной тренировки и подготовки кадров по физической культуре и спорту : материалы Междунар. науч.-практ. конф., Минск, 8–10 апр. 2009 г. – Минск, 2009. – С. 122–124.
- Нечипуренко, Н.И. Характер изменений аксональной и проводящей функций периферических нервов при алкогольной и диабетической невропатиях по данным электронейромиографии / Н.И. Нечипуренко, В.И. Ходулев // Актуальные теоретические и прикладные аспекты патофизиологии : материалы респ. конф. с междунар. участием, Гродно, 14 мая 2010 г. / отв. ред. Н.Е. Максимович. – Гродно, 2010. – С. 162–165.
- Ходулев, В.И. Электронейромиографический паттерн повреждения периферических нервов при алкогольной полиневропатии / В.И. Ходулев, Н.И. Нечипуренко, М.А. Щуревич // Медэлектроника–2010. Средства медицинской электроники и новые медицинские технологии : сб. науч. ст. 6 Междунар. науч.-тех. конф., Минск, 8–9 дек. 2010 г. / Белорус. гос. ун-т информат. и радиоэлектроники ; редкол.: В.С. Улащик [и др.]. – Минск, 2010. – С. 226–229.
- Гипералгезия и гипалгезия – стадии аксональной дегенерации тонких волокон периферических нервов при алкогольной полиневропатии / В.И. Ходулев, Н.И. Нечипуренко, А.Л. Танин, А.И. Верес // Рос. журн. боли. – 2011. – № 2. – С. 56–57.
- Ходулев, В.И. Взаимоотношения миелиновой оболочки и аксона на разных стадиях аксональной дегенерации у пациентов с диабетической невропатией / В.И. Ходулев // Сигнальные механизмы регуляции физиологических функций : тез. докл. 13 съезда Белорус. о-ва физиологов и 2 Междунар. науч. конф., Минск, 19–20 апр. 2012 г., Минск / редкол.: В.В. Лысак [и др.]. – Минск, 2012. – С. 150.
- Ходулев, В.И. Клинико-нейрофизиологическая диагностика повреждений лучевого нерва / В.И. Ходулев // Актуальные вопросы диагностики и лечения нервно-мышечных болезней : материалы Первой Учредительной конф. РОО «Общество специалистов по нервно-мышечным болезням», Москва, 22–23 нояб. 2012 г. – М., 2012. – С. 44–45.
- Ходулев, В.И. Нейрофизиологические механизмы аксональной дегенерации при диабетической дистальной симметричной полиневропатии / В.И. Ходулев, Н.И. Нечипуренко // Клиническая нейрофизиология : материалы науч.–практ. конф. с междунар. участием. – СПб, 2013. – С. 18–19.
- Ходулев, В.И. Электронейромиографическая диагностика лучевого нерва на уровне спирального канала и супинатора с использованием поверхностных электродов / В.И. Ходулев // Клиническая нейрофизиология : материалы науч.–практ. конф. с междунар. участием. – СПб, 2013. – С. 20–21.
- Ходулев, В.И. Электронейромиографические паттерны и механизмы аксональной дегенерации периферических нервов при диабетической полиневропатии / В.И. Ходулев // Дифференциальный диагноз в клинике нервно-мышечных болезней : сб. тезисов Российской науч.–практ. конф. с междунар. участием. – М., 2014. – С. 77–78.
- Ходулев, В.И. Технология электронейромиографической диагностики компрессионных повреждений лучевого нерва на разных уровнях / В.И. Ходулев // Дифференциальный диагноз в клинике нервно-мышечных болезней : сб. тезисов Российской науч.–практ. конф. с междунар. участием. – М., 2014. – С. 78–80.
- Ходулев, В.И., Нечипуренко Н.И. Возбудимость периферических нервов при хронической воспалительной демиелинизирующей полирадикулоневропатии / В.И. Ходулев, Н.И. Нечипуренко // Вестник клин. нейрофизиологии // Клиническая нейрофизиология и нейрореабилитация / Материалы Второй науч.-практ. конф. с междунар. участием. – СПб., 2014. – С. 57-59.
- Ходулев В.И. Нейрофизиологические особенности невропатии, обусловленной моноклональной IgM гаммапатией неопределенного значения // Вестник клин. нейрофизиологии // Клиническая нейрофизиология и нейрореабилитация / Материалы Четвертой науч.-практ. конф. с международным участием. – СПб, 24-26 ноября 2016. – С. 50-51.
Инструкции по применению, утвержденные Министерством здравоохранения Республики Беларусь
- Дифференциально-диагностические критерии аксональных и демиелинизирующих полиневропатий : инструкция по применению № 127-1005 : утв. М-вом здравоохранения Респ. Беларусь 28.04.2006 / ГУ РНПЦ неврологии и нейрохирургии М-ва здравоохранения Респ. Беларусь ; сост. В.И. Ходулев, В.В. Пономарев, Н.И. Нечипуренко, Л.И. Матусевич, Л.А. Василевская, Г.И. Овсянкина, Н.Ю. Щербина // Современные методы диагностики, лечения и профилактики заболеваний : сб. инструкт.-метод. док. – Минск, 2006. – Вып. 7, т. 2. – С. 116–128.
- Электронейромиографическая диагностика компрессионно-ишемической невропатии лучевого нерва на уровне спирального канала и заднего межкостного нерва на уровне супинатора : инструкция по применению № 109-1108 : утв. М-вом здравоохранения Респ. Беларусь 13.02.2009 / ГУ РНПЦ неврологии и нейрохирургии М-ва здравоохранения Респ. Беларусь ; сост. В.И. Ходулев, Н.И. Нечипуренко // Современные методы диагностики, лечения и профилактики заболеваний : сб. инструкт.-метод. док. – Минск, 2009. – Вып. 10, т. 2. – С. 81–86.
- Диагностика и лечебно-реабилитационные мероприятия при компрессионно-ишемических невропатиях с использованием методов лазерной гемотерапии : инструкция по применению № 101-1104 : утв. М-вом здравоохр. Респ. Беларусь 18.12.2009 / ГУ РНПЦ неврологии и нейрохирургии М-ва здравоохр. Респ. Беларусь ; сост. В.И. Ходулев, Н.И. Нечипуренко, Г.В. Забродец, Г.В. Зобнина, Л.А. Василевская, Е.А. Короткевич, Е.Н. Апанель // Современные методы диагностики, лечения и профилактики заболеваний : сб. инструкт.-метод. док. – Минск, 2010. – Вып. 11, т. 2. – С. 135–150.
Периферическая нейропатия — Клинические и электрофизиологические аспекты
Клиника нейровизуализации N Am. Авторская рукопись; доступно в PMC 2015 15 февраля.
Опубликован в окончательной отредактированной форме:
PMCID: PMC4329247
NIHMSID: NIHMS461426
Tae Chung
1 Департамент неврологии, Школа медицины Университета Джонса Хопкинса
Калпана Прасад
1 Отделение неврологии, Медицинская школа Университета Джона Хопкинса, Балтимор, Мэриленд
Thomas E.Ллойд
1 Кафедра неврологии Медицинской школы Университета Джона Хопкинса, Балтимор, Мэриленд
2 Кафедра неврологии, Медицинская школа Университета Джона Хопкинса, Балтимор, Мэриленд
1 Кафедра неврологии, Школа Университета Джонса Хопкинса of Medicine Балтимор, Мэриленд
2 Отделение неврологии, Школа медицины Университета Джона Хопкинса, Балтимор, Мэриленд
См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Эта статья представляет собой учебник по патофизиологии и клинической оценке периферической невропатии для радиолога. Магнитно-резонансная нейрография (МРН) полезна для диагностики многих очаговых поражений периферических нервов. В сочетании с анамнезом, обследованием, электрофизиологией и лабораторными данными будущие достижения в области МРН с высоким полем могут играть все более важную роль в оценке пациентов с периферической невропатией.
Ключевые слова: нейровизуализация, периферическая нейропатия, электромиография, исследование нервной проводимости, невропатия защемления, наследственная невропатия
Введение
Хотя нейровизуализация обычно используется для диагностики очаговых поражений нервов, таких как травмы и опухоли, в течение многих лет, полезность МР-нейрография высокого разрешения в оценке мультифокальных и системных полинейропатий только изучается [1].Для невролога анатомическое распределение, временная прогрессия и электрофизиологические свойства невропатий определяют дифференциальный диагноз, обследование и лечение большинства форм периферической невропатии; и в настоящее время МР-нейрография не является частью стандартного обследования пациентов с периферической невропатией. Например, при болезни Шарко-Мари-Тута и амилоидной невропатии могут наблюдаться диффузные увеличения нервов, которые невозможно легко отличить друг от друга при МР-нейрографии [2], тогда как исследование нервной проводимости (NCS) покажет резкое снижение скорости проводимости при Тип 1А Шарко-Мари-Тута, но нормальная скорость при амилоидной невропатии.По мере совершенствования технологии нейровизуализации новые методы МРТ, такие как молекулярная визуализация, могут сделать МР-нейрографию более полезной при оценке пациентов с нейропатией.
В первой части этой статьи мы рассмотрим подход неврологов к поражению периферических нервов, основываясь на анатомических, патофизиологических и электрофизиологических свойствах периферических нервов. Позже в этой главе будут обобщены характеристики различных поражений периферических нервов.
Основная структура периферической нервной системы
Периферическая нервная система относится к той части нервной системы, которая находится за пределами головного и спинного мозга.Функционально периферические нервы подразделяются на двигательные, сенсорные и вегетативные. Тела (сома) мотонейронов находятся в вентральном сером веществе спинного мозга и называются клетками переднего рога. Моторные волокна часто имеют очень длинные аксоны, которые доходят до нервно-мышечного соединения. Моторная единица состоит из клетки переднего рога, его моторного аксона и всех мышечных волокон, которые он иннервирует, образуя синапс в нервно-мышечном соединении. Сенсорные нейроны биполярны: афферентный аксон получает сенсорную информацию с периферии, а эфферентный аксон входит в центральную нервную систему через спинной корешок.Тело сенсорного нейрона находится в ганглии дорзального корешка или в одном из сенсорных ганглиев сенсорных черепных нервов. Вегетативная нервная система подразделяется на симпатические и парасимпатические нервы. Нейроны симпатических нервов расположены в боковом роге спинного мозга от T1 до L2, тогда как нейроны парасимпатических нервов расположены в стволе головного мозга и крестцовом спинном мозге (S2, S3 и S4).
Периферические нервы имеют несколько слоев соединительной ткани, окружающей аксоны; эпиневрий содержит кровеносные сосуды и другие соединительные ткани, которые окружают несколько пучков нервов ().Каждый пучок покрыт периневриальной соединительной тканью. Внутри каждого пучка; отдельные миелинизированные и / или немиелинизированные аксоны окружены эндоневриальной соединительной тканью. Кровеносные сосуды (vasa vasorum) и нервы (nervi nervorum) также находятся внутри нерва.
Пластиковые срезы икроножных нервов, окрашенные толуидиновым синим в 10 раз (A-C) и 100X (A’-C ’). (A) Нормальный нерв с нормальной плотностью миелинизированных нервных волокон. «Эндо» — эндоневрий, «пери» (стрелка) — периневрий, окружающий пучки, «эпи» — эпиневрий.При большом увеличении (A ’) большие толстые миелинизированные волокна (*) можно отличить от более мелких, тонких миелинизированных волокон (стрелка). (B) икроножный нерв пациента с аксональной невропатией, демонстрирующий пучок со значительно сниженной плотностью нервных волокон. (B ’) показано волокно с« миелиновым овоидом », которое можно увидеть при валлеровской дегенерации. (C) икроножный нерв пациента с болезнью Шарко-Мари-Тута типа 1А. Нерв диффузно увеличен (C) и при большом увеличении (C ’) показывает нервные волокна, подвергающиеся циклам демиелинизации и ремиелинизации, что приводит к типичному внешнему виду« луковицы »(*).
Патофизиология повреждения периферического нерва
Независимо от причины и характера повреждения, реакция периферического нерва на повреждение ограничивается определенными типами физиологических изменений в зависимости от степени повреждения (). Незначительное локальное повреждение периферического нерва приведет к преходящей очаговой блокаде проводимости, тогда как промежуточное повреждение может вызвать очаговую демиелинизацию, которая требует более длительного периода времени для восстановления. Если степень повреждения нерва достаточно серьезна, чтобы нарушить его аксональное содержимое, следует серия физиологических изменений, известных как валлеровская дегенерация, чтобы гарантировать удаление и реформирование поврежденной части нерва.Дистальная дегенерирующая часть аксона претерпевает стереотипные морфологические изменения и впоследствии переваривается шванновскими клетками, открывая путь для регенерации аксонов из проксимальной части.
Таблица 1
Реакция периферического нерва на травму
| Инсульт | Физиологический статус | Этиология | Электрофизиология |
|---|---|---|---|
| Минимальная | Блок проводимости, быстро обратимая | Очаговая компрессия | Блок фокальной проводимости |
| | |||
| Промежуточный | Блок проводимости, пролонгированный | Фокальная демиелинизация | Блокировка очаговой проводимости и замедление |
| | |||
| Тяжелая | Валлеровская дегенерация | и потеря аксона миелиновая оболочка | Отсутствует ответ |
Сразу после перерезки нерва наблюдаются микроструктурные изменения в дистальной части аксона без каких-либо явных световых микроскопических аномалий до 48 часов.В этот период исследование нервной проводимости в дистальной части покажет только небольшое снижение амплитуды и почти нормальную скорость проводимости [3, 4]. Примерно через 48-72 часа аксоны начинают фрагментироваться и образовывать спиральные или крючковидные сегменты; на поперечном срезе биопсии нерва эта фрагментация будет выглядеть как «миелиновые овоиды» (). На 7-е сутки органоиды аксонов полностью отсутствуют. К этому времени в исследованиях нервной проводимости наблюдается значительное снижение или отсутствие двигательных / сенсорных реакций.Учитывая длину всего аксона, как эти реакции происходят согласованным образом в течение относительно короткого периода времени, остается неизвестным. В случае токсической или метаболической нейропатии, когда поражено все нервное волокно — от тела клетки до нервно-мышечного соединения, возникает ретроградная дегенерация, возможно, из-за недостаточного поступления энергии или других ресурсов из сомы. Это явление также называется невропатией «замирания» и обычно сначала поражает самые длинные нервы, вызывая симптомы сначала в стопах.
Повреждение периферического нерва часто классифицируется на три основные категории в зависимости от его этиологии, гистологических особенностей и клинических проявлений: нейропраксия, аксонотмезис и нейротмезис [5] (). Прогноз после травмы плохой, если имеется нарушение целостности эндоневральной трубки.
Таблица 2
Классификация травмы нерва
| Классификация | Физиология | Гистология | Прогноз |
|---|---|---|---|
| Нейропраксия | Блок очаговой проводимости | Местная миелиновая травма; нет повреждения аксона | Восстановление от нескольких недель до месяцев |
| | |||
| Аксонотмезис | Нарушение нервной проводимости в месте повреждения и дистально | Нарушение целостности аксона, но эндоневральная трубка, периневрий и эпиневрий не повреждены | Хорошо |
| | |||
| Нарушение целостности аксона и эндоневральной трубки, но периневрий и эпиневрий не повреждены | Плохо | ||
| | |||
| Нейротмезис | Нарушение проводимости нерва участок и дистально | Разрыв всего нерва | Регенерация возможна только при повторном соединении дистальной культи |
После пересечения нерва процесс регенерации начинается на дистальном конце проксимальной культи.Через 3-8 дней после травмы у терминального аксона появляются небольшие булавовидные ответвления. Это дистальное расширение называется «конусом роста». К 48 часам лишь некоторые из этих коллатералей достигают зоны повреждения. В оптимальных ситуациях для того, чтобы растущие аксоны достигли дистальной части, может потребоваться 8-15 дней. Однако чем ближе к телу клетки находится место повреждения, тем выше скорость роста. Способность нервов к регенерации зависит от технического обслуживания эндоневральной трубки, что на практике зависит от тяжести повреждения нерва и длины, необходимой аксону для регенерации.Примерно через 9-20 дней ремиелинизируется регенерирующий аксон; однако следует отметить, что миелинизация регенерирующего аксона часто бывает неполной и имеет более короткие межузловые расстояния по сравнению с аксоном до повреждения, задерживая распространение потенциалов действия.
Электрофизиология при периферической невропатии
-
Исследование нервной проводимости: Периферическую невропатию можно разделить на те, которые в первую очередь затрагивают аксоны, и те, которые в первую очередь влияют на миелиновую оболочку.Потеря аксонов может наблюдаться после травмы нерва или в результате токсических, ишемических, метаболических или генетических состояний. Демиелинизация может наблюдаться при компрессионных невропатиях, наследственных невропатиях и приобретенных иммуноопосредованных невропатиях, таких как синдром Гийена-Барре (GBS) и хроническая воспалительная демиелинизирующая полинейропатия (CIDP). Исследования нервной проводимости предоставляют информацию, позволяющую дифференцировать первичное поражение с потерей аксона от первичного демиелинизирующего поражения.
-
Потеря аксонов: Амплитуда сложного мышечного потенциала действия (CMAP) коррелирует с количеством аксонов двигательного нерва, и аналогичным образом амплитуда потенциала действия сенсорного нерва (SNAP) отражает количество аксонов сенсорного нерва.Поражения, вызывающие потерю аксонов, обычно приводят к снижению амплитуд CMAP и SNAP. Однако важно помнить, что вторичная потеря аксонов часто возникает при тяжелых или хронических демиелинизирующих поражениях. Кроме того, при аксональной невропатии может произойти умеренное замедление скорости проводимости и удлинение дистального латентного периода (мера дистальной скорости проводимости), если самые быстрые и самые большие аксоны потеряны.
-
Демиелинизация: потеря миелина связана с замедлением скорости проводимости (ниже 75% от нижнего предела нормы), заметным удлинением дистального латентного периода (более 130% от верхнего предела нормы) или с обоими.Изменения амплитуды также могут происходить при демиелинизации из-за вторичной потери аксонов. Снижение моторной амплитуды может также происходить при демиелинизации, если имеется блокад проводимости. При блокаде проводимости амплитуда будет низкой, когда нерв стимулируется проксимальнее места демиелинизации, но будет нормальной при стимуляции ниже блока (). Любое падение амплитуды или площади CMAP более чем на 20% означает блокировку проводимости, а любое увеличение продолжительности CMAP более чем на 15% означает временную дисперсию; оба являются признаками демиелинизации.У пациентов с демиелинизирующими полинейропатиями блокада проводимости в местах, не связанных с захватом, помогает дифференцировать приобретенные (GBS и CIDP) от наследственных невропатий (CMT).
Исследование проводимости по медиане и локтевому нерву, показывающее частичную блокаду моторной проводимости в сегменте предплечья у пациента с приобретенной демиелинизирующей полинейропатией. Обратите внимание, что при стимуляции выше локтя амплитуда (вертикальные синие линии) моторной реакции уменьшается (из-за блокады проводимости) по сравнению с реакцией на запястье.Кроме того, продолжительность ответа (горизонтальные красные линии) увеличивается при стимуляции выше локтя из-за временной дисперсии, общей черты демиелинизации.
Еще одним полезным измерением, полученным в исследованиях нервной проводимости, является ответ «F-волна», который возникает в результате антидромного перемещения потенциала действия вверх по нерву к клетке переднего рога, которая затем оказывает обратное воздействие на небольшую часть клеток переднего рога. , что приводит к ортодромному перемещению обратно по нерву, мимо места стимуляции, к мышце.Ответ F измеряет проводимость по всей длине нерва и обычно заметно увеличивается при демиелинизирующих поражениях.
У пациентов с нейропатией защемления точное место защемления может быть получено путем обнаружения признаков очаговой демиелинизации, либо путем замедления, либо блокирования проводимости через место поражения. Восстановление после защемления может произойти быстро в течение нескольких недель, если компрессия обратима и вызывает только очаговую демиелинизацию. Напротив, захват, вызывающий значительную потерю аксонов, о чем свидетельствует заметное снижение моторных и сенсорных амплитуд, будет иметь более длительное и менее полное восстановление.
-
Электромиография: (ЭМГ) — это регистрация электрической активности мышц в состоянии покоя (спонтанная) и при нагрузке (произвольные двигательные единицы) с помощью вставного электрода. Наличие аномальной спонтанной активности (положительные резкие волны и потенциалы фибрилляции) свидетельствует об активной денервации. Анализ потенциалов двигательных единиц (MUAP) на игольчатой ЭМГ помогает определить остроту и тяжесть повреждения нерва. Длительная продолжительность, большая амплитуда и многофазные потенциалы двигательных единиц наблюдаются при хронической аксональной невропатии из-за неповрежденных моторных аксонов, иннервирующих денервированные мышечные волокна.Во время сокращения мышц есть два способа увеличить мышечную силу: либо двигательные единицы могут увеличить скорость их работы, либо дополнительные двигательные единицы могут начать работу. Набор относится к способности добавлять двигательные единицы по мере увеличения скорости стрельбы. При невропатических заболеваниях рекрутмент снижается и может быть самым ранним физиологическим признаком повреждения нерва. Таким образом, через несколько недель после очагового травматического повреждения нерва ЭМГ покажет аномальную спонтанную активность и пониженное задействование нормально выглядящих моторных единиц, тогда как через несколько месяцев спонтанная активность будет нормальной, рекрутмент останется сниженным, и теперь моторные единицы будет иметь увеличенную продолжительность и увеличенную амплитуду.Таким образом, ЭМГ может не только помочь локализовать поражение нервов, но также определить хронологию невропатического процесса.
Клиническая оценка повреждения периферических нервов
При оценке пациентов с невропатией или повреждением нервов очень важно оценить физиологический статус периферических нервов с помощью исследований нервной проводимости, чтобы сопоставить их физиологию с клиническими симптомами. После оценки физиологического статуса повреждения нерва необходимо тщательно определить его временную прогрессию, тяжесть и анатомическое распределение, чтобы поставить точный диагноз.
-
Анатомическое распространение: Локализация нервных поражений является наиболее важным аспектом неврологического обследования. Тщательный сбор анамнеза и обследование в сочетании с глубоким пониманием анатомии периферической нервной системы должны позволить локализовать поражение. Кроме того, исследование ЭМГ / нервной проводимости может дополнительно локализовать поражение и помочь в понимании патофизиологии. обобщает общие типы невропатий, которые следует рассматривать в соответствии с характерными для них паттернами неврологических симптомов.
Таблица 3
Характер неврологических симптомов
Тип Невропатии, которые следует учитывать Симметричная дистальная слабость, зависящая от длины, с потерей чувствительности (наиболее распространенный тип) Метаболические невропатии (например, диабет), токсические невропатии, болезнь Шарко-Мари-Тута
Симметричная проксимальная и дистальная слабость с потерей чувствительности и арефлексией Воспалительные демиелинизирующие полинейропатии (CIDP и GBS)
Множественные мононевропатии Васкулитная невропатия, наследственная невропатия со склонностью к параличам от давления (HNPP)
Асимметричная слабость при неизменном сенсорном исследовании и SNAP Болезнь двигательных нейронов, мультифокальная двигательная нейропатия
Асимметричная слабость с болью в области распространения дерматома Радикулопатия
Сенсорная атаксия со слабостью или без нее Сенсорные нейронопатии от паранеопластического синдрома, синдрома Шегрена.
Значительное поражение вегетативной нервной системы Амилоидоз, диабетическая невропатия -
Тип нервного волокна: моторное, сенсорное и / или вегетативное; Крупные и / или мелкие волокна
Тщательное внимание к симптоматике пациента и клиническое обследование часто позволяет выявить типы волокон, которые участвуют в заболевании. Как правило, вовлечение моторных волокон может вызвать слабость, фасцикуляции или мышечную атрофию, тогда как сенсорное вовлечение вызывает онемение, покалывание и / или изменение восприятия боли.Кроме того, повреждение крупных волокон вызывает дисбаланс и снижение вибрационных и проприоцептивных ощущений, в то время как дисфункция мелких волокон вызывает снижение ощущения укола булавкой и температуры. Вовлечение вегетативной нервной системы может привести к нарушению потоотделения, ортостазу, запорам, задержке мочи или сердцебиению. Исследования нервной проводимости позволяют оценить только крупные двигательные и сенсорные нервные волокна; тогда как при избирательном повреждении мелких волокон необходимы другие тесты, такие как биопсия кожи, для оценки этих небольших немиелинизированных нервных волокон.
• Патофизиология: демиелинизирующая или аксональная
Исследование нервной проводимости необходимо для определения того, является ли повреждение нерва первичным демиелинизирующим, аксональным или и тем, и другим, и важно при оценке повреждения периферического нерва. Для демиелинизирующей нейропатии характерно снижение скорости проведения и увеличение латентности дистальных и F-волн, тогда как аксональная нейропатия демонстрирует снижение амплитуды. В некоторых ситуациях биопсия нерва может рассматриваться для оценки причины невропатии и наиболее полезна для диагностики васкулитной или амилоидной невропатии и инфильтративной невропатии, вызванной опухолью.Когда возможно, икроножные или поверхностные лучевые сенсорные нервы обычно резецируются для патологического анализа, чтобы оставить минимальный неврологический дефицит. Когда для биопсии рассматриваются другие нервы, МР-нейрография часто помогает определить оптимальное место для биопсии. Хотя в диагностике демиелинизирующих невропатий (например, CIDP или CMT) может помочь биопсия, биопсия нерва редко требуется для диагностики.
• Степень тяжести
Помимо обследования, ЭМГ / NCS чрезвычайно полезны для определения степени тяжести повреждения нерва.Амплитуда моторных и сенсорных ответов является хорошим показателем степени потери аксонов и коррелирует с инвалидностью. ЭМГ может оценить, денервированы ли мышцы, и, если да, то также может определить остроту и тяжесть денервации. Существуют различные количественные методы измерения тяжести повреждения нервов, часто с использованием простых инструментов, таких как камертон Райдела-Зайффера, моноволокна Фон Фрея и ручной динамометр. Также были предложены различные формулы измерения, использующие комбинацию вышеуказанных количественных результатов тестирования.Среди них общая шкала невропатии (TNS) широко используется для многих системных невропатий; его взаимная и внутренняя надежность хорошо известны [6, 7] и особенно полезны при оценке терапевтических ответов.
• Клинический курс
Тщательная оценка временного прогрессирования симптомов пациента в сочетании с осмотром и физиологией может предоставить важную информацию о процессе болезни. Например, токсическая нейропатия или нейропатия, связанная с питанием, может проявляться монофазным течением при адекватном лечении, тогда как хроническая воспалительная нейропатия может проявляться рецидивирующим и ремиттирующим течением.
Захватывающие мононевропатии
Синдром запястного канала — наиболее распространенная мононевропатия, вызываемая ущемлением срединного нерва, когда он проходит в запястном канале запястья. Другие распространенные невропатии защемления включают локтевую нейропатию в локтевом суставе (синдром кубитального канала), лучевую невропатию в области спиральной борозды и малоберцовую невропатию в области головки малоберцовой кости. Состояния, предрасполагающие к синдрому канала запястья и кубитального канала, включают занятия, которые подвергаются повторяющемуся сгибанию / сокращению запястий и локтей, диабет, ожирение, гипотиреоз, артрит и лежащие в основе периферические невропатии, ведущие к гипертрофии нервов.При обследовании выявляются сенсорные нарушения в распределении периферического нерва с моторным дефицитом или без него, а также может быть выявлен «положительный признак Тинеля», при котором перкуссия по месту повреждения нерва воспроизводит сенсорные симптомы пациента. Диагноз обычно ставится с помощью ЭМГ / NCS, но методы визуализации, такие как ультразвук и МР-нейрография, все чаще используются, чтобы помочь хирургам определить этиологию, тяжесть, прогноз и лечение застойных мононевропатий.
Невропатии, связанные с метаболическим заболеванием обычно проявляются медленно прогрессирующей дистальной (зависящей от длины) симметричной сенсомоторной полинейропатией (DSPN) с физиологическими особенностями потери аксонов.
-
Сахарный диабет (СД) — наиболее частая причина периферической невропатии в США и Европе. Риск развития периферической нейропатии коррелирует с продолжительностью СД, гликемическим контролем и наличием ретинопатии и нефропатии [8]. Дистальная симметричная сенсомоторная полинейропатия (ДСПН) является наиболее распространенной формой диабетической невропатии; однако с диабетом связаны множественные формы невропатии. Исследования нервной проводимости обычно показывают зависимую от длины, смешанную демиелинизирующую и аксональную полинейропатию, и это коррелирует с данными биопсии нервов по дегенерации аксонов, регенеративным кластерам и сегментарной демиелинизации.Вегетативные и сенсорные нервные волокна активно участвуют в диабетической DSPN. У некоторых пациентов с диабетом развивается «диабетическая амиотрофия», также известная как «диабетическая пояснично-крестцовая радикулоплексопатия», которая проявляется относительно внезапной, сильной, асимметричной болью в проксимальных отделах бедер, часто длящейся несколько месяцев. Часто развивается мышечная слабость и атрофия проксимальных мышц бедра, хотя течение диабетической амиотрофии носит однофазный характер, и состояние пациентов обычно улучшается без лечения. Некоторые патологические исследования выявили инфильтрацию воспалительных клеток в различных местах корней и периферических нервов у пациентов с диабетической амиотрофией, что свидетельствует об аутоиммунной этиологии [9, 10].Однако эффективность иммунотерапии ВВИГ или преднизоном сомнительна из-за ее благоприятного исхода даже без какого-либо лечения. ()
Таблица 4
Невропатия, связанная с диабетом
Дистальная симметричная сенсомоторная полинейропатия Автономная невропатия
Диабетическая полирадикулоневропатия Диабетическая полирадикулоневропатия ) • Симметричная, безболезненная, полирадикулопатия • Шейная или торакальная радикулопатия
Фокальные мононевропатии • Черепная нейропатия невропатия невропатия -
Гипотиреоз чаще всего предрасполагает пациентов к нейропатии защемления, такой как синдром запястного канала, но редко может вызывать генерализованную сенсорную невропатию, характеризующуюся болезненным пародонтом. эстезия и онемение в дистальных отделах конечностей [11].
-
Дефицит витамина B12 (кобаламина) вызывает периферическую невропатию в дополнение к классическому проявлению «подострой комбинированной дегенерации», относящейся к потере спинных столбов и кортикоспинальных трактов в спинном мозге, что приводит к потере проприоцепции и вибрационной чувствительности. к гиперрефлексии. Невропатия, связанная с дефицитом витамина B12, может наблюдаться не только у строгих вегетарианцев, но и у пациентов, перенесших бариатрическую операцию.
-
Прочие дефициты витаминов.Витамин B1 (тиамин) и дефицит витамина E — редкие причины периферической невропатии. Дефицит тиамина может возникать у пациентов с хроническим употреблением алкоголя. Следует отметить, что как дефицит, так и передозировка витамина B6 (пиридоксина) могут вызывать периферическую невропатию.
-
Уремическая невропатия относится к нейропатии, связанной с почечной недостаточностью. Примерно у 60% пациентов с хронической почечной недостаточностью (обычно при скорости клубочковой фильтрации менее 12 мл / мин) развивается ДСПН [12].Мононевропатии, особенно синдром запястного канала, распространены и, как полагают, связаны с накоплением бета2-микроглобулина во время гемодиализа.
-
Хроническая болезнь печени — еще одна причина невропатии. В одном исследовании DSPN был обнаружен у 71%, а вегетативная нейропатия — у 48% пациентов [13].
Воспалительная и иммуноопосредованная нейропатия
Иммуноопосредованная невропатия представляет собой гетерогенную группу заболеваний, при которых иммунологический процесс может быть направлен либо на периферические нервы, либо на поддерживающие кровеносные сосуды.Миелин периферических нервов — обычная мишень при демиелинизирующей нейропатии. При васкулитной нейропатии патологический процесс возникает в кровеносных сосудах и приводит к ишемии нервов, что приводит к нейропатии, характеризующейся мультифокальной потерей сенсорных и моторных аксонов.
-
Синдром Гийена-Барре (СГБ) является наиболее частой причиной острого вялого паралича во всем мире [14]. СГБ не является отдельным заболеванием, а охватывает несколько типов острых иммуноопосредованных полинейропатий ().
-
Антецедентное заболевание: Около двух третей пациентов с СГБ в течение нескольких предшествующих недель имели заболевание, обычно респираторную или желудочно-кишечную инфекцию. Цитомегаловирус — наиболее часто встречающаяся вирусная инфекция. Campylobacter jejuni, вызывающая гастроэнтерит, является наиболее часто ассоциированной бактериальной инфекцией. Вакцинация может увеличить риск СГБ.
-
AIDP Клинические особенности: СГБ обычно первоначально проявляется онемением и покалыванием в стопах и руках.Даже на ранней стадии рефлексы растяжения мышц обычно теряются или ослабевают. Прогрессирующая слабость сопровождает сенсорное нарушение, обычно восходящее. Однако у некоторых пациентов слабость с самого начала затрагивает проксимальные или осевые мышцы, а слабость лица часто проявляется по крайней мере у половины пациентов в течение болезни. У некоторых пациентов могут развиваться офтальмопарез и бульбарный паралич, и наиболее тревожным признаком является дыхательная недостаточность из-за слабости диафрагмы.
-
Axonal GBS редко встречается в США и Европе, но широко распространен в Азии [15]. AMAN имеет исключительно двигательные признаки со слабостью, обычно начинающейся в ногах. Сухожильные рефлексы сохраняются до сильной слабости. Возможна дыхательная недостаточность. AMSAN клинически и физиологически подобен, но с обнаруживаемым сенсорным вмешательством.
-
Синдром Миллера-Фишера (MFS) характеризуется атаксией, арефлексией и офтальмоплегией. Существует спектр между MFS и энцефалитом Бикерстаффа, который характеризуется атаксией, офтальмоплегией, нарушениями сознания и дисфункцией пирамидного тракта, связанными с МРТ головного мозга, показывающими поражения ствола мозга, повышающие содержание гадолиния.Этим синдромам обычно предшествует инфекция C.jejuni или Mycoplasma, и они связаны с антителами против GQ1b [16].
-
Электрофизиология: NCS при AIDP демонстрирует типичные особенности демиелинизации, включая длительные латентные периоды в дистальных отделах, медленные скорости проводимости, временную дисперсию, блокаду проводимости и длительные латентные периоды F-волн. При аксональном GBS NCS выявляет низкую амплитуду или недоступность CMAPS и / или SNAP, а EMG показывает острую и хроническую денервацию. При синдроме Миллера-Фишера NCS выявляет снижение амплитуды SNAP, непропорционально любому удлинению дистальных латентных периодов или замедлению скорости сенсорной проводимости.CMAP в верхних и нижних конечностях обычно нормальны.
-
Исследования: СМЖ показывает альбуминоцитологическую диссоциацию (повышенные уровни белка СМЖ, сопровождающиеся небольшим количеством мононуклеарных клеток) более чем у 80% пациентов с СГБ через 2 недели. Увеличение нервных корешков можно увидеть на МРТ позвоночника при AIDP. Антиганглиозидные антитела, особенно антитела GM1 IgG, обнаруживаются у некоторых пациентов с AIDP и коррелируют с недавней инфекцией C. jejuni . Серологические данные недавнего C.jejuni с антителами к GM1 или GD1a демонстрируется у большинства пациентов с AMAN; Антитела GM1 обнаруживаются у большинства пациентов с AMSAN [17], а антитела к GQ1b обнаруживаются у многих пациентов с синдромом Миллера-Фишера [16]. Молекулярная мимикрия между ганглиозидами, экспрессируемыми на нервных волокнах, и гликолипидами, присутствующими на C. jejuni , может объяснять их ассоциацию и играть роль в патогенезе заболевания.
-
Прогноз: Скорость прогрессирования СГБ варьируется; у более чем 90% пациентов нижний предел достигается в течение 1 месяца.Тяжесть поражения варьируется от минимальной слабости до полной квадриплегии и необходимости искусственной вентиляции легких. У многих пациентов может возникнуть вегетативная дисфункция. За фазой прогрессирования следует фаза плато, за которой следует восстановление. Плохие прогностические факторы включают пожилой возраст, высокую скорость прогрессирования, потерю аксонов на NCS и сильную слабость в надире. Считается, что иммунотерапия ускоряет выздоровление, но не меняет окончательного прогноза [18-20]. Восстановление может занять много месяцев и может быть неполным.Примерно 15% пациентов с СГБ имеют функционально значимые остаточные нарушения [21].
Таблица 5
Синдромы Гийена-Барре
Острая воспалительная демиелинизирующая полинейропатия (AIDP) Синдром Миллера-Фишера (MFS): атаксия, арефлексия и офтальмоплегия 1Острая моторная аксональная нейропатия (AMAN) Острая моторно-сенсорная аксональная нейропатия (AMSAN) -
-
Хроническая воспалительная демиелинизирующая полинейропатия (CIDP) — это приобретенная иммуноопосредованная периферическая хроническая нейропатия. прогрессирующее или рецидивирующее ремиттирующее расстройство [22].
-
Клинические признаки: при типичном ХВДП двигательный и сенсорный дефицит постепенно развиваются в течение месяцев (минимум 8 недель), часто приводя к значительной инвалидности. У большинства пациентов проявляется прогрессирующая симметричная проксимальная и дистальная слабость верхних и нижних конечностей с онемением и парестезиями в конечностях. Как и при AIDP, рефлексы обычно отсутствуют или заметно ослаблены, а обследование выявляет потерю сенсорных модальностей крупных волокон (вибрация и проприоцепция).Поражение черепных нервов (офтальмопарез, лицевая или бульбарная слабость) наблюдается примерно в 15% случаев. Пациенты с длительным хроническим заболеванием ВДП могут иметь симптомы, типичные для поясничного стеноза и дисфункции конского хвоста. В некоторых случаях гипертрофия нервных корешков может вызывать скученность и защемление корней в пояснично-текальном мешке и поясничном позвоночном канале, включая нервные отверстия [23].
-
Исследования: Как и в случае AIDP, диагноз CIDP подтверждается данными цитоальбуминергической диссоциации и электродиагностическими данными демиелинизации нескольких двигательных нервов.Биопсия нерва выполняется в необычных случаях, например, у пациентов с асимметричным предлежанием и болью, у которых есть опасения по поводу других патологий, таких как васкулит. Биопсия обычно выявляет воспаление и демиелинизацию в дополнение к легкой дегенерации аксонов. Лабораторные исследования должны включать количественную оценку сывороточных иммуноглобулинов и скрининг на моноклональные гаммопатии в сыворотке и моче с помощью иммуноэлектрофореза и иммунофиксации. При обнаружении каппа- или лямбда-легких цепей необходимо проконсультироваться с гематологом и провести биопсию костного мозга, чтобы исключить лимфопролиферативное заболевание или злокачественную дискразию плазматических клеток.Радиологическое исследование скелета должно быть выполнено для поиска остеосклеротической или остеолитической миеломы.
-
Прогноз: течение ХВДП может быть непрерывным, ступенчато-прогрессирующим или рецидивирующим. Большинство пациентов реагируют на иммунотерапию (стероиды, плазмаферез или внутривенный гаммаглобулин), и клинический ответ может помочь в диагностике. У пациентов, которые плохо реагируют на иммунотерапию, следует рассматривать варианты CIDP ().
Таблица 6
CIDP с сопутствующим заболеванием
ВИЧ-инфекция Лимфома Остеосклеротическая миелома, POEMS (полинейропатия, органомегалия, эндокринопатия, моноклональная гриппа Хронический активный гепатит, гепатит С Воспалительное заболевание кишечника Заболевание соединительной ткани Пересадка костного мозга и органов Демиелинизация центральной нервной системы Диабет Нефротический синдром 1Наследственная нейропатия Тиреотоксикоз
-
-
Мультифокальная моторная нейропатия (MMN) — это приобретенная иммуноопосредованная асимметричная моторная нейропатия с фокальной моторикой. блок проводимости по электрофизиологическому исследованию.
-
Клинические особенности. Как правило, MMN возникает в возрасте от 20 до 50 лет, и мужчины поражаются в три раза чаще, чем женщины. Как следует из названия, MMN — это асимметричная моторная нейропатия, которая имеет склонность к верхним конечностям, особенно к нервам, иннервирующим предплечье, и внутренним мышцам руки, ведущим к опущению запястья. Сенсорное вмешательство минимально. Могут наблюдаться фасцикуляции и судороги, что часто вызывает беспокойство при диагностике заболевания двигательных нейронов.Большинство случаев идет медленно прогрессирующим течением.
-
Электрофизиология: очаговая проводимость моторных волокон вне обычных участков защемления является отличительной чертой MMN. Исследования сенсорной проводимости, полученные на одних и тех же участках моторного блока, являются нормальными. Блок проводимости определяется как значительное уменьшение амплитуды вызванного комбинированного мышечного потенциала действия (CMAP) или площади между дистальным и проксимальным участками стимуляции вдоль фокального сегмента нерва при отсутствии аномальной временной дисперсии.
-
Исследования: антитела IgM к GM1 присутствуют примерно в 50% случаев [24].
-
-
Парапротеинемическая невропатия. Моноклональная гаммапатия (или парапротеин), выявленная при электрофорезе сыворотки или мочи, часто обнаруживается у пациентов с нейропатией [25]. IgG — наиболее распространенный парапротеин, за ним следуют IgM и IgA. Моноклональная гаммопатия может быть связана с гематологическими нарушениями, такими как множественная миелома, лимфома, плазмоцитома, глобулинемия Вальденстрема, амилоидоз, криоглобулинемия и хронический лимфолейкоз.Если детальная гематологическая оценка отрицательна, используется термин моноклональная гаммопатия неопределенного значения. Даже если первоначальная оценка отрицательная, этих пациентов следует периодически наблюдать. Связь между парапротеином и невропатией наиболее сильна с IgM. Некоторые парапротеинемические невропатии могут быть вызваны иммунореактивностью парапротеина, тогда как у пациентов с известным гематологическим заболеванием патогенные механизмы, такие как инфильтрация нервов, криоглобулинемия, амилоидоз или повышенная вязкость, могут играть роль.В других случаях парапротеин не может быть причиной невропатии.
-
Гаммопатия IgM: Большинство невропатий, наблюдаемых в связи с гаммопатией IgM, являются демиелинизирующими. Около 50% пациентов с периферической нейропатией и гаммопатией IgM имеют антитела IgM, которые связываются с миелин-ассоциированным гликопротеином (MAG). У этих пациентов наблюдаются медленно прогрессирующие парестезии дистальных отделов конечностей, потеря чувствительности, атаксия походки и тремор с легкой или нулевой слабостью. Это состояние также называют дистальной приобретенной демиелинизирующей симметричной (DADS) невропатией.Исследование нервной проводимости часто показывает заметно увеличенный дистальный латентный период с незначительным снижением скорости проводимости.
-
Синдром POEMS (полинейропатия, органомегалия, эндокринопатия, моноклональная гаммопатия и изменения кожи) — редкое паранеопластическое заболевание, которое обычно возникает у пациентов с остеосклеротической миеломой, но может возникать в связи с макроглобулинемией Вальденстрема или плазмоцитомой. Наиболее распространенным парапротеином является лямбда-цепь IgG или IgA. Клинические и электрофизиологические признаки нейропатии аналогичны ХВДП, но обычно не поддаются иммуносупрессивному лечению.Уровни VEGF в сыворотке часто заметно повышены.
-
Васкулитная невропатия
Васкулитная невропатия — это иммуноопосредованное заболевание, направленное против кровеносных сосудов, приводящее к ишемии и инфаркту периферической нервной системы. [26] Поражение васкулитом периферических нервов обычно вызывает множественные очаговые ишемические поражения. Клиническая картина обычно изначально представляет собой одну из множественных мононевропатий (также называемых множественным мононевритом), но со временем может развиться в дистальную симметричную полинейропатию.Пациенты обычно поступают с острым началом боли и прогрессирующим сенсорным и двигательным дефицитом в распределении определенных нервов. Клиническое течение может быть поэтапным или прогрессивным. ()
-
Диагноз: Электродиагностическое исследование часто показывает картину множественного мононеврита. Лабораторные исследования выполняются для оценки системных форм васкулита (), включая общий анализ крови, СОЭ, С-реактивный белок, функции почек и печени, электролиты, анализ мочи, гликированный гемоглобин, электрофорез иммунофиксации сыворотки, уровни комплемента, криоглобулины, поверхностный гепатит В. антиген, антитело к гепатиту С, антитело к ВИЧ, антинуклеарные антитела, ревматоидный фактор, антитела SSA и SSB, антинейтрофильные цитоплазматические антитела.Окончательный диагноз васкулитной невропатии ставится с помощью биопсии клинически или электрофизиологически пораженного нерва, предпочтительно икроножного или поверхностного лучевого сенсорного нерва. Патологические признаки васкулитной нейропатии включают изменения сосудистой стенки в результате трансмурального воспаления, фибриноидный некроз, эндотелиальное повреждение и кровоизлияние, тромбоз, эндотелиальную гиперплазию, фиброз сосудистой стенки, фрагментацию эластической мембраны, сужение или закупорку просвета, реканализацию, клиновидную аксональность. выпадение, центрально-фасцикулярная дегенерация, субпериневральный отек и вариабельность от пучка к пучку ().Комбинированная биопсия нерва и мышцы повышает диагностическую чувствительность.
Таблица 7
Васкулит, связанный с невропатией
| Первичный системный васкулит |
| Крупные сосуды |
| Гигантоклеточный артериит |
| Средние сосуды |
| Полиартериит сосуды |
| Микроскопический полиангиит |
| Синдром Чарджа-Стросса |
| Гранулематоз Вегенера |
| Вторичный системный васкулит |
| Заболевания соединительной ткани |
| Синдром Шегрена |
| Дерматомиозит |
| Воспалительное заболевание кишечника |
| Болезнь Бехчета |
| Саркоидоз |
| Инфекция |
| Гепатиты B и C, ВИЧ |
| Злокачественные новообразования |
| Несистемный васкулит |
Наследственная девятилетняя невропатия болезнь (CMT), наследственные моторные и сенсорные невропатии (HMSN) охватывают самую большую группу наследственных невропатий.Эти заболевания обычно классифицируются на основе клинической картины (возраст начала и характер наследования) и патологии / электрофизиологии (аксональная: CMT1 против демиелинизирующей: CMT2) [27, 28].
-
Клинические особенности. У большинства пациентов с ШМТ, начиная с детства или раннего взросления, постепенно развиваются прогрессирующая слабость и атрофия стоп. Боль или потеря чувствительности могут быть разными, но обычно не являются главной жалобой. Деформации стопы (кавернозная стопа, высокие своды стопы и молоточковые пальцы стопы) являются обычным явлением и могут привести к инвалидности.Из-за коварного характера этого заболевания большинство пациентов не жалуются на двигательные или сенсорные симптомы до поздних стадий заболевания, и большинство пациентов остаются амбулаторно. При осмотре пациенты обычно имеют дистальную слабость и атрофию стоп, арефлексию и зависимую от длины сенсорную потерю сенсорных модальностей как крупных, так и мелких волокон. У пациентов с более тяжелым поражением разовьется сенсорная атаксия или тремор (синдром Русси-Леви), пальпируемое увеличение нервов (CMT1), слабость, атрофия и потеря чувствительности рук.Пациенты без признаков сенсорного вовлечения при осмотре или электродиагностическом тестировании классифицируются как имеющие наследственную моторную невропатию, тогда как пациенты без доказательств моторного вовлечения классифицируются как наследственная сенсорная или наследственная сенсорная и вегетативная нейропатия.
-
Электрофизиология. При клиническом подозрении на ШМТ наиболее полезным тестом является исследование нервной проводимости. Исследования нервной проводимости обычно позволяют классифицировать заболевание как преимущественно аксональное или демиелинизирующее.Например, наиболее распространенная форма CMT, CMT1A, обычно показывает заметное и равномерное снижение моторной и сенсорной скорости проводимости (обычно 10-30 м / сек). Наследственная невропатия с предрасположенностью к параличам от сдавливания (HNPP) показывает более умеренное замедление скорости проводимости, но часто показывает очаговое замедление или блокаду проводимости в общих местах защемления. Классификация заболевания как аксонального или демиелинизирующего часто может ограничивать необходимое генетическое тестирование, поскольку общие мутации, вызывающие CMT1 (демиелинизирующие), в целом отличаются от мутаций, вызывающих CMT2 (аксональные).
-
Диагностика. Обычно подозрение на ШМТ возникает при наличии в семейном анамнезе периферической нейропатии, поскольку большинство форм ШМТ являются аутосомно-доминантными. Реже ШМТ может быть Х-сцепленным, аутосомно-рецессивным или спорадическим. Примерно 2/3 CMT относится к типу 1, а ~ 2/3 CMT1 — к CMT1A, что вызвано дупликацией гена периферического миелинового протеина 22 (PMP22). Наиболее частая причина аксональной CMT (CMT2A) вызвана мутациями в гене mitofusin2 (MFN2); Как следует из названия, митофузия регулирует слияние митохондрий, процесс, который считается важным для поддержания здоровья аксонов.Хотя лечение определенных форм ШМТ еще не доступно, генетическое тестирование потенциально может дать окончательный диагноз, недоступный никакими другими способами, и может избежать инвазивного тестирования (например, биопсии нерва) и ненужного лечения (например, внутривенного гамма-глобулина). Генетическое тестирование также имеет важное значение для других членов семьи и планирования семьи, и его следует проводить вместе с генетическим консультированием. Когда у пациентов с CMT1 выполняется биопсия нерва, они обычно демонстрируют классический вид «луковиц» (), вызванный тяжелой хронической демиелинизацией и ремиелинизацией.
Невропатии, связанные с амилоидным белком
Амилоиды представляют собой нерастворимые агрегаты различных белков, которые имеют общую трехмерную структуру β-складчатых листов и устойчивы к протеолитическому разложению. Амилоидоз относится к множеству состояний, при которых амилоидный белок накапливается в любом органе, включая периферические нервы, что приводит к дисфункции. Амилоидные отложения имеют характерное яблочно-зеленое двойное лучепреломление при окрашивании конго красным и видимом под поляризационным микроскопом, а также могут быть обнаружены при биопсии нерва ().Амилоидоз может быть приобретенным или наследственным. Приобретенный амилоидоз может быть следствием аномального накопления белка на фоне множественной миеломы, макроглобулинемии Вальденстрема, лимфомы или лимфопролиферативных заболеваний. Полинейропатия развивается примерно у 30% пациентов с приобретенным первичным амилоидозом, что может быть характерным симптомом [29]. Существует склонность к невропатии мелких волокон, вызывающей болезненное жжение в дистальных отделах конечностей. Исследование нервной проводимости обычно показывает симметричную, зависимую от длины сенсомоторную полинейропатию; однако у некоторых пациентов наблюдаются асимметричные множественные мононевропатии.В случае первичного амилоидоза также очень часто встречается синдром запястного канала. Семейный амилоидоз чаще всего вызывается мутациями в гене транстиретина (TTR), но редко может быть вызван мутациями в аполипопротеине A1 или гельсолине.
Васкулитная невропатия: на пластиковом срезе, окрашенном толуидиновым синим, видно поразительное изменение плотности волокон от пучка к пучку в двух соседних пучках. В этом разделе также можно оценить легкий субпериневриальный отек.
Токсическая нейропатия
С практической точки зрения часто бывает трудно доказать причинно-следственную связь при подозрении на токсическую невропатию [30].Однако не следует пренебрегать поиском причины, поскольку токсическая невропатия является одним из тех состояний, при которых доступно лечение, если она диагностирована своевременно. Хотя многие клиницисты рассматривают токсическую невропатию как диагноз исключения, мы обнаружили, что очень полезно использовать инструменты количественного измерения, такие как общий балл невропатии (TNS), чтобы лучше оценить временное соотношение тяжести заболевания и предполагаемого токсина. Показано, что при некоторых невропатиях, вызванных химиотерапией, TNS коррелирует с дозой химиотерапевтических агентов, подтверждая его использование для установления причинно-следственной связи [7].
Большинство токсичных нейропатий вызывают дистальную, зависящую от длины периферическую невропатию, независимо от токсина. Как кратко упоминалось в предыдущем разделе, нейротоксины влияют на всю длину нерва, от его клеточного тела до терминального аксона, более серьезно влияя на дистальную часть. Эта «умирающая» невропатия очень распространена при большинстве форм нейропатии, что затрудняет диагностику токсической нейропатии. Следовательно, другие системные особенности могут быть ключом к диагностике определенных токсических невропатий. Например, токсическая нейропатия, вызванная отравлением мышьяком, может проявлять не только типичную невропатию, зависящую от длины тела, но также и системные симптомы, такие как симптомы со стороны желудочно-кишечного тракта, психоз и / или линия Ми на ногтях.Токсины, которые могут вызывать невропатию, и их патофизиологические характеристики кратко описаны в.
Таблица 8
Общие токсины, которые могут вызывать невропатию
| Токсины | Клинические особенности | Патофизиология |
|---|---|---|
| Алкалоиды барвинка | Симметричная сенсомоторная полинейропатия крупных и мелких волокон | Смешанная дегенерация аксонов и демиелинизация |
| | ||
| Цисплатин | Сенсорная нейронопатия преимущественно крупных волокон | Сенсорная нейронопатия |
| | ||
| Таксаны | Симметричная преимущественно сенсорная полинейропатия | Дегенерация аксонов |
| | ||
| Амиодарон | Сильная проксимальная и дистальная слабость, поражающая ноги больше, чем руки | Демиелинизирующая |
| | ||
| Колхицин | Проксимальная слабость из-за сопутствующей миопатии и потери чувствительности к прикосновению / вибрации | Дегенерация аксонов |
| | ||
| Свинец | Коварная прогрессирующая слабость в верхних конечностях с минимальным вовлечением органов чувств; Симптомы со стороны желудочно-кишечного тракта, синевато-черная линия окраски десен («свинцовая линия») | Дегенерация аксонов |
| | ||
| Алкоголь | Медленно прогрессирующая парастезия, онемение и жгучая боль, более сильные в ногах; вегетативная дисфункция является обычным явлением | Общая сенсомоторная, в первую очередь аксональная полинейропатия |
Нейропатии, связанные с аутоиммунным заболеванием
-
Синдром Шегрена .Периферическая нейропатия присутствует у 10–22% всех пациентов с синдромом Шегрена [31, 32]. Общие формы невропатии включают зависимую от длины аксональную сенсомоторную нейропатию, невропатию мелких волокон и сенсорную нейронопатию.
-
Ревматоидный артрит (РА) . Сообщается, что около 50% пациентов с ревматоидным артритом страдают невропатией, чаще всего из-за защемления [33]. Васкулитная невропатия также может развиваться у пациентов с РА, что делает ее третьей по частоте причиной васкулитной нейропатии в одной серии случаев [34] после узелкового полиартериита и изолированного васкулита периферической нервной системы.Также важно исключить токсическую невропатию, связанную с модифицирующими болезнь противоревматическими препаратами.
-
Системный склероз. Хотя сенсорные жалобы являются обычным явлением и сообщаются до 50% пациентов со склеродермией, распространенность полинейропатии считается низкой [35, 36]. У пациентов с синдромом CREST описаны множественные мононевропатии.
-
Системная красная волчанка (СКВ). СКВ — относительно распространенное мультисистемное заболевание, часто поражающее нервную систему.Хотя СКВ чаще поражает центральную нервную систему, сообщается, что около четверти пациентов с СКВ страдают периферической невропатией [37]. Пациенты обычно жалуются на медленно прогрессирующую потерю чувствительности в дистальных отделах. Сообщается о множественных мононевропатиях, но они встречаются реже.
-
Смешанное заболевание соединительной ткани . Сообщается, что легкая дистальная аксональная сенсомоторная полинейропатия встречается примерно у 10% пациентов [38].
-
Саркоидоз .Центральная и периферическая нервная система может быть поражена саркоидозом. Обычно поражаются черепные нервы, чаще всего лицевой нерв. В одном исследовании были проанализированы клинические особенности 57 пациентов с саркоидной невропатией; наиболее распространенным паттерном был монофазный, асимметричный и не зависящий от длины [39].
-
Целиакия . Около 10% пациентов с глютеновой болезнью имеют неврологические осложнения, из которых наиболее распространены атаксия и периферическая нейропатия.Периферическая нейропатия, связанная с глютеновой болезнью, проявляется дистальными сенсорными органами [40]. Сообщается также о генерализованной сенсомоторной полинейропатии, моторной нейропатии, множественных мононевропатиях, вегетативной нейропатии и нейромиотонии.
-
Воспалительное заболевание кишечника . Язвенный колит и болезнь Крона — воспалительные заболевания кишечника, связанные с различными неврологическими осложнениями, включая периферическую невропатию. Сообщалось о AIDP, CIDP, сенсорной нейропатии, сенсомоторной нейропатии, нейропатии мелких волокон, плечевой плексопатии, множественных мононевропатиях и черепной нейропатии [41].
-
Первичный билиарный склероз . Периферическая невропатия, связанная с первичным билиарным склерозом, характеризуется онемением дистальных отделов и покалыванием. На сенсорные модальности крупных волокон преимущественно влияет первичный билиарный склероз [42].
-
Гиперэозинофильный синдром . Генерализованная периферическая нейропатия из множественных мононевропатий встречается у 6–14% пациентов с гиперэозинофическим синдромом [43].
Невропатии, связанные с инфекцией
-
Проказа вызывается кислотоустойчивыми бактериями Mycobacterium leprae и является наиболее частой причиной периферической невропатии в развивающихся странах, включая Юго-Восточную Азию, Африку и Южную Америку.Медленно прогрессирующая сенсомоторная полинейропатия постепенно развивается из-за обширной инвазии бацилл в нервные волокна [44].
-
Болезнь Лайма вызывается инфекцией Borrelia burgdorferi , которая передается клещами. Существует три стадии болезни Лайма: первая стадия — раннее инфицирование мигрирующей эритемой, вторая стадия — диссеминированная инфекция, а третья стадия — поздняя инфекция. На второй и третьей стадиях инфекции могут развиться неврологические осложнения.При болезни Лайма могут возникать различные невропатии, наиболее распространенная невропатия лица. Мононевропатии, полирадикулопатия и плексопатия также связаны с болезнью Лайма [45]. Проявление полирадикулопатии может напоминать синдром Гийана-Барре. Также важно отметить, что ложноположительные результаты серологических тестов Лайма являются обычным явлением, и поэтому для подтверждения результатов необходимо выполнить вестерн-блоттинг.
-
Дифтерийная невропатия вызвана токсином, выделяемым бактериями. Corynebacterium diphtheria . Черепные нервы могут быть поражены через 3-4 недели после заражения. Генерализованная полинейропатия может развиться через 2-3 месяца после появления первых симптомов.
-
Вирус иммунодефицита человека (ВИЧ) инфекция может вызывать различные неврологические осложнения, включая периферическую невропатию. Около 20% пациентов с ВИЧ-инфекцией развивают невропатию в результате самой вирусной инфекции, оппортунистических инфекций, таких как цитомегаловирусная инфекция, или нейротоксичности от противовирусных препаратов.Наиболее распространенные формы периферических невропатий, связанных с ВИЧ, включают дистальную симметричную полинейропатию, воспалительную демиелинизирующую полинейропатию (острую или хроническую), множественные мононевропатии, полирадикулопатию, вегетативную невропатию и сенсорный ганглинит [46]. Среди них дистальная симметричная полинейропатия является наиболее распространенной формой и обычно наблюдается у пациентов со СПИДом. Во время сероконверсии может развиться острая воспалительная демиелинизирующая полинейропатия.
-
Вирус Т-лимфоцитов человека 1 типа (HTLV-1) связан с аксональной зависимой от длины сенсомоторной полинейропатией, которая проявляется при отсутствии миелопатии [47].
-
Цитомегаловирус (ЦМВ) может вызывать острую пояснично-крестцовую полирадикулопатию и множественные мононевропатии у пациентов с ослабленным иммунитетом.
-
Вирус Эбштейна-Барра (EBV) связан с острой воспалительной демиелинизирующей невропатией, краниальной невропатией, множественными мононевропатиями, плечевой плексопатией, пояснично-крестцовой радикулоплексопатией и сенсорными нейронопатиями.
-
Вирус ветряной оспы (VZV) может вызывать невропатию из-за реактивации латентного вируса или первичной инфекции.Первичная инфекция вызывает «ветряную оспу», а реактивация вируса в более позднем возрасте приводит к появлению кожного опоясывающего лишая. У большинства взрослых пациентов возникает сильная боль и парасетезия в дерматомной области с везикулярной сыпью. У некоторых пациентов также развивается мышечная слабость в той же миотомной области. Редко у пациентов с VZV развивается острая воспалительная демиелинизирующая нейропатия.
-
Вирусы гепатита B и C могут вызывать васкулитную невропатию, часто связанную с криоглобулинемией.
Невропатии, связанные со злокачественными новообразованиями
-
Паранеопластическая невропатия относительно редка и чаще всего связана с раком легких. В частности, паранеопластическая сенсорная нейронопатия / ганглинопатия чаще всего возникает при мелкоклеточном раке легкого (часто связанном с антителами против Hu) и может предшествовать диагностике рака на 4–12 месяцев [48–50]. Причины сенсорной нейронопатии ограничены, и при распознании необходимо провести тщательную диагностику злокачественных новообразований.Кроме того, у пациентов с раком могут развиваться симметричная сенсомоторная полинейропатия и паранеопластическая вегетативная нейропатия.
-
Невропатия, вторичная по отношению к инфильтрации опухоли . Прямая инфильтрация опухолевых клеток в лептоменинги, черепные нервы и нервные корешки может вызвать дисфункцию периферической нервной системы. Это особенно характерно для лейкемии и лимфомы, приводя к мононевропатии, множественным мононевропатиям, полирадикулопатии, плексопатии и генерализованной симметричной дистальной или проксимальной полинейропатии.Особенно распространены полирадикулопатии, а МРТ может показать сдавление опухолью нескольких нервных корешков.
-
Периферические невропатии, связанные с лимфопролиферативными нарушениями. Существует повышенная частота периферической нейропатии у пациентов с моноклональной гаммопатией, и имеется четко установленная причинно-следственная связь между моноклональной гаммапатией IgM и демиелинизирующей сенсомоторной полинейропатией [51]. Антитела против миелин-ассоциированного гликопротеина (MAG) обнаруживаются у пациентов с лимфопролиферативными нарушениями или плазмоцитомами, тогда как моноклональные гаммапатии IgA и IgG встречаются гораздо реже.Множественная миелома обычно связана с дистальной аксональной сенсомоторной полинейропатией. Остеосклеротическая миелома встречается редко, но обычно связана с полинейропатией, иногда одновременно проявляясь гепатоспленомегалией, кожной пигментацией, гипертрихозом, отеком, перикардиальными и плевральными выпотами, так называемым синдромом POEMS (полинейропатия, органегалия, эндокринопатия, М-белок и кожные аномалии). Синдром POEMS также связан с болезнью Кастлемана (гиперплазия ангиофолликулярных лимфатических узлов).
-
Болезнь трансплантат против хозяина (РТПХ) может вызывать различные иммуноопосредованные расстройства, в том числе расстройства периферической нервной системы. Сообщалось о синдроме Гийена-Барре, множественных мононевропатиях и черепной нейропатии у пациентов с РТПХ [52].
Резюме
Периферические нервы поражаются широким спектром заболеваний. Благодаря техническим достижениям, которые позволяют проводить МРТ с высоким разрешением, периферическая нейровизуализация становится все более полезной при оценке заболеваний периферических нервов.МР-нейрография особенно полезна при оценке поражений проксимальных нервов, которые трудно оценить с помощью исследования нервной проводимости; например, МР-нейрография не только обеспечит лучшую диагностику опухоли, сдавливающей плечевое сплетение, чем электрофизиологическое исследование, но также поможет нейрохирургам в их плане лечения. Тем не менее, для радиологов важно иметь представление о различных периферических нервных расстройствах и сообщать полученные результаты лечащим врачам, включая неврологов и нейрохирургов, для оптимального ведения пациентов.
ОкраскаCongo Red показывает двойное лучепреломление яблочно-зеленого цвета под поляризационным микроскопом. Обратите внимание, что аморфный материал с двойным лучепреломлением проникает в стенку сосуда.
Ключевые моменты
-
Дистальная симметричная сенсомоторная полинейропатия (DSPN), вызванная «умирающей» дегенерацией аксонов, является наиболее распространенной формой полинейропатии и обычно вызывается токсическими / метаболическими состояниями, такими как диабет.
-
Электромиография и исследование нервной проводимости (EMG / NCS) — чрезвычайно полезный тест для определения локализации (анатомический тип и тип нервного волокна), патофизиологии (аксональная или демиелинизирующая), остроты зрения и тяжести невропатий.
-
Аксональные невропатии обычно демонстрируют пониженную амплитуду потенциалов действия на NCS и нейрогенные двигательные единицы на ЭМГ.
-
Демиелинизирующие невропатии проявляются снижением скорости проводимости, временной дисперсией и длительным латентным периодом дистальных и F-волн.
-
МР-нейрография играет важную роль в оценке проксимальных очаговых поражений нервов, которые трудно оценить с помощью ЭМГ / NCS.
Сноски
Заявление издателя: Это PDF-файл неотредактированной рукописи, принятой к публикации.В качестве услуги для наших клиентов мы предоставляем эту раннюю версию рукописи. Рукопись будет подвергнута копирайтингу, верстке и рассмотрению полученного доказательства, прежде чем она будет опубликована в окончательной форме для цитирования. Обратите внимание, что во время производственного процесса могут быть обнаружены ошибки, которые могут повлиять на содержание, и все юридические оговорки, относящиеся к журналу, имеют отношение.
Справочные документы
1. Чхабра А., Андрейсек Г., Солдатос Т., Ван К.С., Фламманг А.Дж., Белцберг А.Дж., Каррино Дж.А.МР-нейрография: прошлое, настоящее и будущее. AJR Am J Roentgenol. 2011; 197: 583–91. [PubMed] [Google Scholar] 2. Thawait SK, Chaudhry V, Thawait GK, Wang KC, Belzberg A, Carrino JA, Chhabra A. МР-нейрография с высоким разрешением диффузных поражений периферических нервов. AJNR Am J Neuroradiol. 2011; 32: 1365–72. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Уильямс И.Р., Гиллиатт Р.В. Регенерация дистальнее длительной блокады проводимости. J Neurol Sci. 1977; 33: 267–73. [PubMed] [Google Scholar] 6. Корнблат Д.Р., Чаудри В., Картер К., Ли Д., Сейседадр М., Миерницки М., Джон Т.Общий балл невропатии: исследование проверки достоверности и надежности. Неврология. 1999; 53: 1660–4. [PubMed] [Google Scholar] 7. Cavaletti G, Frigeni B, Lanzani F, Piatti M, Rota S, Briani C, Zara G, Plasmati R, Pastorelli F, Caraceni A, Pace A, Manicone M, Lissoni A, Colombo N, Bianchi G, Zanna C. Оценка невропатии как инструмент оценки курса периферической нейротоксичности, вызванной химиотерапией: сравнение с Общей шкалой токсичности Национального института рака. J Peripher Nerv Syst. 2007; 12: 210–5.[PubMed] [Google Scholar] 8. Дайк П.Дж., Крац К.М., Карнес Д.Л., Личи В.Дж., Кляйн Р., Пач Дж.М., Уилсон Д.М., О’Брайен П.С., Мелтон Л.Дж., 3-е место, Сервисная ФД. Распространенность по степени тяжести различных типов диабетической нейропатии, ретинопатии и нефропатии в популяционной когорте: Рочестерское исследование диабетической невропатии. Неврология. 1993; 43: 817–24. [PubMed] [Google Scholar] 9. Дайк П.Дж., Норелл Дж. Э. Микроваскулит и ишемия при диабетической пояснично-крестцовой радикулоплексической нейропатии. Неврология. 1999; 53: 2113–21. [PubMed] [Google Scholar] 10.Said G, Elgrably F, Lacroix C, Plante V, Talamon C, Adams D, Tager M, Slama G. Болезненная проксимальная диабетическая невропатия: воспалительные поражения нервов и спонтанный благоприятный исход. Энн Нейрол. 1997; 41: 762–70. [PubMed] [Google Scholar] 11. Nemni R, Bottacchi E, Fazio R, Mamoli A, Corbo M, Camerlingo M, Galardi G, Erenbourg L, Canal N. Полинейропатия при гипотиреозе: клинические, электрофизиологические и морфологические данные в четырех случаях. J Neurol Neurosurg Psychiatry. 1987; 50: 1454–60. [Бесплатная статья PMC] [PubMed] [Google Scholar] 12.Огура Т., Макинодан А., Кубо Т., Хаясида Т., Хирасава Ю. Электрофизиологический курс уремической невропатии у пациентов, находящихся на гемодиализе. Postgrad Med J. 2001; 77: 451–4. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13. Чаудри В., Корс А.М., О’Брайен Р., Корнблат Д.Р., Кляйн А.С., Тулуват П.Дж. Вегетативная и периферическая (сенсомоторная) нейропатия при хроническом заболевании печени: клиническое и электрофизиологическое исследование. Гепатология. 1999; 29: 1698–703. [PubMed] [Google Scholar] 14. Юки Н., Хартунг ХП. Синдром Гийена-Барре.N Engl J Med. 2012; 366: 2294–304. [PubMed] [Google Scholar] 15. Гриффин Дж. У., Ли Си Ю, Хо Т. В., Сюэ П., Макко К., Гао Си, Ян С., Тиан М., Мишу Б., Корнблат ДР. Синдром Гийена-Барре в северном Китае. Спектр невропатологических изменений в клинически определенных случаях. Головной мозг. 1995. 118 (Pt 3): 577–95. [PubMed] [Google Scholar] 16. Папарунас К. Анти-GQ1b ганглиозидные антитела при нарушениях периферической нервной системы: патофизиологическая роль и клиническое значение. Arch Neurol. 2004. 61: 1013–6. [PubMed] [Google Scholar] 17.Огавара К., Кувабара С., Мори М., Хаттори Т., Кога М., Юки Н. Аксональный синдром Гийена-Барре: связь с анти-ганглиозидными антителами и инфекцией Campylobacter jejuni в Японии. Энн Нейрол. 2000; 48: 624–31. [PubMed] [Google Scholar] 18. Лаун Н.Д., Флетчер Д.Д., Хендерсон Р.Д., Вольтер Т.Д., Вейдикс Е.Ф. Прогнозирование ИВЛ при синдроме Гийена-Барре. Arch Neurol. 2001; 58: 893–8. [PubMed] [Google Scholar] 19. Корнблат Д. Р., Меллитс Э. Д., Гриффин Дж. В., Маккханн Г. М., Альберс Дж. В., Миллер Р. Г., Фисби Т. Е., Кваски С.А.Исследования моторной проводимости при синдроме Гийена-Барре: описание и прогностическое значение. Энн Нейрол. 1988; 23: 354–9. [PubMed] [Google Scholar] 20. Маккханн GM, Гриффин JW, Корнблат Д.Р., Меллитс Э.Д., Фишер Р.С., Quaskey SA. Плазмаферез и синдром Гийена-Барре: анализ прогностических факторов и эффекта плазмафереза. Энн Нейрол. 1988; 23: 347–53. [PubMed] [Google Scholar] 21. Флетчер Д.Д., Лаун Н.Д., Вольтер Т.Д., Вейдикс Э.Ф. Отдаленные результаты у пациентов с синдромом Гийена-Барре, которым требуется искусственная вентиляция легких.Неврология. 2000; 54: 2311–5. [PubMed] [Google Scholar] 22. Коллер Х., Кизейер БК, Яндер С., Хартунг ХП. Хроническая воспалительная демиелинизирующая полинейропатия. N Engl J Med. 2005; 352: 1343–56. [PubMed] [Google Scholar] 23. Гинзберг Л., Платтс А.Д., Томас П.К. Хроническая воспалительная демиелинизирующая полинейропатия, имитирующая синдром стеноза поясничного отдела позвоночника. J Neurol Neurosurg Psychiatry. 1995; 59: 189–91. [Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Адамс Д., Кунцер Т., Бургер Д., Чофлон М., Магистрис М.Р., Регли Ф., Стек А.Дж.Прогностическая ценность ганглиозидных антител против GM1 при нервно-мышечных заболеваниях: исследование 180 сывороток. J Neuroimmunol. 1991; 32: 223–30. [PubMed] [Google Scholar] 25. Латов Н. Патогенез и терапия невропатий, ассоциированных с моноклональными гаммопатиями. Энн Нейрол. 1995; 37 (Дополнение 1): S32–42. [PubMed] [Google Scholar] 26. Burns TM, Schaublin GA, Dyck PJ. Васкулитные невропатии. Neurol Clin. 2007. 25: 89–113. [PubMed] [Google Scholar] 27. Lloyd TE, Chaudhry V. Лечение и ведение наследственных невропатий.В: Берторини Т., редактор. Нервно-мышечные расстройства: лечение и лечение. Эльзевир; Филадельфия: 2011. С. 191–213. [Google Scholar] 28. Пацко А, Застенчивый ME. Болезнь Шарко-Мари-Тута и связанные с ней генетические невропатии. Continuum (Миннеап Минн) 2012; 18: 39–59. [PubMed] [Google Scholar] 29. Келли Дж.Дж., младший, Кайл Р.А., О’Брайен П.С., Дайк П.Дж. Естественное течение периферической нейропатии при первичном системном амилоидозе. Энн Нейрол. 1979; 6: 1–7. [PubMed] [Google Scholar] 30. Моррисон Б., Чаудри В. Лекарства, токсические и витаминно-зависимые невропатии.Continuum (Миннеап Минн) 2012; 18: 139–60. [PubMed] [Google Scholar] 31. Gemignani F, Marbini A, Pavesi G, Di Vittorio S, Manganelli P, Cenacchi G, Mancia D. Периферическая невропатия, связанная с первичным синдромом Шегрена. J Neurol Neurosurg Psychiatry. 1994; 57: 983–6. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Lopate G, Pestronk A, Al-Lozi M, Lynch T., Florence J, Miller T., Levine T., Rampy T., Beson B, Ramneantu I. Периферическая невропатия в амбулаторной когорте пациентов с синдромом Шегрена.Мышечный нерв. 2006; 33: 672–6. [PubMed] [Google Scholar] 34. Скотт Д.Г., Бэкон П.А., Племя ЧР. Системный ревматоидный васкулит: клиническое и лабораторное исследование 50 случаев. Медицина (Балтимор) 1981; 60: 288–97. [PubMed] [Google Scholar] 35. Авербух-Хеллер Л., Штайнер И., Абрамский О. Неврологические проявления прогрессирующего системного склероза. Arch Neurol. 1992; 49: 1292–5. [PubMed] [Google Scholar] 36. Понселе А.Н., Коннолли МК. Периферическая нейропатия при склеродермии. Мышечный нерв. 2003. 28: 330–5. [PubMed] [Google Scholar] 37.Сиври А., Хасселик З., Селикер Р., Басгозе О. Раннее выявление неврологических нарушений у пациентов с системной красной волчанкой. Электромиогр Клин Нейрофизиол. 1995; 35: 195–9. [PubMed] [Google Scholar] 38. Розенбаум Р. Нервно-мышечные осложнения заболеваний соединительной ткани. Мышечный нерв. 2001; 24: 154–69. [PubMed] [Google Scholar] 39. Burns TM, Dyck PJ, Aksamit AJ. Естественное течение и отдаленные результаты 57 случаев нейропатии саркоидоза конечностей. J Neurol Sci. 2006. 244: 77–87. [PubMed] [Google Scholar] 40.Чин Р.Л., Сандер Х.В., Браннаган Т.Х., Грин PH, Хейс А.П., Алаедин А., Латов Н. Целиакия. Неврология. 2003. 60: 1581–5. [PubMed] [Google Scholar] 41. Гондим Ф.А., Браннаган Т.Х., 3-й, Сандер Х.В., Чин Р.Л., Латов Н. Периферическая невропатия у пациентов с воспалительным заболеванием кишечника. Головной мозг. 2005; 128: 867–79. [PubMed] [Google Scholar] 42. Charron L, Peyronnard JM, Marchand L. Сенсорная нейропатия, связанная с первичным билиарным циррозом. Гистологические и морфометрические исследования. Arch Neurol. 1980; 37: 84–7. [PubMed] [Google Scholar] 43.Дорфман Л.Дж., Рэнсом Б.Р., Форно Л.С., Кельц А. Невропатия при гиперэозинофильном синдроме. Мышечный нерв. 1983; 6: 291–8. [PubMed] [Google Scholar] 44. Ooi WW, Srinivasan J. Проказа и периферическая нервная система: основные и клинические аспекты. Мышечный нерв. 2004. 30: 393–409. [PubMed] [Google Scholar] 45. Гальперин Дж., Люфт Б.Дж., Фолькман Д.Дж., Даттвайлер Р.Дж. Лайм-нейроборрелиоз. Проявления периферической нервной системы. Головной мозг. 1990; 113 (Pt 4): 1207–21. [PubMed] [Google Scholar] 46. Barohn RJ, Gronseth GS, LeForce BR, McVey AL, McGuire SA, Butzin CA, King RB.Поражение периферической нервной системы у большой группы людей, инфицированных вирусом иммунодефицита человека. Arch Neurol. 1993; 50: 167–71. [PubMed] [Google Scholar] 47. Kiwaki T, Umehara F, Arimura Y, Izumo S, Arimura K, Itoh K, Osame M. Клинические и патологические особенности периферической невропатии, сопровождающейся миелопатией, ассоциированной с HTLV-I. J Neurol Sci. 2003. 206: 17–21. [PubMed] [Google Scholar] 48. Амато А.А., Коллинз МП. Невропатии, связанные со злокачественными новообразованиями. Semin Neurol. 1998. 18: 125–44. [PubMed] [Google Scholar] 49.Денни-Браун Д. Первичная сенсорная нейропатия с мышечными изменениями, связанными с карциномой. J Neurol Neurosurg Psychiatry. 1948; 11: 73–87. [Бесплатная статья PMC] [PubMed] [Google Scholar] 50. Dalmau J, Graus F, Rosenblum MK, Posner JB. Anti-Hu — ассоциированный паранеопластический энцефаломиелит / сенсорная нейронопатия. Клиническое исследование 71 пациента. Медицина (Балтимор) 1992; 71: 59–72. [PubMed] [Google Scholar] 51. Латов Н., Шерман У.Х., Немни Р., Галасси Дж., Шионг Дж. С., Пенн А.С., Чесс Л., Оларте М.Р., Роуленд Л.П., Оссерман Э.Ф.Дискразия плазматических клеток и периферическая невропатия с моноклональными антителами к миелину периферических нервов. N Engl J Med. 1980; 303: 618–21. [PubMed] [Google Scholar] 52. Амато А.А., Барон Р.Дж., Сахенк З., Тутчка П.Дж., Менделл-младший. Полинейропатия, осложняющая трансплантацию костного мозга и солидных органов. Неврология. 1993; 43: 1513–8. [PubMed] [Google Scholar]Демиелинизирующая нейропатия — обзор
Исследования нервной проводимости (NCS) могут определить, является ли невропатия следствием повреждения аксона нерва (аксональная нейропатия) или миелиновой оболочки (демиелинизирующая невропатия).Поскольку количество состояний, вызывающих демиелинизирующую невропатию, довольно ограничено, это различие имеет клиническое значение и помогает сфокусировать диагностическую оценку. В то время как конкретные электрофизиологические данные различаются между наследственными и приобретенными демиелинизирующими невропатиями, замедленная скорость проводимости (<70% от нормы) и длительная дистальная моторная латентность (> 150% от нормы) являются характерными чертами обоих.
Диффузно и равномерно замедленная скорость нервной проводимости убедительно свидетельствует о наследственной демиелинизирующей невропатии.Напротив, переменно замедленные скорости проводимости, блокировка проводимости или аномальная временная дисперсия предполагают приобретенный процесс. Острое повреждение аксона или перерезка нерва могут электродиагностически имитировать блокаду проводимости до того, как произойдет валлеровская дегенерация дистального аксона. Это известно как «блок псевдопроводимости», и его можно прояснить, повторив NCS через несколько дней или недель.
Болезнь Шарко-Мари-Тута (CMT) относится к группе наследственных сенсорных и моторных полинейропатий, классифицированных по электрофизиологическим данным (демиелинизирующие или аксональные) и клиническим и генетическим признакам.Признаки, вызывающие подозрение на наследственную невропатию, включают деформации стопы (т. Е. Каверзную стопу, молоткообразные пальцы) и семейный анамнез схожих невропатий. CMT1A, который вызывается дупликацией в гене PMP22 , составляет ~ 70% наследственных демиелинизирующих невропатий. В настоящее время не существует модифицирующей болезнь терапии для любой формы ШМТ, и лечение состоит в основном из поддерживающей терапии, такой как фиксация и физиотерапия.
Наследственная невропатия со склонностью к параличам от сдавливания (HNPP) вызывает полинейропатию с промежуточными скоростями проводимости, а также множественные демиелинизирующие мононевропатии в местах общего защемления нерва (т.например, срединные невропатии запястий, локтевые невропатии локтей и общие малоберцовые невропатии головок малоберцовой кости). HNPP вызывается делецией PMP22 (аллель с CMT1A). Как и в случае с ШМТ, лечения конкретного заболевания не существует.
У пациентов с демиелинизирующими невропатиями с наследственными особенностями генетическое тестирование может установить окончательный диагноз. Точная стратегия тестирования (т. Е. Тестирование на мутацию одного гена, набор генетических тестов, полное секвенирование экзома) зависит от местной стоимости и доступности различных подходов.Тщательное генетическое тестирование позволит выявить ответственную мутацию гена у 90% пациентов с наследственными демиелинизирующими невропатиями.
Помимо HNPP, множественные демиелинизирующие мононевропатии в местах защемления общих нервов должны побуждать к рассмотрению транстиретинового ( TTR ) наследственного амилоидоза. TTR Наследственный амилоидоз часто вызывает аксональную полинейропатию в дополнение к множественным компрессионным невропатиям, а также связан с сердечными и почечными заболеваниями.Идентификация амилоида TTR необходима при эффективной терапии, модифицирующей заболевание (патизиран и инотерсен).
Синдром Гийена-Барре (СГБ) представляет собой клинически неоднородную группу острых воспалительных невропатий. Наиболее распространенным подтипом является острая воспалительная демиелинизирующая полинейропатия (AIDP), быстро прогрессирующая демиелинизирующая полинейропатия, вызывающая нарастающую слабость и онемение. Варианты Axonal GBS имеют сходные клинические характеристики, но не имеют демиелинизирующих данных по NCS.Считается, что GBS, которому часто предшествует легкое вирусное или диарейное заболевание, связан с антигенной молекулярной мимикрией белков, обнаруженных на аксонах нервов или миелиновой оболочке. Цитоальбуминологическая диссоциация (повышенный уровень белка с нормальными лейкоцитами) в спинномозговой жидкости (CSF) подтверждает диагноз GBS, но может отсутствовать на ранних этапах течения заболевания. В то время как различные расстройства могут имитировать СГБ клинически, меньшее количество состояний вызывает как быстро прогрессирующие сенсомоторные симптомы, так и периферическую демиелинизацию, наблюдаемую на NCS при AIDP.К ним относятся связанная с вирусом иммунодефицита человека (ВИЧ) воспалительная демиелинизирующая полирадикулоневропатия, дифтерийная невропатия, полинейропатия, связанная с ингибиторами иммунных контрольных точек (включая ниволумаб, пембролизумаб и ниволумаб), токсичность гексакарбона или мышьяка и, в редких случаях, атипичные нейропатические случаи лимфопатии. По определению AIDP — это монофазное заболевание с медленным выздоровлением в течение нескольких недель или месяцев. Лечение внутривенным иммуноглобулином (ВВИГ) или плазмаферезом улучшает выздоровление.Рецидив заболевания или клиническое ухудшение более чем через 8 недель после появления симптомов должны побуждать к рассмотрению хронической воспалительной демиелинизирующей полинейропатии (ХВДП).
Ряд состояний вызывает более хронически прогрессирующую демиелинизирующую невропатию. ХВДП обычно вызывает медленно прогрессирующую, относительно симметричную слабость и онемение. Слабость обычно более выражена, чем потеря чувствительности, и затрагивает как проксимальные, так и дистальные мышцы. Как и в случае AIDP, цитоальбуминологическая диссоциация спинномозговой жидкости помогает подтвердить диагноз, хотя и ВИЧ, и ингибиторы иммунных контрольных точек могут вызывать CIDP, связанный с повышенным содержанием белка и лейкоцитов в спинномозговой жидкости.Первоначальное лечение должно состоять из кортикостероидов или ВВИГ; также может быть использован плазмаферез. Если резистентный, можно рассмотреть возможность применения ритуксимаба, циклофосфамида и азатиоприна. Рассмотрите возможность тестирования рефрактерных пациентов на антитела против нейрофасцина; если присутствует, рассмотрите возможность терапии ритуксимабом. Мультифокальная приобретенная демиелинизирующая сенсорная и моторная полинейропатия (MADSAM), вариант CIDP, проявляется асимметричной слабостью и онемением, а также мультифокальной моторной нейропатией (MMN), которая связана с антителами против GM1 и проявляется чисто моторными симптомами, наиболее выраженными в верхние конечности.Некоторые хронические демиелинизирующие нейропатии связаны с сывороточными парапротеинами и часто не поддаются традиционному лечению CIDP (см. Главу 91).
КЛИНИЧЕСКАЯ ОЦЕНКА И ИССЛЕДОВАНИЕ НЕВРОПАТИИ
Оценка и исследование возможной невропатии — одна из наиболее частых клинических проблем, с которыми сталкивается невролог общего профиля. Исследования распространенности невропатии в обществе редки, но предполагают цифру от 2 до 8%, 1 что делает периферическую невропатию не менее распространенной, чем инсульт.Несмотря на такую высокую распространенность невропатии, только небольшая часть пациентов с нейропатиями направляется для подробного обследования, в основном это люди с инвалидизирующим заболеванием или без каких-либо очевидных факторов риска, таких как диабет или алкоголизм.
Логический подход к оценке таких пациентов очень важен и может быть разбит на ряд основных вопросов. Невролог, столкнувшийся с пациентом с невропатией, должен иметь дело буквально с тысячами возможных причин, многие из которых крайне редки, и их можно упростить только путем определения невропатии по другим признакам, которые приводят к избранным немногим из наиболее вероятных диагнозов.Отчасти это процесс распознавания образов, но ему может помочь поэтапный подход. Несколько алгоритмов 2 и обзорных статей 3 были опубликованы, чтобы помочь этому процессу, и здесь был построен типичный алгоритм (рис. 1).
Рисунок 1Алгоритм, показывающий пошаговый подход к оценке и исследованию возможной невропатии. ХВДП — хроническая воспалительная демиелинизирующая полирадикулоневропатия; CMT, Шарко-Мари-Зуб; ЭМГ, электромиография; GBS, синдром Гийена-Барре; HNPP, наследственная невропатия со склонностью к параличам от давления; NCS, исследования нервной проводимости.
Подход, принятый в этой статье, состоит в том, чтобы представить оценку в виде списка часто задаваемых вопросов, которые при правильном решении и ответе могут дать диагностически важную информацию и, следовательно, направить соответствующее управление. Это не является исчерпывающим описанием нейропатии, но является личным взглядом, иллюстрирующим обычно принятый диагностический процесс.
УКАЗЫВАЕТ ЛИ ИСТОРИЯ И ОБСЛЕДОВАНИЕ, ЧТО ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС ЛОКАЛИЗИРОВАН В ПЕРИФЕРИЧЕСКОМ НЕРВЕ?
На этот вопрос обычно легко ответить, но иногда пациенты могут проявлять необычные проявления, и множественные патологии могут затруднить диагностический процесс.Заболевание спинного мозга является одним из наиболее частых вопросов дифференциальной диагностики у пациентов с симптомами нейропатического типа (вставка 1). При наличии сенсорных симптомов с небольшими клиническими признаками классические признаки расстройства нижних мотонейронов могут отсутствовать, а поперечный миелит, миелопатия или другое заболевание центральной нервной системы может маскироваться под невропатию. Вовлечение черепных нервов (например, онемение или слабость лица, глазодвигательные расстройства) при острой воспалительной невропатии помогает исключить поражение спинного мозга с псевдо-нижним паттерном двигательных нейронов, как это может происходить при острых миелопатиях.
Вставка 1
Диагностические ошибки при установлении невропатииРаспространенным сочетанием, особенно у пожилых, является сочетание шейной спондилотической миелопатии и преимущественно сенсорной аксональной нейропатии с поздним началом. В том же контексте спондилотические радикулопатии могут сочетаться с невропатиями ущемления верхних конечностей. В этих обстоятельствах требуется опыт и осторожность для выявления доминирующего патологического процесса, а это не всегда возможно.Определенные невропатии сосуществуют с заболеванием ЦНС, такие как дефицит витамина B12, адреномиелоневропатия, нейроакантоцитоз, спиноцеребеллярные синдромы и многие другие. В этих ситуациях нет замены распознаванию образов и, если это не удается, структурированному подходу, оба из которых имеют больше шансов на успех, чем случайное расследование.
ПОЛНОСТЬЮ ОПИСАНА ПРЕДСТАВЛЕННАЯ ЖАЛОБА?
Удивительно, как часто можно упустить из виду простые, четко различимые черты истории.Это особенно характерно для наследственных невропатий и врожденных синдромов. Смешные ноги, неровная обувь, неуклюжесть в детстве и подростковом возрасте, особенно в спорте и задачах, требующих хорошей координации, — все это важные ключи к болезни, которая может продолжаться намного дольше, чем более очевидные симптомы пациента.
Продолжительность развития симптомов важно определить, и следующие категории используются в качестве общих рекомендаций в кругах невропатии: острая (<4 недель), подострая (1-3 месяца) и хроническая (> 3 месяцев).Поражения васкулита часто представляют собой сверхострые мононевропатии, обычно продолжающиеся в течение 24–72 часов. В некоторых обстоятельствах, таких как ранняя оценка после появления симптомов, это не может быть прояснено при предъявлении диагноза, но становится очевидным позже. Синдром Гийена-Барре (СГБ), например, по определению достигает своего низшего уровня в течение четырех недель после начала, и любое дальнейшее развитие может указывать на рецидив заболевания или переход в хроническую воспалительную демиелинизирующую полирадикулоневропатию (ХВДП), оба из которых потребуют дальнейшего лечения.В анамнезе часто встречаются трудности с отделением остаточного дефицита после острого события от хронического процесса. Временной график помогает ограничить дифференциальный диагноз, особенно для острых и хронических демиелинизирующих синдромов (вставка 2).
Вставка 2
Демиелинизирующие невропатии-
Острый
-
Хроническая токсичность
-
— хроническая воспалительная демиелинизирующая полирадикулоневропатия (ХВДП)
-
— парапротеинемия
-
— токсичность амиодарона
-
— Болезнь Рефсума
-
— Шарко-Мари-Туф (CMT) типов 1, X и AR CMT 1
-
— метахроматическая лейкодистрофия
-
— статины
-
Один часто недооцениваемый аспект сбора анамнеза касается точных деталей места и характера сенсорных симптомов.Подробные отчеты об этом доступны из многих источников. 4 Очаговые симптомы могут дать важные ключи к разгадке отдельных нервных или корневых заболеваний, которые сами по себе могут быть достаточными для постановки точного диагноза, например, парастетической мералгии. Дистальные отмирающие задние аксонопатии имеют очень характерный зависимый от длины паттерн развития симптомов, который обычно является симметричным, поражая стопы, затем руки, затем переднюю часть туловища. Демиелинизирующая невропатия также может иметь зависимый от длины паттерн сенсорной эволюции, потому что в диффузном процессе более длинные волокна имеют более высокую вероятность блокирования.Напротив, мультисегментные паттерны сенсорного вовлечения, включая туловище, предполагают ганглионопатии дорсального корешка, которые могут возникать, например, при невропатии синдрома Шегрена.
Помимо места возникновения, характер сенсорных симптомов необходимо определить из анамнеза, поскольку они часто плохо описываются пациентами и могут быть диагностически полезными. Боль, потеря чувствительности к температуре и вегетативные симптомы — все это признаки избирательного поражения мелких волокон.Негативный сенсорный симптом неустойчивости, который более заметен в темноте или при закрытии глаз, характерен для сенсорной атаксии, вызванной вовлечением крупных волокон. Эти паттерны сенсорного вовлечения не позволяют локализовать поражение даже на периферическом нерве, но они действительно указывают на поражение типа волокна и, следовательно, сужают вероятные причины.
ПОЛУЧИЛ ЛИ Я ДОСТУПНОЕ ПРОШЛОЕ, СЕМЬЮ, ПРОФЕССИОНАЛЬНУЮ ИСТОРИЮ И НАРКОТИКИ?
Очень важно установить, является ли невропатия изолированным заболеванием периферического нерва, или возникает ли она в контексте болезни в другом месте, или других исторических факторов.Важные общие сведения и информация часто упускаются из виду в первом раунде оценки и обнаруживаются только ретроспективно.
Несомненно, важное значение имеют сопутствующие системные заболевания, особенно органная недостаточность, эндокринные нарушения и заболевания соединительной ткани. Всегда следует искать диабет и скрытый диабет. Подробный семейный анамнез часто имеет решающее значение, даже если он отрицательный, при условии, что семья достаточно большая, чтобы быть информативной. Это может включать случайное обследование сопровождающих родственников, даже если оно ограничивается простукиванием подергивания лодыжки или записью скорости моторной проводимости нижних конечностей.
Воздействие токсичных веществ на рабочем месте становится менее заметным фактором риска по мере улучшения промышленной среды. Таким образом, свинец, мышьяк, акриламид и летучие растворители являются редкими причинами невропатии. Однако история наркотиков имеет решающее значение, как по рецепту, так и для отдыха. Список прописанных лекарств, вызывающих невропатию, слишком длинный, чтобы его перечислять, основными виновниками являются амиодарон, фенитоин, статины, многие антибиотики и химиотерапия: если сомневаетесь, поищите его в своем BNF! Злоупотребление наркотиками представляет собой двойной риск: сам наркотик — например, табак (паранеопластический), алкоголь (токсичный), кокаин (васкулитный) — и связанные с поведением последствия, включая инфекцию ВИЧ или гепатита С, а также недостаточность питания.
В рамках этнического разнообразия и глобализации путешествий, наблюдаемых в многорасовой Великобритании, определенные типы невропатии могут быть более заметными в определенных группах. Нет смысла подозревать шотландского горца в проказе, но он, возможно, заразился нейроборрелиозом или вернулся с ним из пешеходной экскурсии по Шварцвальду. Напротив, иммигрант из Индии, проказа является одной из наиболее частых причин невропатии во всем мире. Веганы уязвимы к дефициту питательных веществ; внутрисемейные браки вызывают рецессивные невропатии.
КАКИЕ ОСОБЕННОСТИ ДИАГНОСТИЧЕСКОЙ ПОМОЩИ Я МОГУ ПОЛУЧИТЬ ПРИ ОБСЛЕДОВАНИИ?
Все мы знаем апокрифические истории о том, как нетерпеливый специалист-регистратор оставляет горшок с мочой на подоконнике, чтобы диагностировать порфирию. Однако систематический подход к выявлению специальных диагностических признаков при общем обследовании непростой, и часто требуется повторный визит к пациенту, чтобы найти то, что другие анализы могут вызвать у вас подозрение. Таким образом, пупочные кератомы при болезни Фабри, линии токсичности мышьяка Миса и оранжевые миндалины при болезни Танжера — это лишь небольшая часть редких диагностических возможностей, доступных для хорошо обученных.
Некоторые аспекты исследования периферических нервов более полезны с практической точки зрения. Согласно условию, мы начинаем с черепных нервов. Таким образом, аносмия возникает при болезни Рефсума и дефиците B12; атрофия зрительного нерва, если она не связана со смешанным центральным и периферическим демиелинизирующим заболеванием, может указывать на наследственный синдром. Анизокория и нарушение зрачковых световых рефлексов указывают на парасимпатическое повреждение и могут быть изолированными, как при синдроме Ади, или направлять более тщательный поиск вегетативных поражений в другом месте, как это может происходить при диабетической невропатии или острой дизавтономии, иногда наблюдаемой в спектре GBS.Нарушение подвижности глаз предполагает ботулизм или синдром Миллера-Фишера, слабость лица — частый признак СГБ и потеря чувствительности тройничного нерва при невропатии Шегрена. Паралич нижних черепных нервов типичен для болезни Кеннеди, что наряду с гинекомастией позволит вам поставить точный диагноз у постели больного в случае диффузной двигательной нейронопатии.
Оценка силы мышц обычно проводится с использованием шкалы Совета медицинских исследований, и ничто не заменило ее, несмотря на неудобно широкий диапазон мощности в группе 4.Это не недостаток конструкции шкалы, созданной в 1941 году для оценки тяжелых нервных повреждений, полученных в ходе боевых действий, а приятное напоминание о том, что сегодня мы склонны жаловаться на меньшие вещи, чем наши предшественники. Динамометрия может использоваться для более точных измерений, необходимых для клинических испытаний, или для оценки реакции отдельных групп мышц на лечение, такое как внутривенный иммуноглобулин (IVIg) при мультифокальной моторной невропатии (MMN).
Как бы то ни было, измерение мощности важно для правильного проведения и регистрации, а определение слабых мест имеет решающее значение для диагностики.Широкие знания о периферических нервных территориях и корневых ценностях — это наш неврологический хлеб с маслом. Трудности могут возникнуть, когда множественные мононевропатии сливаются, поскольку их трудно отделить от полинейропатий, а также при обследовании сложных поражений плечевого и поясничного сплетений. В таких ситуациях часто требуется электрофизиологическая помощь. Мнение студента-медика о том, что слабость при полинейропатии неизменно дистальна, также редко подтверждается в современной практике. Это может иметь место при аксонопатиях, зависящих от длины, таких как Шарко-Мари-Туф 2 (CMT 2) или метаболических невропатиях.Демиелинизирующая нейропатия, такая как GBS и CIDP, часто характеризуется проксимальной доминантной слабостью, так как блокировка проводимости часто влияет на несколько корней и может даже вызывать «псевдопирамидный» паттерн слабости.
Отличительным признаком обследования невропатии является выявление сухожильных рефлексов. Утрата очагового рефлекса с сохранением на других участках имеет очевидные последствия. Утрата дистального рефлекса, проявляющаяся отсутствием рывков в голеностопном суставе, но сохранением рефлексов в другом месте, очень характерна для аксонопатий, зависящих от длины.При приобретенных демиелинизирующих невропатиях потеря рефлекса обычно носит генерализованный характер, как и при CMT 1.
К сенсорному исследованию лучше всего подходят методы тестирования, которые поддерживают функцию крупных волокон (чувство вибрации и проприоцепция) и мелких волокон (укол, боль и температура), в сочетании с учетом как фокальных, так и зависящих от длины особенностей, поскольку это может обеспечить ключевые ключи к вероятной причине. К сенсорному обследованию следует подходить с четкой диагностической целью и руководствоваться знанием основных кожных нервов и паттернов корней, в противном случае оно, вероятно, будет неблагоразумно осмотрительно.
ЯВЛЯЕТСЯ ФОКУСНЫМ, МУЛЬТИФОКАЛЬНЫМ ИЛИ ОБОБЩЕННЫМ НЕВРОПАТИИ?
Характер распределения поражения периферических нервов очень помогает в постановке диагноза. Таким образом, мононевропатии, особенно в месте защемления, часто являются изолированным явлением, возможно, связанным с беременностью, заболеванием щитовидной железы или профессией, но, что важно, также могут возникать как признаки более общего расстройства, такого как наследственная невропатия со склонностью к параличам от давления (HNPP). или амилоидоз.Мононевропатии, возникающие вне участков защемления, более важно исследовать полностью, особенно при подозрении на васкулит, так как это требует тщательной оценки для лечения. Если картина предполагает поражение одного нерва или сплетения в необычном месте компрессии или инвазии, например, поражение лучевого нерва, сдавленное на стуле у пациента после ночного переедания, или инвазия плечевого сплетения со злокачественным новообразованием груди, это явно важно обнаружить. Список возможных причин фокальных или мультифокальных невропатий значительно сокращен по сравнению с генерализованными невропатиями (вставка 3).
Вставка 3
Фокальные и мультифокальные невропатии-
Невропатия защемления — например, синдром плодолистного канала (CTS), локтевой нерв в локте, общий малоберцовый нерв над головкой малоберцовой кости
-
Микседема, акромегалия
-
Амилоид
-
Диабет
-
Наследственная невропатия со склонностью к параличам от давления (HNPP A)
-
Васкулит
-
Мультифокальная моторная нейропатия
Другой вопрос — определить, поражает ли нейропатия верхние или нижние конечности преимущественно.Большинство аксонопатий, зависящих от длины, начинается в ногах, но иногда унаследованные невропатии и нейронопатии в некоторых семьях начинаются с рук. При наследственной амилоидной невропатии руки часто поражаются рано. При приобретенной демиелинизирующей невропатии руки могут быть поражены в большей степени, чем можно было бы ожидать, исходя из степени поражения ног.
КАКОВА ОТНОСИТЕЛЬНАЯ СТЕПЕНЬ УЧАСТИЯ ДВИГАТЕЛЬНОГО И СЕНСОРНОГО НЕРВА?
Очевидно, что некоторые синдромы нейропатии являются чисто моторными, например мультифокальная моторная нейропатия с блоком проводимости (MMNCB), тогда как другие являются чисто сенсорными, например, подострая сенсорная нейронопатия (SSN), вызванная паранеопластическими или другими аутоиммунными ганглионопатиями дорсальных корешков (вставка 4).Однако клиническая жизнь редко бывает такой простой, и большинство невропатий смешанные, если не симптоматически, то, по крайней мере, при клиническом или электрофизиологическом обследовании. Даже при MMNCB некоторые очень незначительные сенсорные симптомы или признаки (включая электрофизиологические) на территориях с двигательным поражением иногда очевидны и не должны исключать диагноз, хотя могут побудить вас рассмотреть тесно связанный синдром, мультифокальную приобретенную демиелинизирующую сенсорную и моторную невропатию (MADSAM, Синдром Льюиса-Самнера).Напротив, сенсорное вовлечение никогда не должно иметь место при болезни двигательного нурона (БДН) и может вызвать серьезные сомнения в этом диагнозе. Точно так же двигательное вовлечение никогда не должно происходить при чистой ганглионопатии задних корешков; тем не менее, невропатия, связанная с антителами против Hu, не является столь единообразной для SSN, как утверждают учебники, в этой группе пациентов часто можно обнаружить двигательные нарушения. 5 Таким образом, этот вопрос предназначен в качестве полезного руководства для диагностики, а не неизменного правила.
ЯВЛЯЕТСЯ ЗНАЧИТЕЛЬНЫМ УЧАСТИЕ В МАЛЫХ ВОЛОКНАХ И АВТОНОМНОСТИ?
Вегетативные особенности, включая поражение зрачков, потовых желез, сердечно-сосудистой системы и желудочно-кишечного тракта, являются особенностями диабетической и амилоидной невропатии и иногда могут быть заметными при СГБ (вставка 5). Это требует тщательного сбора анамнеза для выявления симптомов непереносимости света, постуральной гипотензии, ночной диареи, нарушения потоотделения и дисфункции мочевого пузыря. Обследование может включать в себя тщательный анализ световых реакций зрачка, измерение артериального давления в положении лежа и стоя, а также оценку синусовой аритмии с измерением ЭКГ во время глубокого дыхания.
Вставка 5
Мелкие волокна и вегетативные невропатииЯВЛЯЕТСЯ НЕВРОПАТИЯ АКСОНАЛЬНОЙ ИЛИ ДЕМИЛИНИРОВАННОЙ НА КЛИНИЧЕСКИХ УСЛОВИЯХ?
Это не может быть определено клинически с какой-либо степенью точности и требует нейрофизиологии с измерением скорости проводимости в нескольких нервах, оценкой блокады проводимости, измерением сенсорных потенциалов действия и измерением латентности дистального отдела и латентности зубца F, как описано ниже.
Однако есть некоторые клинические подсказки, которые могут быть полезны. Широко распространенная потеря рефлексов, в том числе в группах мышц, которые не являются особенно слабыми или истощенными, в большей степени является признаком демиелинизации. Напротив, избирательная потеря толчков в голеностопном суставе при дистальном истощении и слабости более типична для аксонопатии, особенно если она сопровождается распределением сенсорной потери в чулках.
Таким образом, полная оценка пациента с нейропатией может охарактеризовать клинический синдром как хроническую многоочаговую, преимущественно моторную, демиелинизирующую нейропатию.Этот тип нейропатии будет иметь ограниченный дифференциальный диагноз и будет направлен на исследования, направленные на дифференциацию CIDP от парапротеинемии и токсичности амиодарона.
Самая большая и самая сложная группа — это смешанная моторная сенсорная нейропатия с характером, предполагающим умирающую заднюю аксонопатию и подтверждением аксональной невропатии по электрофизиологии (вставка 6). Здесь первостепенное значение имеет тщательный сбор анамнеза с подробным исследованием других системных заболеваний и подробное генеалогическое древо.Построение генеалогического древа может выявить детали забытых родственников со стигматами наследственной невропатии, например, с высокими сводчатыми стопами.
Вставка 6
Хроническая аксональная невропатияКАКОЙ ДОПОЛНИТЕЛЬНОЙ ИНФОРМАЦИИ Я МОГУ ОЖИДАТЬ ОТ НЕЙРОФИЗИОЛОГИЧЕСКОЙ ОЦЕНКИ?
Подробное рассмотрение этого вопроса выходит за рамки нашего введения, но стоит отметить несколько моментов.Нейрофизиологическое обследование не может проводиться изолированно от клинической оценки, оно должно основываться на исторических и клинических данных. Многие клинические электрофизиологи собирают анамнез и проводят обследование перед электрофизиологическими исследованиями, чтобы определить место проведения и методы тестирования, но это по необходимости часто довольно ограничено. Поэтому для клинициста чрезвычайно полезно выделить наиболее важные вопросы, которые задает лаборатория, в идеале путем обсуждения или, альтернативно, в форме запроса.В последнем случае невролог должен кратко указать информацию, необходимую для нейрофизиологической оценки пациента, но не должен указывать отдельные тесты, необходимые для этого!
Сенсорные исследования часто являются первым подходом к определению наличия невропатии. Если объективная потеря чувствительности, затрагивающая крупные волокна, клинически очевидна, наличие нормально сохраненных потенциалов действия сенсорных нервов (SNAP) указывает на то, что причина не находится дистальнее ганглия дорзального корешка, и предполагает центральное или корневое заболевание.Очаговые защемления часто можно легко выявить путем параллельного сравнения при обследовании сенсорных нервов. Зависимые от длины невропатии крупных волокон характеризуются исчезновением SNAP дистальных отделов ног (то есть поверхностных малоберцовых и икроножных нервов) перед SNAP верхних конечностей. Исследования сенсорных нервов редко бывают полностью нормальными при невропатиях с сенсорными симптомами, за исключением сложной категории поздних болезненных невропатий мелких волокон, например, при беспокойных ногах.
Самый простой и наиболее часто задаваемый вопрос исследований моторной проводимости (хотя и не обязательно самый простой) — есть ли доказательства демиелинизации.Протоколы, определяющие согласованные критерии демиелинизации, были подготовлены для пациентов с подозрением на наличие GBS 6 или CIDP 7 , и они полезны. Установление того, что у пациента явно демиелинизирующая невропатия, имеет решающее значение для последующей последовательности исследований. Интерпретация модели демиелинизации — это довольно специализированная область, которую лучше всего оставить на усмотрение вашего нейрофизиолога, но она очень полезна. Таким образом, равномерная демиелинизация скорее способствует наследственной невропатии, тогда как неоднородные результаты с различиями между нервами и сегментами внутри нерва больше в пользу приобретенного синдрома. 8, 9 Латентность зубца F полезна на ранних стадиях СГБ для оценки замедления проксимальной проводимости и действительно может быть единственной аномалией на ранней стадии заболевания. 10 Некоторые синдромы имеют свои индивидуальные особенности; таким образом, демиелинизирующая нейропатия, связанная с иммуноглобулином IgM антителами к миелин-ассоциированному гликопротеину (MAG), характерно связана с длительными латентными дистальными моторными движениями.
Другой распространенный клинический вопрос, в котором решающее значение имеет электрофизиолог, — определить, является ли нейропатия симметричной и сливной, присутствуют ли фокальные или мультифокальные особенности.В случае асимметричной нейропатии, поражающей верхние конечности, есть ли доказательства блокады проводимости, позволяющие предположить диагноз мультифокальной моторной невропатии в отличие от БДН? 11 Такие исследования должны включать оценку проксимального блока путем стимуляции в точке Эрба, что не может быть выполнено рутинно. Мультифокальный паттерн поражения, наблюдаемый при васкулитной невропатии, часто очень полезно отделить от множественных защемлений или поражений корней. При синдроме Миллера-Фишера или бульбо-спинальной нейронопатии главный вопрос может заключаться в том, уменьшились ли потенциалы сенсорного действия в размерах.
КАКИЕ СКРИНИНГОВЫЕ ИСПЫТАНИЯ Я ДОЛЖЕН ПРОВЕСТИ?
Вставка 7 показывает разумный первый экран для нового проявления аксональной невропатии без очевидной причины.
Вставка 7
Первый раунд отборочных испытанийЕсли из вышеперечисленного не было найдено никакой причины и в прошлой истории болезни нет клинических признаков, было бы разумно углубиться в семейный анамнез и попытаться, если возможно, обследовать родственников.На этом этапе обычно проводятся дальнейшие тесты в соответствии с клиническими признаками, которые предполагают более необычные или эзотерические причины невропатии. Примером может служить измерение антител против Hu для выявления скрытой грудной клетки или гинекологических злокачественных новообразований. 5 Невозможно перечислить все исследования, которые могут быть полезны, и следует подчеркнуть, что они должны быть нацелены на клиническую ситуацию. После этих тестов второй линии самые последние исследования показывают, что по крайней мере у 15% пациентов не может быть обнаружена причина. 12 Исследования этой группы предполагают, что некоторые из них могут иметь иммунное происхождение, а другие — нераспознанные генетические невропатии. Основной клинической проблемой у пациентов, состояние которых ухудшается, является наличие васкулита, ограниченного периферическими нервами. Такой диагноз может быть поставлен только на основании биопсии нерва, но результат биопсии при хронической идиопатической симметричной невропатии очень мал. Если невропатия возникла недавно и прогрессирует, или есть предположение о системном заболевании или повышенной скорости оседания эритроцитов (СОЭ), следует рассмотреть возможность проведения биопсии.В противном случае целесообразно продолжить наблюдение. Антитела против Hu имеют важное значение, поскольку их присутствие тесно связано с паранеопластической невропатией 13 и нераскрытым злокачественным новообразованием, обычно легким или яичником.
Анализ ЦСЖ
Анализ спинномозговой жидкости (ЦСЖ) полезен для различения иммуно-опосредованных невропатий, таких как ХВДП, или хронических иммуно-опосредованных аксональных невропатий, при которых белок ЦСЖ часто значительно повышен. Наличие значительного плеоцитоза при подострой невропатии должно вызвать подозрение на другие острые воспалительные невропатии, такие как боррелия или саркоидоз.
Специальные испытания
К счастью, в последние годы генетические тесты на невропатию быстро разрослись и решили многие диагностические головоломки. Район подробно описан Рейли и Ханной. 14 Другая область, где резко возросло количество тестов, — это дисиммунные синдромы, особенно тестирование на антитела. Обязательно диагностировать паранеопластические синдромы путем тестирования антител у пациентов с подострыми сенсорными нейронопатиями, и на практике сеть часто бывает шире, чем это клиническое показание.Для конкретных показаний также доступен широкий спектр других тестов на антинейрональные антитела.
Анти-ганглиозидные антитела ищутся у пациентов с подозрением на MMN. Антитела IgM к GM1 присутствуют примерно у 50% пациентов с этим синдромом, поэтому их отсутствие не исключает диагноза, но их наличие полезно с диагностической точки зрения.
Anti-GQ1b IgG-антитела являются высоконадежным маркером синдрома Миллера-Фишера, где они неизменно присутствуют в сыворотке крови острой фазы.В моторном аксональном варианте GBS также часто обнаруживаются антитела против GM1 и GD1a, которые присутствуют более чем в 50% случаев.
При синдромах хронической нейропатии, особенно связанных с парапротеинами IgM, ищут антитела к MAG, сульфатиду и ганглиозиду GD1b, поскольку они определяют довольно дискретные клинические фенотипы. Ни при одном из этих последних синдромов присутствие антител не предсказывает хороший ответ на лечение.
Когда мне следует делать биопсию нерва?
Биопсия сенсорного нерва стала использоваться в качестве диагностической процедуры для исследования некоторых типов невропатии за последние 30 лет. 15 Появление генетических тестов на многие невропатии уменьшило потребность в биопсии, но она остается основным методом постановки диагноза васкулитной невропатии, когда гистология недоступна из других источников. Комбинированная биопсия нерва и мышцы обычно рекомендуется в случаях подозрения на васкулит, чтобы увеличить диагностическую ценность. 16 Эти биопсии обычно затрагивают поверхностные малоберцовые или промежуточные латеральные нервы, которые позволяют получить доступ к мышце в пределах одного разреза.Поскольку большинство васкулитов возникает в эпиневрии, обычно предпочтительна биопсия на всю толщину. 17 Ценность биопсии нерва была рассмотрена в проспективном исследовании, проведенном в больнице Гая. В этой последовательной серии из 50 биопсий икроножного нерва лечение было изменено в 60% случаев, а диагноз — в 14% случаев. Считалось, что такая биопсия вызывает стойкую боль в месте биопсии у 33% пациентов. Это последнее открытие подчеркивает необходимость ограничить биопсию тщательно отобранными случаями и в идеале зарезервировать для центров, обладающих опытом в соответствующих методах.
Биопсия нервов может быть полезна в диагностике ХВДП, когда диагностикой может быть гистологическая идентификация воспалительных клеток или явной макрофагальной демиелинизации с помощью электронной микроскопии. К сожалению, многие пациенты с ХВДП не имеют воспалительных клеток в чувствительных нервах, и биопсия, вероятно, не требуется пациентам с типичной электрофизиологией и клиническими особенностями ХВДП. 18 Результат биопсии при хронической аксональной невропатии очень мал и, вероятно, не оправдан, если васкулит маловероятен.Пациенты с аксональной нейропатией, моделирующей аксональную форму CMT, иногда могут иметь амилоид, особенно при наличии мелких волокон. Диагноз у этих пациентов часто может быть установлен путем поиска мутаций транстиретина у большинства пациентов без использования биопсии, но если генетика не помогает, биопсия кажется разумной.
ССЫЛКИ
- ↵
Martyn CN , Hughes RA. Эпидемиология периферической невропатии.J Neurol Neurosurg Psychiatry, 1997; 62: 310–18.
- ↵
Schaumburg HH , Berger AR, Thomas PK, Заболевания периферического нерва . Филадельфия: Ф. А. Дэвис, 1992: 26–32.
- ↵
Хьюз Р . Периферическая невропатия. BMJ2002; 324: 466–9.
- ↵
Mendell JR , и др. . Диагностика и лечение заболеваний периферических нервов.В: Современная неврология, серия . Оксфорд: Издательство Оксфордского университета. 2001: 10–29.
- ↵
Hughes RAC , Antoine JC, Honnorat J, и др. . Паранеопластическая периферическая нейропатия, связанная с антителами против Hu. Клинико-электрофизиологическое исследование 20 пациентов. Brain2002; 125: 166–75.
- ↵
Эсбери AK , Корнблат DR. Оценка современных диагностических критериев синдрома Гийена-Барре.Ann Neurol1990; 27 (доп.): S21–4.
- ↵
Специальный подкомитет Целевой группы по СПИДу Американской академии неврологии . Критерии исследования для диагностики хронической воспалительной демиелинизирующей полирадикулоневропатии (ХВДП). Неврология, 1991; 41: 617–18.
- ↵
Fross RD , Daube JR. Невропатия при синдроме Миллера-Фишера: клинические и электрофизиологические данные.Неврология 1987; 37: 1493–8.
- ↵
Олни Р.К. , Аминофф MJ, So YT. Клинические и электродиагностические особенности Х-сцепленной рецессивной бульбоспинальной нейронопатии. Неврология, 1991; 4: 823–8.
- ↵
Kiers L , и др. . Количественные исследования F-ответов при синдроме Гийена-Барре и хронической воспалительной демиелинизирующей полинейропатии. Электроэнцефалография и клиническая нейрофизиология, 1994; 93: 255–64.
- ↵
Chaudhary V , Corse AM, Cornblath DR, и др. . Мультифокальная моторная нейропатия: особенности электродиагностики. Мышцы и нервы, 1994; 17: 198–205.
- ↵
Notermans NC , Wokke JH, Fransen H, и др. . Хроническая идиопатическая полинейропатия, проявляющаяся в среднем или пожилом возрасте: клиническое и электрофизиологическое исследование 75 пациентов. J Neurol Neurosurg Psychiatry, 1993; 56: 1066–71.
- ↵
Graus F , Bonaventura I, Uchuya M, и др. . Паранеопластическая сенсорная нейропатия, ассоциированная с индолентным анти-Hu. Неврология, 1994; 44: 2258–61.
- ↵
Рейли MM , Ханна MG. Генетическое нервно-мышечное заболевание. J Neurol Neurosurg Psychiatry, 2002; 73 (приложение II): ii12–21.
- ↵
Dyck PJ , et al. Методы фасцикулярной биопсии периферического нерва человека для электрофизиологического и гистологического исследования. Mayo Clin Proc, 1966; 41: 778.
- ↵
Саид G , Lacroix-Ciaudo C, Fujimura H, и др. . Периферическая невропатия некротического артериита: клинико-патологическое исследование. Энн Нейрол 1988; 23: 461–5.
- ↵
Саид G . Значение биопсии нерва? Lancet2001; 357: 1220–21.
- ↵
Molenaar DS , Вермёлен М., де Хаан Р. Диагностическое значение биопсии икроножного нерва при хронической воспалительной демиелинизирующей полинейропатии. J Neurol Neurosurg Psychiatry 1998; 64: 84–9.
Хроническая воспалительная аксональная полинейропатия | Журнал неврологии, нейрохирургии и психиатрии
Введение
Аксональный синдром Гийена-Барре (СГБ) хорошо известен как отдельная сущность.1 «Хроническая воспалительная демиелинизирующая полинейропатия аксонов» (ХВДП) редко сообщалась в 1990-е гг. 2 Однако существовали некоторые сомнения относительно существования такой формы, «аксональной ХВДП» или хронической воспалительной аксональной полинейропатии (ХВДП). В этой статье мы сообщаем о нашем опыте 33 случаев «иммунотерапевтической хронической аксональной полинейропатии (IR-CAP)» в Университете Алабамы в Бирмингеме (UAB) и представляем доказательства биопсии нерва воспалительной аксональной нейропатии у этого субъекта.Мы думаем, что эта сущность представляет собой CIAP, и, наконец, представляем предлагаемые диагностические критерии CIAP.
Материалы и методы
Диагноз IR-CAP был поставлен при соблюдении всех трех следующих обязательных критериев: (1) приобретенная, хроническая прогрессирующая или рецидивирующая симметричная или асимметричная полинейропатия с продолжительностью прогрессирования> 2 месяцев; (2) электрофизиологические доказательства аксональной невропатии по крайней мере двух нервов без каких-либо доказательств «строгих критериев демиелинизации»; и (3) определенная реакция на иммунотерапию.
Электрофизиологический критерий аксональной нейропатии определяется как исследование аномальной нервной проводимости (NCS) без каких-либо электрофизиологических критериев демиелинизации в любых моторных или сенсорных NCS в блоке 1.3–5.
Вставка 1Электрофизиологические критерии демиелинизации *
Проводимость по двигательному нерву
-
Скорость нервной проводимости (NCV): <40% от нормального среднего
-
Терминальная (дистальная моторная) латентность:> 150% от нормального среднего
-
Латентность F-волны:> 150% от нормального среднего
-
Блок проведения:> 50% уменьшение амплитуды комбинированного потенциала действия мышц (CMAP) (общий или отрицательный пик)
-
Дисперсия: дистальная и проксимальная дисперсия на отрицательный пик или общая продолжительность CMAP:
-
Дистальный:> 8 мс для длительности отрицательного пика или 35 мс для общей длительности
-
Проксимальный:> 30% для длительности отрицательного пика или> 33% для общей сравниваемой длительности с дистальным CMAP.
-
Сенсорная нервная проводимость
-
Отрицательный пик NCV: <40% от нормального среднего
-
Дисперсия: продолжительность сложного потенциала нервного действия:> 2,8 мс с записью поверхностного электрода или> 4,8 мс с близким запись нервной иглы
Для оценки степени инвалидности мы использовали балльную систему оценки периферической невропатии. Согласно этой системе 0 — нормально, а 20 — максимально отключено.Оценка инвалидности представляет собой общую сумму четырех различных модальностей: две двигательные функции (дистальная и проксимальная) и две сенсорные функции (укол булавкой и прикосновение, вибрация и положение) .6 Улучшение определяется, когда есть объективное улучшение не менее чем на 2 балла. «баллы по инвалидности» в течение 1 года лечения.
Рутинные исследования нервов (NCS) были выполнены с использованием стандартного размещения электродов на поверхности e, как описано ранее. Всем пациентам были выполнены двигательные NCS в срединных, локтевых, малоберцовых и большеберцовых нервах, сенсорные NCS в срединных, локтевых и икроножных нервах и смешанные NCS в срединных и локтевых нервах.ЭМГ с монополярной иглой была проведена у всех пациентов в мышцах, выбранных EMGer. У одного пациента была выполнена сенсорная NCS иглы на нервах икроножного нерва.
У 32 пациентов ЦСЖ был получен с помощью люмбальной пункции с диагностической целью. Все пациенты прошли базовое обследование периферической нейропатии, которое включало тироидный и ревматологический профили, витамин B 12 и фолиевую кислоту, гемоглобин A1C, скорость оседания и иммуноэлектрофорез сывороточного белка с помощью иммунофиксации.
Биопсия икроножного нерва была выполнена стандартным методом за боковой лодыжкой и исследована на замороженных, парафиновых и полутонких срезах у 31 пациента.7 Дегенерация аксонов определяется камерами переваривания миелина на замороженных срезах. Воспалительные клетки оценивают на замороженных и парафиновых срезах. Демиелинизацию оценивают на полутонком срезе.
Клинические и лабораторные характеристики IR-CAP сравнивались с ранее опубликованными характеристиками CIDP8.
Результаты
Диагноз
За 25-летний период с 1990 по 2014 гг. Выявлено 39 пациентов с хронической аксональной полинейропатией, получавших иммунотерапию.Среди 39 пациентов мы выявили 33 пациента с IR-CAP, у которых соблюдаются все критерии 1, 2 и 3. Шесть пациентов были исключены из-за отсутствия ответа на иммунотерапию в течение 3–9 лет. Среди этих шести пациентов у одного наблюдалось прогрессирование в течение 4-летнего периода даже при продолжении лечения ежемесячным ВВИГ вместе с различными комбинациями циклорфосфамида, микофенолят монфетила и циклоспорина. В других пяти случаях их неврологический статус стабилизировался в основном с помощью ВВИГ и азатиоприна более 0.5–6 лет.
Клинические особенности IR-CAP
Пять пациентов имели предыдущий эпизод невропатии до нашей оценки (таблица 1). У одного был диагностирован аксональный СГБ за 4 года до первого рецидива невропатии. У одного было два эпизода двоения в глазах и невропатии за 7-летний период.9 У одного был один эпизод невропатии, который невропатолог, направивший его, резко улучшил после приема стероидов. Два случая имели предыдущий эпизод спонтанно улучшившейся невропатии. Предыдущее событие или инфекция за 4–8 недель до начала заболевания наблюдались в восьми случаях: гриппоподобный эпизод в четырех, диарея в одном, прививка от гриппа в одном, операция по удалению грыжи в одном и опоясывающий лишай в одном.Симметричная моторно-сенсорная нейропатия была наиболее частой формой нейропатии в 26 случаях. Только в одном случае была симметричная сенсорная нейропатия. В 22 случаях проксимальные и дистальные мышцы конечностей были вовлечены в невропатию, тогда как дистальные мышцы только в восьми случаях и проксимальные мышцы в трех случаях. Нарушения чувствительности были обнаружены в 25 случаях в дистальной области конечностей и в 7 случаях в проксимальной части конечностей. Астреогнозис присутствовал в двух случаях. Атаксическая походка наблюдалась в трех случаях. Атрофия наблюдалась в руках у двух и в трех случаях в ногах.В шести случаях черепные нервы были поражены: полная офтальмоплегия в одном, частичная офтальмоплегия с онемением лица в одном, анискория в одном, диплегия лица в одном, затруднение глотания в одном и затруднение дыхания в двух. За исключением одного случая с повышенными коленными рефлексами, во всех случаях рефлексы были снижены или отсутствовали в одном из четырех протестированных рефлексов. Во всяком случае, фасцикуляции не наблюдалось.
Таблица 1Сравнение клинических и лабораторных характеристик хронической аксональной полинейропатии (IR-CAP) с ответом на иммунотерапию и хронической воспалительной демиелинизирующей полинейропатии (CIDP)
Лабораторные данные
Все стандартные обследования периферической нейропатии были отрицательными, за исключением парапротеинемии в пяти случаях, и низкий иммуноглобулин в 1.Панель нейропатии аутоантител в сыворотке, включая GM1, была проверена в 12 случаях. В одном случае с симметричной моторно-сенсорной нейропатией были положительные антитела к MAG без какой-либо моноклональной гаммопатии в начале и отрицательные антитела к MAG через 3 года. В одном случае, имитирующем хроническую атаксическую нейропатию, офтальмоплегию, синдром агглютинации М-белков с дисиалозил-антителами (CANOMAD) имел моносиалозильные антитела.8 9 Таким образом, ассоциированные заболевания были обнаружены в шести случаях: моноклональная гаммопатия в трех, биклональная гаммопатия в одном, гипогаммоглобулинопатия в одном и множественная миелома один.
Самым заметным лабораторным отклонением от нормы был повышенный уровень белка в спинномозговой жидкости (> 55 мг / дл) в 25 (78%) из 32 исследованных случаев. Ни в одном из случаев увеличения клеток не наблюдалось. Уровень IgG был повышен в четырех случаях.
Электрофизиологические данные
NCS был аномальным во всех случаях. Во всех случаях была аксональная нейропатия. Ни один из случаев не соответствовал критериям демиелинизации согласно критериям UAB или Руководству Объединенной целевой группы Европейской федерации неврологических обществ (EFNS) / Общества периферических нервов (PNS).10 Наиболее выраженным паттерном нейропатии при NCS была смешанная моторная и сенсорная нейропатия в 28 случаях. Три случая имели паттерн моторной нейропатии (чистая моторная аномалия NCS). Паттерн сенсорной нейронопатии, указывающий на сенсорную ганглионопатию, наблюдался в одном случае. В одном случае наблюдалась сенсорная нейропатия.
Двигатель NCS был ненормальным в 31 случае. Наиболее частым нарушением проводимости двигательного нерва было отсутствие или низкая амплитуда CMAP в 51 (39%) из 132 тестов. Медленная NCV наблюдалась в 48 (36%) тестах, в то время как длительная волна F и терминальная латентность наблюдались в 49 (37%) и 42 (32%) тестах в каждом.Зубец F отсутствовал в 17/121 (14%) тестах. Процент увеличения выше средних значений F-волн был ниже 22% во всех четырех нервах.
Сенсорные NCS срединного, локтевого и икроножного нервов были аномальными в 28 случаях. Наиболее частым отклонением от нормы была медленная NCV в 62 (63% из 99 тестов, за которыми следовала низкая амплитуда сенсорного сложного нервного действия (CNAP) в 48 (48%) из 99 тестов и отсутствие потенциала в 40 (40%) из 99 тестов). CNAP был наиболее распространен в икроножном нерве (23 случая), в отличие от срединного (5 случаев) и локтевого (5 случаев) нервов.«Сохранение икроножной мышцы» (аномальная медианная или локтевая и нормальная проводимость икроножных чувствительных нервов) наблюдалась в двух случаях.
Смешанные NCS сегментов предплечья и плеча срединного и локтевого нервов были аномальными в 25 случаях. Наиболее частой аномалией была низкая амплитуда смешанного CNAP в 15 (23%) из 66 тестов, за которым следовала медленная смешанная NCV в 9 (14%) из 66 тестов и отсутствие смешанного CNAP в 4 (6%) из 66 тестов. Проведение сенсорного нерва в подошвенном нерве с помощью иглы около нерва (NNN) показало отсутствие потенциала в двух случаях и нормальное обнаружение в одном случае.Проведение нерва по игле нерва в икроножном нерве в одном случае показало «аксональную невропатию» 5.
Фибрилляция и положительные острые волны были обнаружены в дистальных мышцах в 26 (89%) из 29 протестированных случаев, в проксимальных мышцах в 12 (86%) из 14 протестированных случаев и в пояснично-крестцовых параспинальных мышцах в 11 (85%) из 13 случаев. проверенные кейсы.
МРТ корней и сплетений
У одного пациента был «рождественский световой узор» в пояснично-крестцовой области и высокое содержание белка в спинномозговой жидкости. Она полностью выздоровела после длительного лечения стероидами.
Результаты биопсии нерва
Биопсия икроножного нерва в 31 случае показала нормальные результаты в одном случае. Наиболее заметной находкой была воспалительная нейропатия в 14 (45%) случаях с дегенерацией аксонов в 11 (36%) случаях. Воспалительные клетки были обнаружены в периваскулярных областях эпиневрии (рисунок 1). Следующим наиболее заметным открытием была аксональная нейропатия, продемонстрированная камерами переваривания миелина в модифицированном трихромном окрашивании в замороженных срезах в 16 (51%) случаях. В двух случаях при поддразнивании нерва было обнаружено множество миелиновых овоидов, характерных для дегенерации аксонов.
Рисунок 1Результаты биопсии икроножного нерва при хронической воспалительной аксональной полинейропатии. (A) Модифицированное окрашивание трихромом. Замороженный раздел. × 200 Видимая камера переваривания миелина, представляющая активную дегенерацию аксонов. (B) Окрашивание H&E × 200 периваскулярных скоплений воспалительных клеток в эпиневриальном пространстве. (C) Полутонкий разрез. Толуидиновый синий и основное окрашивание фуксином (множественное окрашивание Paragon) × 200 — умеренная потеря аксонов без признаков образования луковицы или тонкого миелинизированного волокна. (D) Дразнящие нервные волокна.Окраска осмиевой кислотой. × 200 Миелиновые овоиды, представляющие дегенерацию аксонов.
Ответ на лечение и результат
Спонтанного улучшения не наблюдалось ни в одном из случаев. Во всех случаях использовалась различная иммунотерапия. Клиническое улучшение было задокументировано в 33 случаях. Максимальное клиническое улучшение было достигнуто при лечении в течение периода от 1 недели до 1 года, в течение 6 месяцев в 90% случаев. Преднизонотерапия была основным лечением в 20 случаях. Азатиоприн был следующим широко используемым иммуносупрессорным препаратом в 15 случаях.Внутривенный иммуноглобулин (ВВИГ) был наиболее часто добавляемым лечением в 16 случаях. Плазмообмен использовался только в двух случаях. Циклоспорин, микофенолятмофетил и метотрексат использовались в качестве дополнительных лекарств в трех случаях. Последующий ответ на лечение от 6 месяцев до 20 лет отмечен в 29 случаях. В 29 случаях улучшенный статус сохранялся с помощью преднизона в 14 случаях, азатиоприна в 14, внутривенного иммуноглобулина в 12 различных комбинациях. Рецидив зарегистрирован в 14 (42%) случаях.
Сравнение IR-CAP и CIDP
Единственное существенное различие (p = 0.0057) между IR-CAP и CIDP представляла собой «чистую моторную невропатию», которая чаще встречается при CIDP. В остальном IR-CAP имел много общего по клиническим, лабораторным и терапевтическим характеристикам CIDP (таблица 1).
Конечные (дистальные моторные) латентные периоды и моторные NCV сравнивались между IR-CAP (CIAP) (рисунок 2). Средняя терминальная латентность четырех двигательных нервов на 21–33% выше среднего значения при IR-CAP и на 109–135% выше среднего значения при CIDP, за пределами «маркера демиелинизации» (> 50% от среднего среднего значения). Средние NCV в четырех нервах составляют 0–23% снижение нормального среднего при IR-CAP и 33–38% снижение нормального среднего при CIDP, рядом с маркерами демиелинизации (> 40% ниже среднего среднего) при CIDP.Таким образом, сравнение терминальных латентных периодов и NCS ясно показало, что аномальная нервная проводимость при IR-CAP является «аксональной» по сравнению с «демиелинизацией» при CIDP.
Рисунок 2Сравнение терминальной (дистальной моторной) латентности и скорости нервной проводимости между хронической воспалительной аксональной полинейропатией (CIAP) и хронической воспалительной демиелинизирующей полинейропатией (CIDP). Терминальная латентность: средняя терминальная латентность срединного, локтевого, малоберцового и большеберцового нервов. 0% представляет собой нормальное (N) среднее значение. > 50% (красная линия, на 50% больше нормы, представляет демиелинизацию).Скорость нервной проводимости: средняя скорость нервной проводимости в срединных, локтевых, малоберцовых и большеберцовых нервах. 100% представляет собой нормальное (N) среднее значение. <60% (красная линия; на 40% ниже нормы) представляет демиелинизацию. D дистальный (локтевый – лучезапястный) сегмент. P - проксимальный (подмышечно-локтевой) сегмент.
По определению, в IR-CAP не было случаев блокировки проводимости или рассеивания. При ХВДП блокада проводимости наблюдалась в 19–32% тестов по четырем нервам и временная дисперсия в 18–36% тестов по четырем нервам.Средняя латентность F-волны была ниже 150% (маркер демиелинизации) как при IR-CAP, так и при CIDP. Среднее увеличение -F-волны за пределы нормы составило 29–37% при CIDP и 18–22% при IR-CAP. Однако отсутствие зубца F было более распространенным (20% тестов) при CIDP по сравнению с 14% тестов при IR-CAP.
Обсуждение
Хроиновая воспалительная аксональная полинейропатия
Наше исследование показало, что существует хроническая аксональная полинейропатия, отвечающая на иммунотерапию. Из-за отсутствия лучшего термина мы назвали эту организацию «IR-CAP» для анализа данных.Мы полагаем, что это заболевание носит воспалительный характер, учитывая наличие «воспалительных клеток», что является важным обнаружением при биопсии икроножного нерва. В 45% биопсий икроножного нерва были обнаружены воспалительные клетки эпиневрии. Аксональная нейропатия была еще одной заметной особенностью биопсии нерва, которая наблюдалась в 51% случаев биопсии икроножного нерва. На основании этих наблюдений мы полагаем, что IR-CAP лучше всего описать как CIAP.
Клиническая разница между CIAP и CIDP
Клинические профили пациентов с CIAP были очень похожи на профили пациентов с CIDP.8 Клинические характеристики CIDP (предыдущий эпизод, высокая частота рецидивов и более низкая частота предшествующей инфекции, поражение черепных нервов, дыхательная недостаточность и спонтанное улучшение) также наблюдаются в CIAP.11 12 Рецидив невропатии описывается как характерная черта CIDP от начало и в настоящее время считается лучшим клиническим показателем, указывающим на CIDP.12 В нашем исследовании у нас было пять пациентов с нейропатией в анамнезе. Таким образом, мы считаем, что эти данные сильно указывают на CIAP, хотя это случается редко.В нашей серии одно из этих трех (предыдущий анамнез, предшествующее событие и поражение черепных нервов) наблюдалось у 13 пациентов, и иммунотерапия была эффективной у всех 13 пациентов. Слабость проксимальных мышц сильно указывает на полирадикулопатию и CIDP.13–15 Проксимальная слабость наблюдалась в 76% случаев IR-CAP по сравнению с 67% при CIDP. Однако нужно исключить другие причины, такие как диабет. При диабетической амиотрофии слабость проксимальных мышц является одним из характерных признаков.16 Одно существенное различие отмечено в количестве подтипов моторной невропатии между CIAP и CIDP, которое значительно реже встречается при IR-CAP (p = 0.0057).
Высокий уровень содержания белка в спинномозговой жидкости схож по среднему значению и примерно у двух третей пациентов в обеих группах. Положительные аутоантитела в сыворотке наблюдались в двух случаях IR-CAP. Сообщается, что положительный уровень аутоантител в сыворотке также низкий и при ХВДП.
Терапевтически CIAP похож на CIDP на иммунотерапию. Хотя существует меньше случаев «улучшения до нормы» и больше случаев «отсутствия улучшений» при IR-CAP, что позволяет предположить, что IR-CAP немного более устойчив к иммунотерапии, чем CIDP, статистическая разница несущественна.Таким образом, можно сделать вывод, что ответ на различные виды иммунотерапии у двух субъектов схож.
Электрофизиологические различия между CIAP и CIDP
По диагностическим критериям демиелинизация при CIAP не обнаружена. Сравнение моторных NCV и терминальных латентных периодов ясно показало, что их значения находятся в пределах « аксонального диапазона » критериями UAB, а также совместной рабочей группой EFNS / PNS Guideline.3 10 Таким образом, электрофизиологические данные также подтверждаются дегенерацией аксонов при биопсии нерва. .
Тест NNN-сенсорной нервной проводимости и тест тройной стимуляции (TST), другие сложные тесты для выявления демиелинизации, не проводились систематически у наших пациентов с IR-CAP, чтобы исключить CIDP.17 18 Мы провели только NNN-проводимость в трех случаях IR-CAP, в которых обнаружена аксональная нейропатия.
Воспалительная природа CIAP
Воспалительная природа «аксонального CIDP» подозревалась клинически в опубликованной серии исследований. Однако это не было доказано семью биопсиями нервов в литературе.19–24. Выявлена дегенерация аксонов в пяти клетках, но без воспалительных клеток. Воспалительная природа CIAP была патологически подтверждена в одном случае вскрытия, как описано ниже.25
Самым замечательным открытием в настоящем исследовании является демонстрация воспалительной клеточной и аксональной дегенерации, как наиболее заметных результатов биопсии нерва при IR-CAP. Напротив, биопсия нерва при ХВДП показывает эпиневральные воспалительные клетки в 27–54% нерва, подвергнутого биопсии, и эндоневральные воспалительные клетки в 11–65% нервов, подвергнутых биопсии.7 12 По определению, демиелинизация, основной патологический признак CIDP, не наблюдалась в наших случаях CIAP. Дегенерация аксонов — наиболее частая находка при биопсии нерва, как и ожидалось, с учетом паттерна аксональной нейропатии в NCS.
Воспалительная аксональная нейропатия классически наблюдается при васкулитной нейропатии.7 26 В наших случаях мы исключили васкулитную невропатию с помощью серийных разрезов при биопсии нерва и других клинических и лабораторных признаков.
В нашем обзоре 53 случаев воспалительной аксональной нейропатии при биопсии икроножного нерва в нашей лаборатории гистопатологии мышечных нервов наиболее частыми причинами были иммуноопосредованная нейропатия в 81% случаев, включая васкулит, сахарный диабет и моноклональную гаммапатию как три наиболее распространенных. причины.27 Это причина, по которой васкулитная или диабетическая нейропатия была исключена как свидетельство «воспаления» при биопсии нерва в третьем критерии CIAP.
CIAP по сравнению с аксональным CIDP
Другим возможным альтернативным нозологическим обозначением IR-CAP является аксональный CIDP.2 Мы предпочитаем CIAP, описательный термин, потому что аксональный CIDP предполагает, что «аксональные изменения в CIAP» вторичны по отношению к CIDP. Однако это еще не доказано, хотя клинический профиль и иммунотерапия схожи при IR-CAP и CIDP.Сложный тест, такой как проводимость по сенсорному нерву NNN или TST для исключения демиелинизации, не проводился систематически в случаях IR-CAP.17 18
Обзор 14 случаев CIAP в литературе
Pollard et al подняли вопрос об аксональном CIDP в 1983 году, сообщив о двух случаях хронической рецидивирующей полирадикулоневропатии, в которых биопсия нерва показала дегенерацию аксонов и плазмаферез неэффективен в отличие от В трех случаях биопсия нерва показала демиелинизацию и плазмаферез.19 С тех пор, согласно данным поиска PubMed, было зарегистрировано 16 полностью описанных случаев аксонального CIDP.19–25 28–30 Два случая были исключены из-за электродиагностической характеристики демиелинизации: 25 м / с в моторном NCV и 8 мс в латентном состоянии в срединном нерве. демиелинизация при биопсии нерва в случае Жюльена и блокада проводимости в случае Катаджи.22 30 Таким образом, здесь проанализировано 14 случаев. Четырнадцать пациентов были взрослыми> 17 лет и в основном мужчины (шесть женщин). Все они имели историю симптомов от 2 месяцев до 5 лет.У одного пациента в анамнезе был СГБ до рецидива нейропатии. В семи случаях была моторная невропатия, в шести — моторно-сенсорная нейропатия и в одном — сенсорная нейропатия. ЦСЖ показал высокое содержание белка в 10 из 12 протестированных случаев и увеличение количества клеток в 2. Антитело GM1 было отрицательным в пяти испытанных случаях. Биопсия нерва в семи случаях показала дегенерацию аксонов в пяти случаях и отсутствие воспалительных клеток. Иммунотерапия показала улучшение в 10 из 13 пролеченных случаев: полное выздоровление в 4 случаях. В течение периода наблюдения в шести случаях произошел рецидив.Таким образом, по определению, 10 случаев зарегистрированного аксонального CIDP имели IR-CAP.
Вскрытие показало серьезную потерю аксонов в передних корешках и периневральную периваскулярную лимфоцитарную инфильтрацию в смешанных нервах и корешках спинного мозга в случае Гордона и умеренную потерю клеток в ганглиях задних корешков, но без воспалительных клеток или демиелинизации в нервном корешке в случае Жюльена. 25 В случае Жюльена было проведено вскрытие через год после эпизода невропатии. 22 Таким образом, по крайней мере в одном случае была задокументирована «воспалительная полирадикулопатия».25
Предлагаемые диагностические критерии CIAP
Что касается диагностических критериев CIAP, мы предлагаем три обязательных критерия, как описано во вставке 2, все из которых были выполнены в наших 33 случаях IR-CAP. Таким образом, их можно использовать в качестве руководящих принципов для иммунотерапии пациентов с CIAP.
Вставка 2Предлагаемые диагностические критерии хронической воспалительной аксональной нейропатии
Диагноз хронической воспалительной аксональной полинейропатии был поставлен при соблюдении всех трех следующих обязательных критериев:
-
Приобретенная, хроническая прогрессирующая или рецидивирующая симметричная или асимметричная полинейропатия с длительностью прогрессирования> 2 месяцев.
-
Электрофизиологические доказательства аксональной невропатии по крайней мере двух нервов без каких-либо доказательств «строгих критериев демиелинизации» (вставка 1).
-
Один из двух критериев поддержки: a или b.
-
Высокий белок ЦСЖ (> 55 мг / дл) или
-
Воспалительная аксональная нейропатия при биопсии нерва, за исключением диабетической или васкулитной нейропатии.
-
Первый критерий относится к клиническим признакам прогрессирования невропатии с продолжительностью более 2 месяцев.Это идентично клиническим признакам в критериях CIDP 1991 ANA и EFNS / PNS 2010.10 31 Это явно исключает GBS с продолжительностью менее 4 недель и подострую воспалительную демиелинизирующую полинейропатию с продолжительностью 4-8 недель8.
Второй критерий — это основное различие между CIAP и CIDP: электрофизиологическое доказательство аксональной невропатии, определяемое как аномальная нервная проводимость без каких-либо доказательств демиелинизации в любой нервной проводимости. Мы приняли критерии демиелинизации UAB, которые основаны на «средних значениях», а не на «нижнем пределе» в других системах.3 Мы предпочитаем средние значения, потому что они хорошо установлены и опубликованы. Напротив, нижние пределы четко не определены и четко не опубликованы. Независимо от нижнего предела, все наши случаи не соответствовали критериям демиелинизации, установленным Объединенной целевой группой Руководства EFNS / PNS10.
Третий критерий отражает «воспалительную природу» невропатии. «Воспаление» подтверждается высоким содержанием белка в спинномозговой жидкости или воспалительными клетками в биопсии нерва. Мы придерживались этой точки зрения, что высокий уровень белка в спинномозговой жидкости представляет воспалительную полирадикулопатию, наблюдаемую при GBS и CIDP.11 12 Воспалительные клетки были зарегистрированы в замороженных и парафиновых срезах биопсированного нерва.7 Чтобы соответствовать третьему критерию диагностических критериев CIAP, в восьми случаях потребовалась биопсия нерва в настоящем исследовании: отсутствие теста CSF в одном и нормальный белок CSF в Семь. Несмотря на то, что биопсия нерва является инвазивной, мы считаем, что она показана в этих случаях с учетом потенциального ответа на иммунотерапию при CIAP. Мы исключили другие известные причины воспалительной аксональной нейропатии, включая диабетическую и васкулитную невропатию, из третьего критерия.16 26 27
Если у кого-то нет доступа к биопсии нерва, мы предлагаем использовать любые клинические и спинномозговые данные, указывающие на «CIDP» и связанную с ним гаммопатию, в качестве практических рекомендаций для иммунотерапии. К ним относятся: предыдущий эпизод невропатии, предшествующие события, поражение черепных нервов, дыхательная недостаточность, слабость проксимальных мышц, высокий уровень белка спинномозговой жидкости и гаммопатия. Если мы будем использовать эти практические рекомендации для иммунотерапии, то иммунотерапия была бы предложена всем пациентам с IR-CAP, кроме одного в настоящем исследовании.Ответ на иммунотерапию при невропатии, связанной с гаммопатией, хорошо известен.32
Периферическая нейропатия: дифференциальная диагностика и лечение
Периферические нервы состоят из пучков длинных нейрональных аксонов, выходящих из центральной нервной системы (ЦНС). Некоторые периферические нервы обернуты миелиновой оболочкой, генерируемой шванновскими клетками, тогда как другие не миелинизированы. Периферические нервы выполняют различные моторные, сенсорные и вегетативные функции. Термин периферическая невропатия обычно используется для описания симметричного и универсального повреждения соседних нервов.Повреждение и клинические проявления обычно локализуются дистально с проксимальным прогрессированием. Некоторые заболевания могут повредить периферические нервы и вызвать периферическую невропатию; Важно отличать реальную невропатию от других расстройств, которые могут иметь сходные клинические проявления.
Эпидемиология
По оценкам одного исследования, распространенность периферической невропатии в условиях семейной медицины составляет 8 процентов у лиц 55 лет и старше1. Распространенность среди населения в целом может достигать 2.4 процента2. Исследование на уровне сообщества оценило распространенность периферической нейропатии у пациентов с сахарным диабетом 2 типа в 26,4 процента3.
Диагноз
Периферическая невропатия может быть вызвана различными системными заболеваниями, токсическим воздействием, лекарствами и т.д. инфекции и наследственные заболевания (таблица 1). Наиболее частыми излечимыми причинами являются диабет, гипотиреоз и дефицит питательных веществ.
Просмотр / печать таблицы
Таблица 1.Причины периферической нейропатии
| Причина | Тип невропатии | Комментарии | Лабораторные исследования | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Заболевания | 6 A | В основном сенсорный | Тест на вирус иммунодефицита человека | |||||||
| Карцинома (паранеопластический синдром) | A | -Hu, анти-Yo, анти-Ri, анти-Tr, анти-Ма и антитела против CV2) | ||||||||
| Хроническое заболевание печени | M | В основном демиелинизирующее, особенно при вирусном гепатите | Печеночные трансаминазы, билирубин, альбумин и щелочной уровни фосфатазы | |||||||
| Критическая нейропатия | A | Обычно острый или подострый | Специфических лабораторных исследований нет | |||||||
|
| 918 03 Сахарный диабет 03 Сахарный диабет 03 ; может преобладать аксональный Уровень глюкозы в крови натощак, тест на толерантность к глюкозе, уровень A1C | |||||||||
| Терминальная стадия почечной недостаточности | A | — | Уровни креатинина в сыворотке крови и мочевины | |||||||
| Гипотиреоз | A | Обычно острый или подострый, но может быть хроническим | Уровень тиреотропного гормона | |||||||
| 88 0 03 Обычно сенсорные | Фенольные антитела к гликолипиду-1, биопсия кожи | |||||||||
| Болезнь Лайма | A | — | 000 00 6000 6
00 00 900800 M | В основном аксональные | Общий анализ крови, визуализация | |||||
| Моноклональная гаммопатия | Обычно хроническая | Электрофорез белков мочи и сыворотки с иммунофиксацией | 0 | 0 | 0 | 0Обычно сенсорная | ||||
| Множественная миелома | M | Преобладает повреждение аксонов после лечения | ||||||||
| остеосакса 18 | Может иметь некоторое повреждение аксонов | |||||||||
| Моноклональная гаммапатия неустановленного значения | ||||||||||
| IgM 88 | D | Наиболее распространенные; может иметь некоторое повреждение аксонов | ||||||||
| IgG или IgA | M | Часто преобладают демиелинизирующие признаки | ||||||||
| 3000 | ||||||||||
| 3 Порфирия Острый | Титры порфирина | |||||||||
| Сифилис | A | — | Быстрый плазменный реагин, ВДРЛ, дефицит спинномозговой жидкости 4 4 4 | A | Сенсорная чувствительность больше, чем двигательная | Витамин B 6 уровень | ||||
| Витамин B 12 дефицит | A10 8 Перипатия верхняя двигательные нейронные знаки 9000 3 | СВС; витамин B 12 и уровни гомоцистеина; Тест с метилмалоновой кислотой | ||||||||
| Лекарственные средства * | ||||||||||
| Амиодарон (кордарон) | M | В основном аксональный с сенсомоторным | 9000len88 9008 | 9000len88 ) | D | Может иметь некоторое повреждение аксонов | ||||
| Дигоксин | A | В основном сенсорный | 983 00 | 983 | Сенсорно-моторный | |||||
| Гидралазин | A | В основном сенсорный | ||||||||
| Изониазид |
|
| 9180 6 Литий | A | Сенсормотор | |||||
| Метронидазол (Flagyl) | A | 02 В основном сенсорный | 9182 A | Двигатель | ||||||
| Нитрофурантоин (Фурадантин) | A |
Sensorimotor | ||||||||
| В основном сенсорный | ||||||||||
| Прокаинамид (Пронестил) | D | Может иметь некоторое повреждение аксонов | ||||||||
| Основное 00 A 910 910 910 910 00 910 918 910 910 | 9 0083 | |||||||||
| Винкристин (Онковин) | A | Сенсорно-моторный | ||||||||
| Витамин B 6 избыток | A 8 9188 918 СенсорныйГенетические нарушения † | |||||||||
| Болезнь Шарко-Мари-Тута | Генетическое тестирование | |||||||||
| Тип 1 | D 03 8 Также называется | |||||||||
| Тип 2 | A | Также называется HMSN-II | ||||||||
| Метахроматическая лейкодистрофия 88 | 000 8 | 000 8 | 000 | |||||||
| Невропатия с нарушением функций y к сдавленным параличам | D | — | ||||||||
| Болезнь Рефсума | D | Также называется HMSN-IV | 00 | 00 | ||||||
| Дифтерийный токсин | D | Острое проявление | Гистопатология | |||||||
| Этанол (спирт) |
03 0
03 лабораторный тест | |||||||||
| Тяжелые металлы (e.g., мышьяк, свинец, ртуть, золото) | A | Свинец и ртуть в основном вызывают моторную невропатию | 24-часовой сбор мочи для определения титров тяжелых металлов | |||||||
| Причины мышьяка сенсомоторная нейропатия | ||||||||||
| Золото может вызывать некоторую демиелинизацию | ||||||||||
| Органофосфаты | A | 9002 9183 Практический лабораторный тест 03 9002 | Столбняк | A | Двигатель; острое предлежание | Никаких специальных или практических лабораторных тестов | ||||
| Тиковый паралич | A | Двигатель; острое проявление | Специфических или практических лабораторных исследований нет | |||||||
| Другие причины | ||||||||||
| Идиопатическая полинейропатия | A | Диагноз исключения; обычно хронический | Без лабораторных исследований | |||||||
Причины периферической нейропатии
| Причина | Тип невропатии | Комментарии | Лабораторные исследования | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Заболевания | ||||||||||
| Основное 9188 03 003003 | Тест на вирус иммунодефицита человека | |||||||||
| Карцинома (паранеопластический синдром) | A | Обычно сенсорная | Паранеопластическая панель (анти-Hu, анти-Yo) -Tr, анти-Ма и антитела против CV2) | |||||||
| Хроническое заболевание печени | M | В основном демиелинизирующее, особенно при вирусном гепатите | Печеночные трансаминаза, альбумин, билирубин уровни щелочной фосфатазы | |||||||
| Критическая нейропатия | A | Обычно острая или подострая | Специфических лабораторных исследований нет | |||||||
| Сахарный диабет | M | Хронический; может преобладать аксональный | Уровень глюкозы в крови натощак, тест на толерантность к глюкозе, уровень A1C | |||||||
| Терминальная стадия почечной недостаточности | A | — | Уровни креатинина в сыворотке крови и мочевины | |||||||
| Гипотиреоз | A | Обычно острый или подострый, но может быть хроническим | Уровень тиреотропного гормона | |||||||
| 88 0 03 Обычно сенсорные | Фенольные антитела к гликолипиду-1, биопсия кожи | |||||||||
| Болезнь Лайма | A | — | 000 00 6000 6
00 00 900800 M | В основном аксональные | Общий анализ крови, визуализация | |||||
| Моноклональная гаммопатия | Обычно хроническая | Электрофорез белков мочи и сыворотки с иммунофиксацией | 0 | 0 | 0 | 0Обычно сенсорная | ||||
| Множественная миелома | M | Преобладает повреждение аксонов после лечения | ||||||||
| остеосакса 18 | Может иметь некоторое повреждение аксонов | |||||||||
| Моноклональная гаммапатия неустановленного значения | ||||||||||
| IgM 88 | D | Наиболее распространенные; может иметь некоторое повреждение аксонов | ||||||||
| IgG или IgA | M | Часто преобладают демиелинизирующие признаки | ||||||||
| 3000 | ||||||||||
| 3 Порфирия Острый | Титры порфирина | |||||||||
| Сифилис | A | — | Быстрый плазменный реагин, ВДРЛ, дефицит спинномозговой жидкости 4 4 4 | A | Сенсорная чувствительность больше, чем двигательная | Витамин B 6 уровень | ||||
| Витамин B 12 дефицит | A10 8 Перипатия верхняя двигательные нейронные знаки 9000 3 | СВС; витамин B 12 и уровни гомоцистеина; Тест с метилмалоновой кислотой | ||||||||
| Лекарственные средства * | ||||||||||
| Амиодарон (кордарон) | M | В основном аксональный с сенсомоторным | 9000len88 9008 | 9000len88 ) | D | Может иметь некоторое повреждение аксонов | ||||
| Дигоксин | A | В основном сенсорный | 983 00 | 983 | Сенсорно-моторный | |||||
| Гидралазин | A | В основном сенсорный | ||||||||
| Изониазид |
|
| 9180 6 Литий | A | Сенсормотор | |||||
| Метронидазол (Flagyl) | A | 02 В основном сенсорный | 9182 A | Двигатель | ||||||
| Нитрофурантоин (Фурадантин) | A |
Sensorimotor | ||||||||
| В основном сенсорный | ||||||||||
| Прокаинамид (Пронестил) | D | Может иметь некоторое повреждение аксонов | ||||||||
| Основное 00 A 910 910 910 910 00 910 918 910 910 | 9 0083 | |||||||||
| Винкристин (Онковин) | A | Сенсорно-моторный | ||||||||
| Витамин B 6 избыток | A 8 9188 918 СенсорныйГенетические нарушения † | |||||||||
| Болезнь Шарко-Мари-Тута | Генетическое тестирование | |||||||||
| Тип 1 | D 03 8 Также называется | |||||||||
| Тип 2 | A | Также называется HMSN-II | ||||||||
| Метахроматическая лейкодистрофия 88 | 000 8 | 000 8 | 000 | |||||||
| Невропатия с нарушением функций y к сдавленным параличам | D | — | ||||||||
| Болезнь Рефсума | D | Также называется HMSN-IV | 00 | 00 | ||||||
| Дифтерийный токсин | D | Острое проявление | Гистопатология | |||||||
| Этанол (спирт) |
03 0
03 лабораторный тест | |||||||||
| Тяжелые металлы (e.g., мышьяк, свинец, ртуть, золото) | A | Свинец и ртуть в основном вызывают моторную невропатию | 24-часовой сбор мочи для определения титров тяжелых металлов | |||||||
| Причины мышьяка сенсомоторная нейропатия | ||||||||||
| Золото может вызывать некоторую демиелинизацию | ||||||||||
| Органофосфаты | A | 9002 9183 Практический лабораторный тест 03 9002 | Столбняк | A | Двигатель; острое предлежание | Никаких специальных или практических лабораторных тестов | ||||
| Тиковый паралич | A | Двигатель; острое проявление | Специфических или практических лабораторных исследований нет | |||||||
| Другие причины | ||||||||||
| Идиопатическая полинейропатия | A | Диагноз исключения; обычно хронический | Лабораторных исследований нет | |||||||
ИСТОРИЯ И ФИЗИЧЕСКОЕ ОБСЛЕДОВАНИЕ
Когда у пациента появляются симптомы дистального онемения, покалывания и боли или слабости, первым шагом является определение того, являются ли симптомы результатом периферическая невропатия или поражение ЦНС, а также вовлечен ли один нервный корешок, несколько нервных корешков или периферическое нервное сплетение.Поражения ЦНС могут быть связаны с другими особенностями, такими как затруднение речи, двоение в глазах, атаксия, поражение черепных нервов или, в случае миелопатии, нарушение функций кишечника и мочевого пузыря. Рефлексы глубоких сухожилий обычно оживленные, а мышечный тонус спастический. Поражения корешков периферических нервов обычно асимметричны, следуют дерматомному паттерну сенсорных симптомов и могут сопровождаться болью в шее и пояснице. Поражения сплетения асимметричны с сенсомоторным поражением нескольких нервов на одной конечности.
Для проверки вибрационных ощущений в конечностях следует использовать камертон 128 Гц. Потеря чувствительности (включая вибрацию, проприоцепцию, температуру и ощущения укола булавкой) в дистальных отделах конечностей предполагает периферическую невропатию, как и градиент рефлекторного возбуждения от дистального к проксимальному отделу.
После того, как поражение было локализовано на периферических нервах, следующим шагом является определение этиологии и исключение потенциально поддающихся лечению причин, таких как приобретенные токсические, пищевые, воспалительные или иммуноопосредованные демиелинизирующие расстройства.Кроме того, невропатии должны характеризоваться началом и хронологией симптомов, типом и степенью поражения, а также типом вовлеченных нервных волокон (т. Е. Сенсорными, моторными или вегетативными).
На ранних стадиях периферической невропатии у пациентов обычно появляются прогрессирующие симптомы, включая потерю чувствительности, онемение, боль или жжение в дистальных отделах конечностей при распределении «носки и перчатки». Со временем онемение может распространяться в проксимальном направлении, и может возникнуть небольшая дистальная мышечная слабость и атрофия.При расстройствах, вызывающих острую периферическую невропатию, например, вызванных токсическим воздействием, пациенты могут иметь сходные, но более скоротечные симптомы, и преобладать боль; симптомы также обычно имеют более быстрое прогрессирование. При других расстройствах, таких как острое воспалительное демиелинизирующее расстройство (например, синдром Гийена-Барре) и хроническая воспалительная демиелинизирующая полинейропатия, обычно преобладает слабость, а не потеря чувствительности, что может быть самым ранним признаком заболевания.
Наличие невропатических симптомов, снижение рефлексов голеностопных суставов и снижение ощущений в дистальных отделах, независимо от слабости и атрофии дистальных мышц, делает диагноз периферической невропатии вероятным.4 Изолированное присутствие нейропатических симптомов или снижение рефлексов голеностопного сустава менее важно для диагностики. Некоторые причины периферической невропатии характеризуются мононевропатией, некоторые затрагивают несколько нервов, а другие имеют вегетативную дисфункцию или выраженность боли (Таблица 2).
Просмотр / печать таблицы
Таблица 2.Причины периферической нейропатии на основе клинических данных
| Состояния, вызывающие мононевропатию | |||||
| Острый (связанный с травмой нерва) | |||||
| Хронический | |||||
| Заболевания, вызывающие множественную мононевропатию | |||||
| Острый | |||||
| Сахарный диабет * | |||||
| 918окал10 | |||||
| Хронические | |||||
| Синдром приобретенного иммунодефицита | |||||
| Проказа * | |||||
| 00
| 02 Состояния, вызывающие невропатию с вегетативными особенностями |||||
| Алкоголизм | |||||
| Амилоидоз | |||||
| Невропатия, связанная с химиотерапией | |||||
|
03Тяжелый металл, токсичность | |||||
| Порфирия | |||||
| Первичная дизавтономия | |||||
| Витамин B 12 дефицит | |||||
| Состояния, вызывающие болезненную невропатию | |||||
|
0303 Алкоголизм | |||||
| Химиотерапия (токсичность тяжелых металлов) | |||||
| Диабет | |||||
| Идиопатическая полинейропатия | |||||
| Порфирия | |||||
| Паранеопластический синдром | |||||
Причины периферической нейропатии на основании клинических данных
| Состояния, вызывающие мононевропатию | ||||
| Острые (связанные с травмой) | ||||
| Хронические (защемление нерва) | 84 0884, вызывающие множественные заболевания | |||
| Острый | ||||
| Сахарный диабет * | ||||
| Мультифокальная моторная нейропатия | ||||
9004 033 974 974 974 974 | 974 974 | Синдром приобретенного иммунодефицита | ||
| Проказа * | ||||
| Саркоидоз | ||||
| Состояния, вызывающие невропатию с вегетативными особенностями 90 003 | ||||
| Алкоголизм | ||||
| Амилоидоз | ||||
| Невропатия, связанная с химиотерапией | ||||
| Диабет | ||||
| Первичная дизавтономия | ||||
| Дефицит витамина B 12 | ||||
| Состояния, вызывающие болезненную невропатию | ||||
| Алкоголизм | ||||
|
| ||||
| токсичность металлов) | ||||
| Диабет | ||||
| Идиопатическая полинейропатия | ||||
| Порфирия | ||||
| Паранеопластический синдром | ||||
ДИАГНОСТИЧЕСКОЕ ТЕСТИРОВАНИЕ
Оценка пациента с периферической невропатией начинается с простых анализов крови, включая общий анализ крови, комплексный метаболический профиль, измерение скорости оседания эритроцитов и уровня глюкозы в крови натощак, витамина B 12 и стимуляторов щитовидной железы. уровни гормонов5 (Рисунок 1).Дополнительные тесты, если есть клинические показания, могут включать паранеопластическую панель для оценки скрытой злокачественности; антимиелин-ассоциированные гликопротеиновые антитела для оценки сенсомоторной невропатии; антиганглиозидные антитела; криоглобулины; анализ спинномозговой жидкости (CSF) для оценки хронической воспалительной демиелинизирующей невропатии; антисульфатидные антитела для оценки аутоиммунной полинейропатии; и генетическое тестирование при подозрении на наследственную периферическую невропатию (Таблица 3).
Просмотр / печать Рисунок
Диагноз пациента с подозрением на периферическую невропатию
Рисунок 1.
Обращение к пациенту с периферической невропатией. (ANA = антинуклеарные антитела; C-ANCA = цитоплазматические антинейтрофильные цитоплазматические антитела; ВИЧ = вирус иммунодефицита человека; P-ANCA = перинуклеарные антинейтрофильные цитоплазматические антитела; RPR = быстрый плазменный реагин; SPEP = электрофорез белков сыворотки; UPEP = электрофорез белков мочи. )
Диагностика пациента с подозрением на периферическую нейропатию
Рисунок 1.
Обращение к пациенту с периферической невропатией.(ANA = антинуклеарные антитела; C-ANCA = цитоплазматические антинейтрофильные цитоплазматические антитела; ВИЧ = вирус иммунодефицита человека; P-ANCA = перинуклеарные антинейтрофильные цитоплазматические антитела; RPR = быстрый плазменный реагин; SPEP = электрофорез белков сыворотки; UPEP = электрофорез белков мочи. )
Просмотреть / распечатать таблицу
Таблица 3.